
【题目】普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型)。
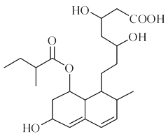
下列关于普伐他汀的性质描述正确的是 ( )
A. 能与FeCl3溶液发生显色反应
B. 该物质的分子式为C23H38O7
C. 能发生加成、取代、消去反应,能使酸性KMnO4溶液褪色
D. 1mol该物质最多可与1molNaOH反应
科目:高中化学 来源: 题型:
【题目】现有下列物质:① N2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl。
(1)只由非极性键构成的物质是__________________(填编号)。
(2)由离子键和极性键构成的物质是_______________。
(3)⑤H2O2的电子式为:_________________。
(4)用电子式表示⑥MgF2的形成过程:______________。
(5)下列说法不正确的是________。
①共价化合物中含共价键,也可能含离子键
②因为H2CO3酸性<H2SO3酸性,所以非金属性C<S
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤熔融状态能导电的物质是离子化合物
⑥由分子组成的化合物中一定存在共价键
A. ①③⑤ B. ①②⑥ C. ①②④⑤ D. ①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是

A. 与金属钠反应时,键①断裂
B. 在加热和Cu催化下与O2反应时,键①、③断裂
C. 与浓硫酸共热发生消去反应时,键②③断裂
D. 与乙酸、浓硫酸共热发生酯化反应时,键①断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的图示与对应的叙述不相符的是( )
A.图1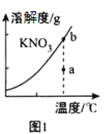 表示KNO3的溶解度曲线,图中a点表示的溶液通过恒温蒸发可以达到b点
表示KNO3的溶解度曲线,图中a点表示的溶液通过恒温蒸发可以达到b点
B.图2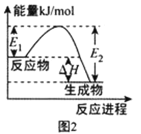 表示某一放热反应,若使用合适的催化剂,
表示某一放热反应,若使用合适的催化剂,![]() 、
、![]() 均减小,
均减小,![]() 不变
不变
C.图3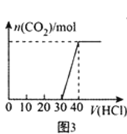 表示向Na2CO3和NaOH的混合溶液中滴加稀盐酸时,产生CO2的情况
表示向Na2CO3和NaOH的混合溶液中滴加稀盐酸时,产生CO2的情况
D.图4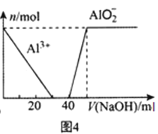 表示向100mL0.1mol/L的AlCl3和0.1mol/L的(NH4)2SO4混合溶液中滴加1mol/L的NaOH溶液时n(Al3+)和n(AlO2-)的变化情况
表示向100mL0.1mol/L的AlCl3和0.1mol/L的(NH4)2SO4混合溶液中滴加1mol/L的NaOH溶液时n(Al3+)和n(AlO2-)的变化情况
查看答案和解析>>
科目:高中化学 来源: 题型:
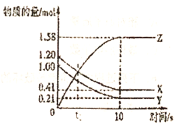
【题目】一定温度下,在![]() 的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
A.![]() 后,该反应停止进行
后,该反应停止进行
B.反应的化学方程式为:![]()
C.在t1时刻,正反应速率等于逆反应速率
D.反应前![]() 内,以Z表示的平均反应速率为
内,以Z表示的平均反应速率为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①—⑨在表中的位置,回答问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中⑧元素单质可用作________。
(2)③、④、⑧的原子半径最小是________(用元素符号回答)。
(3)⑤、⑥、⑦的最高价氧化物对应的水化物中,碱性最强的是________(用化学式回答)。
(4)②、③、④的气态氢化物中,稳定性最弱的是________(用化学式回答)(5)②和③按原子数![]() 形成的化合物的电子式为________,该晶体气化的过程中克服的微粒间作用力为________。
形成的化合物的电子式为________,该晶体气化的过程中克服的微粒间作用力为________。
(6)③和⑧形成的化合物属于________(填“离子化合物”或“共价化合物”),该晶体属于________晶体(填“离子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高价氧化物的水化物互相反应的化学方程式为:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D都是周期表中的短周期元素,它们的核电荷数依次增大。A原子、C原子的L能层中都有两个未成对的电子,C、D同主族。E、F都是第四周期元素,E原子核外有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号为____,D基态原子含有_____个未成对电子。
(2)E2+的价层电子排布图是_______,F原子的电子排布式是_____。
(3)A的最高价氧化物对应的水化物分子结构式为____,其中心原子采取的轨道杂化方式为____,B的气态氢化物的VSEPR模型为_____。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的结构式为____。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6。甲的水溶液可以用于实验室中E2+的定性检验,检验E2+的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组对SO2的性质进行探究。用如图所示装置进行实验。

(1)A的装置中浓硫酸的作用是___。
(2)请将A方框中的装置补充完整___。
(3)实验过程中,说明SO2与水反应生成了酸的实验现象是__。
(4)D的装置中发生反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体化合物 X 由 3 种元素组成。某学习小组进行了如下实验:
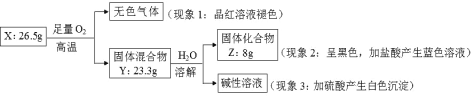
请回答:
(1)由现象 1 得出化合物 X 含有____元素(填元素符号),X 的化学式_____。
(2)固体混合物 Y 的成分_____(填化学式)。
(3)实验室常将氨气(NH3)通过红热的黑色固体化合物 Z 制备氮气,该反应的化学方程式是___,当有28克氮气生成时转移的电子的物质的量为______mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com