
【题目】氮元素可形成多种化合物,在工业生产中具有重要价值。请回答下列问题:
(1)一定温度下,将一定量的N2和H2充入固定体积的密闭容器中进行合成氨反应。
①下列描述能说明该可逆反应达到化学平衡状态的有__。
A.容器内气体的密度不变
B.c(N2):c(H2):c(NH3)=1:3:2
C.容器内的压强不变
D.相同时间内有3molH-H键断裂,有6molN-H键形成
E.3v正(H2)=2v逆(NH3)
F.容器内气体的平均相对分子质量不变
②恒温恒压条件下,为提高合成氨反应中N2和H2的利用率,可采用的方法__(一种即可)。
(2)一定温度下,2L密闭容器中充入0.40molN2O4,发生反应:N2O4(g)![]() 2NO2(g),一段时间后达到平衡,测得数据如下:
2NO2(g),一段时间后达到平衡,测得数据如下:
时间/s | 20 | 40 | 60 | 80 | 100 |
c(NO2)/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
①20s内,v(NO2)=__,该温度下反应的化学平衡常数数值为__。
②升高温度时,气体颜色加深,则正反应是__(填“放热”或“吸热”)反应。
③相同温度下,若开始向该容器中充入0.40mo1NO2,则达到平衡后:c(NO2)__0.15mol/L(填“>”、“=”或“<”)
【答案】C、F 移出NH3 6×10-3mol/(L·s) 1.8 吸热 >
【解析】
(1)①可逆反应达到平衡状态时,正逆反应速率相等,反应体系中各物质的物质的量不变、物质的量浓度不变、百分含量以及由此引起的一系列物理量不变;
(2)①根据表格数据找出平衡时各物质的浓度,计算平衡常数;
③利用等效平衡思想分析。
(1)①A.气体质量和体积不变,容器内气体的密度始终不变,不能说明反应达到平衡状态,故A不选;
B.平衡时各物质的浓度不再改变,但浓度之比不一定等于计量数之比,与反应物投料及转化率有关,故B不选;
C.该反应前后气体系数之和不同,未平衡时气体的物质的量会发生变化,而容器恒容,所以容器内压强会变,容器内的压强不变说明反应达到平衡状态,故C选;
D.相同时间内有3molH-H键断裂,有6mol N-H键形成,二者描述的都是正反应速率,只要反应进行,该关系就存在,故D不选;
E.速率之比等于化学方程式计量数之比,为正反应速率之比,2v正(H2)=3v逆(NH3)能说明反应达到平衡状态,但3v正(H2)=2v逆(NH3)不能证明反应达到平衡状态,故E不选;
F.反应前后气体质量不变,气体物质的量变化,所以未平衡时容器内气体的平均相对分子质量会变,不变时说明反应达到平衡状态,故F选;
综上所述选C、F;
②恒温恒压条件下,可以及时移走生成的NH3使平衡正向移动,增大反应物的利用率;
(2)①20s内,v(NO2)=![]() = 6×10-3mol/(L·s);
= 6×10-3mol/(L·s);
根据表格数据可知80s时反应已经达到平衡,此时△c(NO2)=0.30mol/L,根据方程式可知△c(N2O4)=0.15mol/L,初始投料0.40molN2O4,容器体积为2L,所以平衡时c(N2O4)=0.05mol/L,则该温度下平衡常数为![]() =1.8;
=1.8;
②升高温度颜色加深,说明向生成NO2的方向移动,即正向移动,所以正反应为吸热反应;
③若开始向该容器中充入0.40mo1NO2,极限转化相当于充入0.20molN2O4,假如二者达到等效平衡,则c(NO2)=0.15mol/L,但实际上由于气体的物质的量减少,容器内压强降低,平衡会在等效平衡的基础上向生成NO2的方向移动,所以c(NO2)>0.15mol/L。


科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。
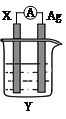
请回答下列问题:
(1) 电极X的材料是______;电解质溶液Y是________;
(2) 银电极为电池的__________极,发生的电极反应式为____________;X电极上发生的电极反应为______反应;(填“氧化”或“还原”)
(3) 外电路中的电子_________(填“流出”或“流向”)Ag电极。
(4) 当有1.6 g铜溶解时,银棒增重______ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某华人科学家和他的团队研发出“纸电池” (如图)。这种一面镀锌、一面镀二氧化锰的超薄电池在使用印刷与压层技术后,变成一张可任意裁剪大小的“电纸”,厚度仅为0.5毫米,可以任意弯曲和裁剪。纸内的离子“流过”水和氧化锌组成电解液,电池总反应式为: Zn+2MnO2+H2O=ZnO+2MnO(OH)。下列说法正确的是

A.该电池的正极材料为锌
B.该电池反应中二氧化锰发生了氧化反应
C.电池的正极反应式为2MnO2 +2H2O+2e-= 2MnO(OH)+2OH-
D.当有0.1mol锌溶解时,流经电解液的电子数为1.204×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是25 ℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为_______________________________________。
(2)向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=________。
(3)向碳酸钠溶液中滴加少量氯水的离子方程式为_____________________。
(4)若0.1mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(CH3COO-)=_______________mol·L-1(填精确计算结果)。
(5) 将CH3COOH溶液与大理石反应所产生的标况下44.8L气体全部通入到2L 1.5mol/L的NaOH溶液中充分反应,则溶液中所有离子的物质的量浓度由大到小的顺序为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,N表示粒子数。下列叙述正确的是( )
A. 在标准状况下2.24LCCl4中含有的C—Cl键数为0.4NA
B. 将1mol Cl2通入水中,则N(HClO)+N(Cl)+N(ClO)=2NA
C. 将CO2通过Na2O2使其质量增加a g时,反应转移的电子数为aNA/14
D. 3.0g含甲醛(HCHO)的冰醋酸中含有的原子总数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国药学家屠哟哟因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖。青蒿素结构式如图所示,下列有关青蒿素研究的说法不正确的是( )
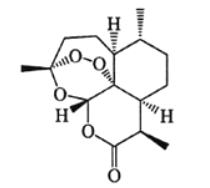
A.可使用质谱仪测出这个分子的相对分子质量,也可用紫外光谱确定这个分子的环状结构
B.提取过程中为防止破坏青蒿素结构,应避免高温,故采用低沸点溶剂乙酸进行萃取
C.青蒿素是脂溶性的,既可看作是醚类也可看作是酯类,既有氧化性又有还原性
D.元素分析仪可以确定青蒿素中是否含有C、H、O等元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合气体由两种气态烃组成。2.24L该混合气体完全燃烧后,得到4.48L二氧化碳(气体均已折算为标准状况)和3.6g水。则这两种气体可能是( )
A.CH4和C3H4B.CH4和C3H8
C.C2H6和C3H4D.C2H4和C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化钛是目前使用最广泛的白色颜料。工业上,以钛铁矿(主要成分为钛酸亚铁[FeTiO3],含有少量SiO2杂质)为原料制备二氧化钛的过程如下图所示。
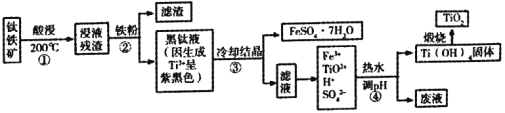
已知:①超过70℃TiO2+易水解;低于0℃ FeSO4·7H2O大量结晶。
②钛的化合价主要有+4价和+3价,其中Ti3+(紫黑色)还原性比Fe2+强
③有关氢氧化物开始沉淀的pH如下:
氢氧化物 | Ti(OH)4 | Ti(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀时的pH | 0.5 | 3.0 | 1.5 | 7.6 |
根据相关信息回答下列问题;
(1)酸浸过程选用的酸是__________。
(2)步骤①中生成Fe2+和TiO2+的化学反应方程式为__________。
(3)以下相关描述正确的是__________。
A 步骤②中加入铁粉,在防止Fe2+转化成Fe3+的同时也将部分TiO2+氧化成了Ti3+
B 步骤③中的降温结晶过程可以选择冰水混合物
C ③中发生了反应Fe3++ Ti3++H2O== Fe2++ TiO2++2H+
D 废液成分中有硫酸,可以循环利用
(4)步④中生成Ti(OH)4的离子方程式为__________,选择的pH范围是__________。
(5)证明步骤④中Ti (OH)4固体已经洗涤干净的方法是__________。
(6)钛酸锂(Li4Ti5O12)是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池总反应式为:LiXO2(s)+Li4Ti5O12(s)=Li1-aXO2+Li4+aTi5O12(s),则其负极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组说法均不正确的是( )
①CH3—CH=CH—C≡C—CF3 分子结构中最多有 4 个碳原子在一条直线上
②用催化加氢的方法可除去乙烷中混有的少量乙烯
③丁二烯和丁烯为同系物
④正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤14 g 乙烯和丙烯混合气体中的氢原子数为 2NA
⑥能够快速、微量、精确的测定相对分子质量的物理方法是核磁共振氢谱法
A.②③⑥B.①③⑥C.②③④D.③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com