
【题目】下列有关反应热的叙述中正确的是( ) ①已知2H2(g)+O2(g)═2H2O(g)△H=﹣483.6kJmol﹣1 , 则氢气的燃烧热为△H=﹣241.8kJmol﹣1
②由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
③X(g)+Y(g)═Z(g)+W(s)△H>0,恒温恒容条件下达到平衡后加入X,上述反应的△H增大
④已知:
共价键 | C﹣C | C═C | C﹣H | H﹣H |
键能/(kJmol﹣1) | 348 | 610 | 413 | 436 |
上表数据可以计算出 ![]() (g)+3H2(g)→
(g)+3H2(g)→ ![]() (g)的反应热;
(g)的反应热;
⑤由盖斯定律,推知在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量相等;
⑥25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量为碳的燃烧热.
A.①②③④
B.③④⑤
C.④⑤
D.⑥
【答案】D
【解析】解:①燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,氢气燃烧生成液态水,由热化学方程式可知,氢气的燃烧热<﹣241.8kJmol﹣1 , 故错误;②单质A转化为单质B是一个吸热过程,则B的能量比A的高,能量越高越不稳定,故错误;③一定条件下,反应热与平衡移动无关,与化学计量数与物质的状态有关,故错误;④反应热=反应物总键能﹣生成物总键能,由于苯环中不存在碳碳双键,不能计算反应热,故错误;⑤金刚石与石墨的结构不同,能量不相同,在相同条件下,金刚石或石墨燃烧生成1molCO2固体时,放出的热量不相等,故错误;⑥碳的燃烧热指:25℃,101kPa时,1mol碳完全燃烧生成CO2所放出的热量,故正确, 故选D.
①燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,氢气燃烧生成液态水;②能量越高越不稳定;③一定条件下,反应热与平衡移动无关,与化学计量数与物质的状态有关;④苯环中不存在碳碳双键;⑤金刚石与石墨的结构不同,能量不相同;⑥燃烧热指:25℃,101kPa时1mol物质完全燃烧生成稳定氧化物放出的热量.


 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】以下各组离子因发生氧化还原反应而不能大量共存的是( )
A. Ca2+、H+、SO42-、HCO3-B. H+、Fe2+、SO42-、 NO3-
C. Na+、Cu2+、Cl-、S2-D. Fe3+、K+、SCN-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛,请回答下列问题:
(1)相同条件下,pH相同的NH4Al(SO4)2中c(NH4+)(填“=”、“>”或“<”)NH4HSO4中c(NH4+).
(2)如图一是0.1molL﹣1电解质溶液的pH随温度变化的图象. 
①其中符合0.1molL﹣1 NH4Al(SO4)2的pH随温度变化的曲线是(填写字母);
②室温时,0.1molL﹣1 NH4Al(SO4)2中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)=
molL﹣1(填数值)
(3)室温时,向100mL 0.1molL﹣1 NH4HSO4溶液中滴加0.1molL﹣1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图二所示.试分析图中a、b、c、d四个点,水的电离程度最大的是;在c点,溶液中各离子浓度由大到小的排列顺序是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CMA(醋酸钙、醋酸镁固体的混合物)是高速公路的绿色融雪剂.以生物质废液﹣﹣木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)及白云石(主要成分MgCO3CaCO3 , 含SiO2等杂质)等为原料生产CMA的实验流程如图1: 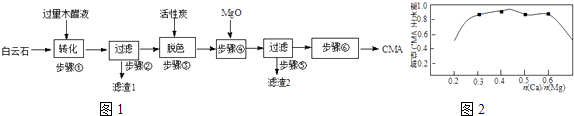
(1)步骤①发生的反应离子方程式为 .
(2)步骤②所得滤渣1的主要成分为(写化学式);步骤②所得滤液常呈褐色,颜色除与木醋液中含有少量的有色的焦油有关外,产生颜色的另一主要原因是 .
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪效果成正比)关系如图2所示,步骤④的目的除调节n(Ca):n(Mg)约为(选填:1:2;3:7;2:3)外,另一目的是 .
(4)步骤⑥包含的操作有、过滤、洗涤及干燥.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学电源的叙述错误的是( )
A.普通锌锰干电池中碳棒为正极
B.铅蓄电池中覆盖着PbO2的电极板是负极板
C.氢氧燃料电池的正极是通入氧气的那一极
D.碱性锌锰干电池的比能量和储存时间比普通锌锰干电池高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是乙醇燃料电池的实验装置图,下列有关说法一定正确的是( ) 
A.若用此装置给铁棒上镀上层银,则N电极改用铁电极,M电极改用银电极
B.甲池中负极的电极反应式为:CH3CH2OH﹣12e﹣+3H2O=2CO2+12H+
C.甲池KOH溶液中经过0.05mol电子时,理论上乙池中的M电极质量增加5.04g
D.M电极上的电极反应式为:Ag++e﹣=Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)配制时必须的玻璃仪器有:烧杯、玻璃棒、 、 。
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(3)下列配制的溶液浓度偏低的是 ;
A、称量NaOH时,砝码错放在左盘
B、向容量瓶中转移溶液时(实验步骤C)不慎有液滴洒在容量瓶外面
C、加蒸馏水时不慎超过了刻度线
D、定容时俯视刻度线
E、配制前,容量瓶中有少量蒸馏水
(4)某同学改用固体Na2CO3配制Na2CO3溶液的过程如图所示,其错误操作序号是 

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com