
过碳酸钠(2Na2CO4·3H2O)是一种新型高效固体漂白杀菌剂,它具有无臭、无毒、无污染的特点,被大量应用于洗涤、印染、纺织、造纸、医药卫生等领域中。依托纯碱厂制备过碳酸钠可降低生产成本,其生产流程如下:
试回答下列问题:
(1)过碳酸钠溶于水后所得溶液显 (填“酸性”、“碱性”或“中性”)。请用离子方程式表示:______________________。
(2)操作①需要的玻璃仪器有 (填写仪器名称)。
(3)工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。
①要检验工业纯碱中杂质的存在,最好选用下列试剂中的__________(选填序号)。
a. 氢氧化钡溶液 b. 稀硝酸 c. 硫氰化钾溶液 d. 硝酸银溶液
②检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若观察到 说明装置不漏气。
③装置A的作用是 ,装置C中的试剂为 。
④某同学认为在D装置后应再连接E装置(装有适当试剂),你认为是否必要? (选填“必要”或“不必要”),判断的理由是 。
(1) 碱性(1分) CO42– + H2O  HCO4– + OH–
HCO4– + OH–
(2)漏斗(1分) 烧杯(1分) 玻璃棒(1分)
(3) ①bd ②漏斗内的水面高于瓶内的水面,且保持一段时间不变 ③吸收空气中的CO2,避免干扰,并赶走装置中滞留的气体 浓硫酸(1分) ④必要(1分) 避免空气中的CO2进入D装置,提高实验的准确性
解析试题分析:(1)过碳酸钠大量用于洗涤,可推测其显碱性,因为过碳酸根离子水解呈碱性:CO42– + H2O  HCO4– + OH–。(2)从溶液中分离出晶体,在实验室应采用过滤的方法,过滤操作需要的玻璃仪器漏斗、烧杯、玻璃棒。(3)①检验纯碱中是否含量有NaCl杂质,应先加入AgNO3溶液,再加入过量的稀HNO3,若仍有白色溶液,说明溶液中含有Cl–,故选bd;②漏斗内的水面高于瓶内的水面,且保持一段时间不变,则说明装置不漏气;③本实验设计原理为通过测定生成的CO2的质量确定纯碱中Na2CO3的含量,所以B装置内滞留的气体应能被D装置中的碱石灰充分吸收,设计A装置的目的就是通过鼓入空气赶走B装置中滞留的气体,但又不能让空气中的CO2影响测定结果,因此A装置中所盛溶液必须能除去空气中的CO2,设计C装置的目的是除去CO2中混合的水蒸气,故装置A的作用是:吸收空气中的CO2,并赶走装置中滞留的气体,装置C中的试剂为:浓硫酸;④定量实验应尽量精确,减小误差,实验中需要称量的是实验前后D装置的质量,如果空气中的CO2进入D装置会造成实验误差,影响实验的精确度,所以D装置后必须连接一个E装置。
HCO4– + OH–。(2)从溶液中分离出晶体,在实验室应采用过滤的方法,过滤操作需要的玻璃仪器漏斗、烧杯、玻璃棒。(3)①检验纯碱中是否含量有NaCl杂质,应先加入AgNO3溶液,再加入过量的稀HNO3,若仍有白色溶液,说明溶液中含有Cl–,故选bd;②漏斗内的水面高于瓶内的水面,且保持一段时间不变,则说明装置不漏气;③本实验设计原理为通过测定生成的CO2的质量确定纯碱中Na2CO3的含量,所以B装置内滞留的气体应能被D装置中的碱石灰充分吸收,设计A装置的目的就是通过鼓入空气赶走B装置中滞留的气体,但又不能让空气中的CO2影响测定结果,因此A装置中所盛溶液必须能除去空气中的CO2,设计C装置的目的是除去CO2中混合的水蒸气,故装置A的作用是:吸收空气中的CO2,并赶走装置中滞留的气体,装置C中的试剂为:浓硫酸;④定量实验应尽量精确,减小误差,实验中需要称量的是实验前后D装置的质量,如果空气中的CO2进入D装置会造成实验误差,影响实验的精确度,所以D装置后必须连接一个E装置。
考点:本题为综合实验考查,主要考查实验原理、药品与仪器、基本操作、评价与设计等。


科目:高中化学 来源: 题型:实验题
偶氮苯是橙红色晶体,溶于乙醇,微溶于水,广泛应用于染料制造和橡胶工业,以硝基苯、镁粉和甲醇为原料制备偶氮苯的实验步骤如下:
步骤1:在反应器中加入一定量的硝基苯、甲醇和一小粒碘,装上冷凝管,加入少量镁粉,立即发生反应。
步骤2:等大部分镁粉反应完全后,再加入镁粉,反应继续进行,等镁粉完全反应后,加热回流30 min。
步骤3:将所得液体趁热倒入冰水中,并不断搅拌,用冰醋酸小心中和至pH为4~5,析出橙红色固体,过滤,用少量冰水洗涤。
步骤4:用95%的乙醇重结晶。
(1)步骤1中反应不需要加热就能剧烈进行,原因是________________。镁粉分两次加入而不是一次性全部加入的原因是___________________ _____________________________________________________。
(2)步骤3中析出固体用冰水洗涤的原因是________________。若要回收甲醇,实验所需的玻璃仪器除冷凝管、酒精灯、牛角管(应接管)和锥形瓶外还应有________________________________________________________________。
(3)取0.1 g偶氮苯,溶于5 mL左右的苯中,将溶液分成两等份,分别装于两个试管中,其中一个试管用黑纸包好放在阴暗处,另一个则放在阳光下照射。用毛细管各取上述两试管中的溶液点在距离滤纸条末端1 cm处,再将滤纸条末端浸入装有1∶3的苯环己烷溶液的容器中,实验操作及现象如下图所示: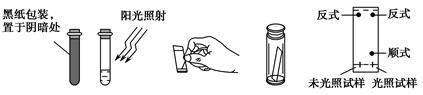
①实验中分离物质所采用的方法是________法。
②由实验结果可知:________________;利用该方法可以提纯反式偶氮苯。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某课外活动小组根据Mg与CO2的反应原理,探究Mg与NO2的反应及固体产物。该小组通过实验确认Mg能在NO2中燃烧,并对固体产物提出三种假设:
I.假设为:固体产物为MgO II.假设为:______________III.假设为:______________
请回答下列问题:资料信息:2NO2+2NaOH=NaNO3+NaNO2+H2O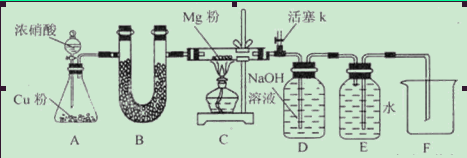
(1)如图连接好仪器,装药品前如何检验装置的气密性_____________________________
(2)装置B中盛装的干燥剂可以是(填序号)___________________
①浓硫酸 ②无水CaCl2 ③碱石灰 ④五氧化二磷
(3)开始打开活塞k,让A中反应进行一段时间,待C中充满红综色气体后,关闭活塞k,再点燃C处酒精灯,同时D中碱液盛的很满,这样做的目的是_________________________
(4)E中收集到的气体对氢气的相对密度是14,该气体是__________________
(5)实验得到固体残留物的质量是实验前Mg粉质量的1.5倍,则假设__________________成立。C中发生的化学反应方程式有_______________________________________________
(6)本实验中存在明显缺陷,改进措施是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用左下图所示装置模拟工业制取并收集ClO2。
(1)A中反应产物有K2CO3、ClO2和CO2等,请写出该反应的化学方程式: 。
(2)A必须添加温度控制装置,除酒精灯、烧杯外,还需要的玻璃仪器有 ,B也必须添加温度控制装置,应该是 (选填“冰水浴”或“热水浴”)装置。
(3)反应后在装置C中可得NaClO2溶液。已知NaClO2饱和溶液中在温度低于38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2。根据上图所示的NaClO2的溶解度曲线,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
① ;② ;③洗涤;④干燥。
(4)ClO2很不稳定,需随用随制,用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10 mL,稀释成100 mL试样;量取V1mL试样加入锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;此时发生的离子方程式为: ;
步骤3:加入淀粉指示剂,用c mol/L Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL。则原ClO2溶液的浓度为 g/L(用含字母的代数式表示)。
(已知2 Na2S2O3+I2= Na2S4O6+2NaI)
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子形式存在。实验室从海藻中提取碘的流程如下:
(1)指出提取碘的过程中有关实验操作的名称:
①为 ,③为 ;过程②中有关反应的离子方程式是 。
(2)提取碘的过程中可供选择的有机溶剂是( )
| A.甲苯、酒精 | B.四氯化碳、苯 | C.汽油、乙酸 | D.汽油、甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
实验室合成乙酸乙酯的步骤如下:在图甲的圆底烧瓶内加入乙醇、浓硫酸和乙酸,加热回流一段时间,然后换成图乙装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。




请回答下列问题:
(1)图甲中冷凝水从_________(a或b)进,图乙中B装置的名称为____________
(2)反应中加入过量的乙醇,目的是_________________________________________
(3)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
则试剂a是:____________, 试剂b是____________ , 分离方法III是___________。
(4)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯得到乙酸乙酯,在未用指示剂的情况下,他们都是先加NaOH溶液中和酯中过量的酸,然后用蒸馏法将酯分离出来。甲、乙两人蒸馏产物结果如下:甲得到了显酸性的酯的混合物,乙得到了大量水溶性的物质。丙同学分析了上述实验目标产物后认为上述实验没有成功。试解答下列问题:ks5u
① 甲实验失败的原因是:_______________________________________________
② 乙实验失败的原因是:_______________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
(1)为检验起始滤液中的Cl-,所用试剂除稀HNO3,还应有
(填化学式)
(2)试剂Ⅰ、Ⅱ、Ⅲ的化学式分别为 、 、
(3)步骤①和②中,所用的玻璃仪器除胶头滴管,还应有
(4)步骤①中,判断试剂Ⅰ已加入过量的方法是:
(5)某同学根据最终所得KCl晶体和原样品的质量求算出氯化钾样品的纯度,你认为其结果是否可靠?并说明理 (不考虑实验误差):
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某研究性学习小组将一定浓度的Na2CO3溶液滴入MgSO4溶液中得到白色沉淀。甲同学认为两者反应只生成MgCO3一种沉淀;乙同学认为这两者相互促进水解,只生成Mg(OH)2一种沉淀;丙同学认为生成MgCO3和Mg(OH)2两种沉淀。(查阅资料知:MgCO3和Mg(OH)2均不带结晶水)
(1)按照乙同学的理解Na2CO3溶液和MgSO4溶液反应的化学反应方程式为___________________;
在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①过滤②洗涤③干燥。
(2)请用下图所示装置,选择合适的实验装置和必要的试剂,证明沉淀物中只有碳酸镁。
①各装置连接顺序为__________________(用装置编号表示);
②装置C中装有试剂的名称是______________;
③能证明生成物中只有MgCO3的实验现象是_______。
(3)若Mg(OH)2和MgCO3两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。
实验结束时通入过量的空气的作用是______________________________。
A装置和E装置的共同作用是__________________________。
③实验过程中测定的数据有:W1:样品的质量,W2:反应后装置B中残渣的质量,W3:反应生成水的质量,W4:反应生成二氧化碳的质量,为了测定其组成,至少需要其中____个数据,请将可能的组合填入下表中(每个空格中填一种组合)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学兴趣小组以工业碳酸钙(含少量Al2O3、Fe2O3、SiO2等杂质)生产二水合氯化钙晶体(CaCl2·2H2O)的操作流程为:
(1)CaCO3与盐酸反应的离子方程式 。
(2)加入氢氧化钙溶液调节溶液的pH为8.0—8.5,此时A13+、Fe3+沉淀完全,则滤渣主要成分的化学式为 ,若用氢氧化钠溶液除杂则产品中可能混有的物质为 。
(3)酸化时加盐酸将溶液的pH调节到4.0左右,其主要目的是 。
(4)操作Ⅰ中应包括①蒸发浓缩②冷却结晶③过滤④ ⑤ 等实验步骤。
(5)为测定样品中CaCl2·2H2O的含量,称取7.350 g样品配成200.0 mL溶液,与205.0 mL 0.5000 mol/LAgNO3溶液恰好完全反应。
①样品中CaCl2·2H2O的质量分数为 。
②若计算出结果有明显偏差,你认为在操作Ⅰ的五个步骤中由 引起的(填序号),理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com