
【题目】下列各组物质互为同分异构体的是
A. 红磷和白磷B. 氕和氘
C. 水和双氧水D. 正丁烷和异丁烷
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列变化中不属于化学变化的是
A. 紫色的石蕊试液中通入CO2后变色B. SO2漂白草编制品
C. 木炭使红棕色的NO2气体褪色D. 淀粉遇碘变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.0×10-16。下列说法错误的是
A. AgCl不溶于水,不能转化为AgI
B. 在含有浓度均为0.001mol·L-1的Cl-、I-的溶液中缓慢加入AgNO3稀溶液,首先析出AgI沉淀
C. AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI
D. 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于![]() ×10-11mol·L-1
×10-11mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的氮肥,合成原理为: N2(g)+3H2(g)![]() 2NH3(g) △H= —92.4 kJ/mol。在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各种物质的量变化如图,回答下列问题:
2NH3(g) △H= —92.4 kJ/mol。在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各种物质的量变化如图,回答下列问题:

(1)10 min内以NH3表示的平均反应速率:______;
(2)在10 ~20 min内:NH3浓度变化的原因可能是______________
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加NH3物质的量
(3)第1次平衡的平衡常数K1 = _________________(带数据的表达式),第2次平衡时NH3的体积分数=___________(小数点后保留一位);
(4)在反应进行至25 min时:①曲线发生变化的原因______________,② 达第二次平衡时,新平衡的平衡常数K2 ____ K1(填“大于”“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的前四周期元素,X的电子总数=周期序数=族序数,他们的单质或化合物存在如图所示的转化关系,其中甲、戊是两种最常见的金属单质,丁是非金属单质,其余为氧化物。下列说法正确的是

A. W的原子序数是Z的两倍,金属性强于Z
B. Z元素在周期表中的位置是第三周期Ⅲ族
C. 丙属于两性氧化物
D. 己的熔点高、硬度大,可用作耐火坩埚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类,

(1)如图所示的物质分类方法名称是___。
(2)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②、④、⑥、⑧、⑩后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①H2SO4 ②__ | ③NaOH ④___ | ⑤Na2SO4 ⑥___ | ⑦SO2 ⑧__ | ⑨NH3 ⑩__ |
(3)SO2和CO2都属于酸性氧化物,在化学性质上有很多相似的地方,请写出少量的⑦与③反应的化学反应方程式为:___。
(4)磷的一种化合物叫亚磷酸(H3PO3),从交叉分类的角度看,它属于二元弱酸,则Na2HPO3属于___盐(填正盐、酸式盐或碱式盐)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下关于甲烷的说法中错误的是( )
A. 甲烷化学性质比较稳定,不被任何氧化剂氧化
B. 甲烷分子具有正四面体结构
C. 甲烷分子中具有极性键
D. 甲烷分子中四个C﹣H键是完全相同的键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是研究铁钉腐蚀的装置图,下列说法不正确的是
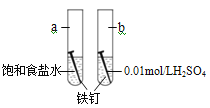
A. 铁钉在两处的腐蚀速率:a < b
B. a、b两处铁钉中碳均正极
C. a、b两处铁钉中的铁均失电子被氧化
D. a、b两处的正极反应式均为O2+4e-+4H+===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)氯原子的结构示意图_____;工业上利用电解饱和食盐水来获得氯气,其化学方程式为_____。
(2)将氯气通入石灰乳中可制取漂白粉,化学方程式为_____。漂白粉溶于水后,和空气中的二氧化碳作用,所得的溶液可用于漂白这是利用生成的 HClO,而该溶液长时间放置又会失去漂白能力,所涉及的化学反应方程式为_____。
(3)向盛有 KI 溶液的试管中加入少许 CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4 层会逐渐变浅,最后变成无色。
完成下列填空:
(a)写出并配平 CCl4层由紫色变成无色的化学反应方程式,并用“单线桥”标出电子转移的方向和数目。_____________
_____+_____+_____→_____HIO3+_____该反应中,_____元素的化合价升高。
(b)把 KI 换成 KBr,则 CCl4层变为_____色,继续滴加氯水,CCl4 层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_____。
(c)加碘盐中含碘量为 20mg~50mg/kg。制取加碘盐(含 KIO3 的食盐)1000kg,若 KI 与 Cl2 反应之 KIO3,至少需要消耗 Cl2_____mol(保留 2 位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com