
【题目】合成氨工业中,每生产2molNH3 , 放出92.4kJ热量.
(1)写出合成氨反应的热化学方程式为 .
(2)已知: 
1mol N﹣H键断裂吸收的能量等于kJ.
(3)已知关于铁的氧化物存在下列三个热化学方程式: Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣24.8kJ/mol ①
Fe2O3(s)+ ![]() CO(g)═
CO(g)═ ![]() Fe3O4(s)+
Fe3O4(s)+ ![]() CO2(g)△H=﹣15.73kJ/mol ②
CO2(g)△H=﹣15.73kJ/mol ②
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol ③
则CO还原FeO的热化学方程式为CO(g)+FeO(s)═Fe(s)+CO2(g)△H=kJ/mol.
【答案】
(1)N2(g)+3H2(g)?2NH3(g)△H=﹣92.4KJ?mol﹣1
(2)391
(3)﹣218
【解析】解:(1)每生产2molNH3,放出92.4kJ热量,所以热化学方程式为:N2(g)+3H2(g)2NH3(g)△H=﹣92.4KJmol﹣1,所以答案是:N2(g)+3H2(g)2NH3(g)△H=﹣92.4KJmol﹣1;(2)合成氨工业中:3H2+N22NH3,反应焓变=反应物断裂化学键吸收的能量﹣生成物形成化学键放出的能量=3×436+945.8﹣6×N﹣H键键能=﹣92.2,N﹣H键键能=391kJ,所以答案是:391;(3)已知:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=﹣24.8kJ/mol ①;
Fe2O3(s)+ ![]() CO(g)═
CO(g)═ ![]() Fe3O4(s)+
Fe3O4(s)+ ![]() CO2(g)△H=﹣15.73kJ/mol ②;
CO2(g)△H=﹣15.73kJ/mol ②;
Fe3O4(s)+CO(g)═3FeO(s)+CO2(g)△H=+640.4kJ/mol ③;
根据盖斯定律将方程式变形 ![]() ×①﹣
×①﹣ ![]() ×②﹣
×②﹣ ![]() ×③得:
×③得:
FeO(s)+CO(g)═Fe(s)+CO2(g),△H=[ ![]() ×(﹣24.8)﹣
×(﹣24.8)﹣ ![]() ×(﹣15.73kJ)﹣
×(﹣15.73kJ)﹣ ![]() ×640.4kJ=﹣218kJ/mol,所以答案是:﹣218.
×640.4kJ=﹣218kJ/mol,所以答案是:﹣218.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热.


科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.将SO2气体通入NaClO溶液中:SO2+2ClO﹣+H2O═SO32﹣+2HClO
B.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣
C.向Na2S2O3溶液中通入足量氯气:S2O32﹣+2Cl2+3H2O═2SO32﹣+4Cl﹣+6H+
D.电解饱和MgCl2溶液:2Cl﹣+2H2O ![]() 2OH﹣+H2↑+Cl2↑
2OH﹣+H2↑+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X2(g)+Y2(g)2Z(g),已知X2、Y2、Z起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度可能是( )
A.c(Z)=0.4 mol/L
B.c(X2)=0.2mol/L
C.c(Y2)=0.4mol/L
D.c(X2)+c(Y2)+c(Z)=0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大,m、n、p、q依次为四种元素的单质;r、t、u 为二元化合物,其中u 是我国北方主要的大气污染物之一,可使品红溶液褪色;25℃,0.01mo/L的v溶液pH=12;上述物质间转化关系如图,下列说法错误的是
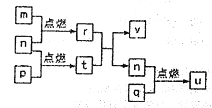
A. Y、Z、W的简单离子半径:W>Y>Z
B. W、Y 分别与X形成的简单化合物的沸点: Y>W
C. X和Y、Z和Y都能形成不止一种二元化合物
D. X、Y、Z、W 中任意三种元素形成的化合物都抑制水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳和乙二醇在氧化锌或锌盐催化下可合成碳酸乙烯酯。
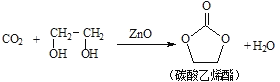
回答下列问题:
(1)锌基态离子的价电子排布图为_______________;在基态18O原子中,核外电子存在_________种空间运动状态。
(2)乙二醇中C、H、O的电负性大小关系是__________ ;碳酸乙烯酯中碳原子的杂化轨道类型有___________;1mol 碳酸乙烯酯中含有的σ键的数目为__________NA。
(3)锌盐水溶液中Zn2+可与H2O之间形成[Zn(H2O)6]2+,配体中的配位原子是_________(填微粒符号),[Zn(H2O)6]2+中所含化学键的类型为__________________________。
(4)阴离子X-与CO2互为等电子体且X-内含共价键和氢键,则X-的化学式为______________。
(5)一种锌金合金晶体的立方体晶胞中,金原子位于顶点,锌原子位于面心,则该合金中金原子与锌原子的个数之比为_________;若该晶体的晶胞棱长为apm(1pm=10-12m),则该合金的密度为_______g·cm-3(用NA表示阿伏加德罗常数的值,列出算式不要求结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生以铁丝和Cl2为原料进行下列三个实验.从分类角度分析,下列选项正确的是( ) 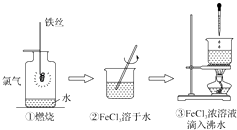
A.实验①、②所涉及的物质均为电解质
B.实验②、③均为放热反应实验
C.②、③均未发生氧化还原反应
D.实验①、③反应制得的物质均为纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于细胞结构和生物体内化合物的叙述正确的是
A.细菌代谢速率极快,其细胞器膜为酶提供了附着位置
B.人体细胞内有细胞核、线粒体和叶绿体
C.植物体内的无机盐大多数以离子形式存在
D.脂质中的磷脂参与构成核糖体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com