
����Ŀ�����գ�����Ȼ��ͨѶ���������ҹ�������ѧκ����Ŷӿ�����һ�ֹ����������������μ�������ֱ���ڶ������������������������������Ĥ��
��1������Nԭ�ӵĵ����Ų�ͼ��ʾ��״̬�У�������ߵ���___��������͵���___(����ĸ��ʾ)��
A.![]() B.
B.![]()
C.![]() D.
D.![]()
��2���ڶ���������Ԫ���У�����һ�����ܴ�С����һ��������B��N֮���Ԫ����___�֡�
��3��Na��N�γɵ�NaN3���������������İ�ȫ���ң����������ӵĿռ乹��Ϊ___��Na�ڿ�����ȼ������ɫ���棬���ֻ�ɫ��ɫ�ù�������ȡ�Ĺ���Ϊ___����(��������������������)��
��4����֪NH3���ӵļ���ԼΪ107������ͬ�������⻯��PH3���ӵļ���ԼΪ94�������ü۲���ӶԻ������۽���NH3�ļ��DZ�PH3�ļ��Ǵ��ԭ��___��
��5��BH3��NH3��һ����Ч����ȫ�Ĺ��崢����ϣ�����BH3��NH3��Ӧ���ɣ�B��N֮���γ���λ������ԭ���ṩ___����BH3��NH3��Bԭ�ӵ��ӻ���ʽΪ___����������������������ͬ���ڱ�״����Ϊ��ɫ��ζ�İ�ɫ���壬��ˮ���ܽ��Ҳ�ϴ���ԭ����___��
��6����������������ԭ�Ӿ��壬�侧���ṹ��ͼ1��ʾ������Ϊ��ԭ�Ӵ�����ԭ��Χ�ɵ�ij�ֿ�϶�У���ԭ�Ӵ�����ԭ��Χ�ɵ�___(��ռ�ṹ)��϶�С�ͼ2��������������z���ͶӰͼ������ͼ��Բ����Ϳ��������N�����λ��___��
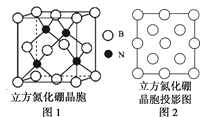
��֪������������ܶ�Ϊdg��cm-3�������ӵ�������ֵΪNA��������ԭ���뵪ԭ�ӵ��������Ϊ___nm��(ֻҪ������ʽ)
���𰸡�D A 3 ֱ���� ���� N��ԭ�Ӱ뾶PС���縺�Ա�P��ʹ��NH3�����й¶Ե���֮��ľ����PH3�����н��������� �µ��Ӷ� sp3 BH3��NH3���Ӽ���������Ҳ����ˮ�����γ��������������Ӳ��� �������� 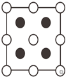
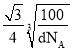 ��107
��107
��������
�ڵ����Ų�ͼ�У������������ԭ���Ų�����������ͣ����ܼ�Խ�ߵĹ���е�����Խ�࣬������Խ�����ж�������ͬ����Ԫ�ص�һ�����ܵı仯���ɼ�IIA��VA��������𣻸��ݼ۲���Ӷ����жϿռ乹�ͣ����ݼ۲���ӶԻ��������жϼ��Ǵ�Сԭ���ݼ����γ�ʵ�ʼ��γ��������𣻸��ݾ���ṹ���ܶȼ��㾧�����ⳤ�����ⳤ�ټ�����ԭ�ӵľ��롣
��1��Nԭ�ӵ����Ų�ͼ��ʾ��״̬�У������������ԭ��������������ͣ�����Խ�ߵĹ���е��Ӹ���Խ�࣬������Խ�ߣ�����ͼ֪��A�����������ԭ����D�������ϸߵĹ���е�������࣬����������ߣ���ΪD��A��
��2��ͬ��������Ԫ����ԭ�����������һ�����ܳ��������ƣ�IIA�塢VA��Ϊȫ�����������ȶ�״̬����һ�����ܸ���ͬ��������Ԫ�أ������B��N֮�仹��Be��C��O����Ԫ�أ���Ϊ3��
��3��N3 -��������Nԭ�Ӽ۲���Ӷ���=2+ ![]() =2���۲���Ӷ���Ϊ2���µ��Ӷ�Ϊ0��Nԭ���ӻ���ʽΪsp�ӻ������ӿռ乹��Ϊֱ���Σ����ӴӼ���̬ԾǨ�����ܼ����Թ����ʽ�ͷ�������NaԪ�ط�����ɫ��Ӧ����Ϊ������ԭ�ӣ�������ף���Ϊֱ���Σ����䡣
=2���۲���Ӷ���Ϊ2���µ��Ӷ�Ϊ0��Nԭ���ӻ���ʽΪsp�ӻ������ӿռ乹��Ϊֱ���Σ����ӴӼ���̬ԾǨ�����ܼ����Թ����ʽ�ͷ�������NaԪ�ط�����ɫ��Ӧ����Ϊ������ԭ�ӣ�������ף���Ϊֱ���Σ����䡣
��4��NH3��PH3������ԭ�Ӿ�Ϊsp3�ӻ���N�ĵ縺�Ա�P��Nԭ�Ӱ뾶��Pԭ�Ӱ뾶С��Nԭ�ӶԼ��ϵ���������ǿ�����NH3�����гɼ����ӶԼ�ľ���Ͻ����ɼ����Ӷ�֮��ij�������ʹNH3�ļ��DZ�PH3�ļ��Ǵ�ΪN�ĵ縺�Ա�P��Nԭ�Ӱ뾶��Pԭ�Ӱ뾶С��NH3�����гɼ����ӶԼ�ľ���Ͻ����ɼ����Ӷ�֮��ij�������
��5��Bԭ���γ�3��B-H����Bԭ���пչ������������Nԭ����1�Թµ��Ӷԣ�B��N֮���γ���λ������ԭ���ṩ�µ��Ӷԣ���BH3��NH3��Bԭ���γ�3��B-H����B���γ�1����λ����Bԭ���ӻ������ĿΪ4��Bԭ���ӻ���ʽΪ��sp3�ӻ�����ˮ���ܽ�Ƚϴ�����ΪBH3NH3�������ڼ��Է��ӣ��������ܣ���BH3��NH3���Ӽ�����������ˮ����֮�����γ������������������ˮ�������鲻�ܣ���Ϊ�µ��Ӷԣ�sp3�ӻ���BH3NH3�������ڼ��Է��ӣ��������ܣ���BH3��NH3���Ӽ�����������ˮ����֮�����γ������������������ˮ�������鲻�ܡ�
��6����������������ԭ�Ӿ��壬�侧���ṹ��ͼ1��ʾ��������ÿ��Nԭ������4��Bԭ�ӣ���4��Bԭ�ӹ�����Nԭ��Ϊ���ĵ���������ṹ��ͼ2��������������z���ͶӰͼ����ͼ��Բ����Ϳ��������N�����λ��Ϊ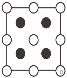 ����֪������������ܶ�Ϊdg��cm-3�������ӵ�������ֵΪNA��������Nԭ����Ϊ4 ��Bԭ��8�������һ����6�����ĸ�һ������Bԭ����=8��
����֪������������ܶ�Ϊdg��cm-3�������ӵ�������ֵΪNA��������Nԭ����Ϊ4 ��Bԭ��8�������һ����6�����ĸ�һ������Bԭ����=8��![]() +6��
+6��![]() =4������������m=
=4������������m= ![]() g=
g= ![]() g���������V=(a��10-7cm)3���������ܶ�Ϊdg��cm-3����
g���������V=(a��10-7cm)3���������ܶ�Ϊdg��cm-3����![]() �ó�
�ó�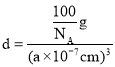 ���������ⳤa=
���������ⳤa=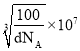 nm�����������������е�ԭ������Χ��4����ԭ���γ�������ṹ������Nԭ��������������Bԭ�����ߴ��ھ�����Խ����ϣ��Ҷ��߾�����ھ�����Խ��߳��ȵ�
nm�����������������е�ԭ������Χ��4����ԭ���γ�������ṹ������Nԭ��������������Bԭ�����ߴ��ھ�����Խ����ϣ��Ҷ��߾�����ھ�����Խ��߳��ȵ�![]() ��������Խ��߳��ȵ��ھ����ⳤ��
��������Խ��߳��ȵ��ھ����ⳤ��![]() ������ԭ���뵪ԭ������ľ���Ϊx nm����x=
������ԭ���뵪ԭ������ľ���Ϊx nm����x= ![]() anm����a���룬x=
anm����a���룬x=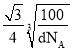 ��107nm����Ϊ�������壬
��107nm����Ϊ�������壬 ��
��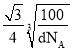 ��107��
��107��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Cu(s)��2H��(aq)===Cu2��(aq)��H2(g) ��H1
2H2O2(l)===2H2O(l)��O2(g) ��H2
2H2(g)��O2(g)===2H2O(l) ��H3
��ӦCu(s)��H2O2(l)��2H��(aq)===Cu2��(aq)��2H2O(l)����H��
A. ��H����H1��1/2��H2��1/2��H3 B. ��H����H1��1/2��H2��1/2��H3
C. ��H����H1��2��H2��2��H3 D. ��H��2��H1����H2����H3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��p=p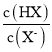 =-lg
=-lg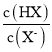 �������£���0.10mo1��L-1��HX��Һ�еμ�0.1mol��L-1��NaOH��Һ����ҺpH��p�ı仯��ϵ��ͼ������˵����ȷ���ǣ� ��
�������£���0.10mo1��L-1��HX��Һ�еμ�0.1mol��L-1��NaOH��Һ����ҺpH��p�ı仯��ϵ��ͼ������˵����ȷ���ǣ� ��

A.a����Һ�У�c(HX)+c(X-)=0.10mo1��L-1
B.c����Һ�У�c(Na+)��10c(HX)
C.b������Ϊ(0��4.50)
D.��Һ��ˮ�ĵ���̶ȣ�c��b��a
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W��RΪ���ֶ�����Ԫ�أ���ԭ�Ӱ뾶������������֮��Ĺ�ϵ����ͼ��ʾ������˵���������
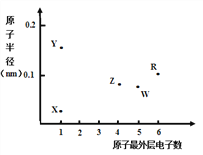
A. �����Ӱ뾶��Y < W
B. ����������Ӧˮ��������ԣ�Z < W
C. RΪ��Ԫ��
D. X��Z�����γ���������ṹ�ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������ɽ��������������Ҳ���Ҹ�����ӵ�����������̡�ˮ�������ü�����ÿ���й��˵����롣�ش��������⣺
��1���ŷŵ������еĵ�������������___��Ⱦ��
��2�����ʡ����͡�ϡ���������ȹ�ҵ�����ŷų���Ũ�ȵİ�����ˮ��������ˮ����ɺ�����������Ӫ��������Ҫ���ء�
��ij���ʳ������İ�����ˮ�еĵ�Ԫ�ض���NH4+��NH3��H2O��ʽ���ڣ�Ϊ�ﵽ���Ϊ���������õ�Ŀ�ġ��ɲ�ȡ�ķ�����___��
��ij�Ŷ���ƴ����������£�
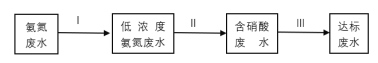
���̢�Ϊ�������̣��������������ʵ��NH4+��NO2-��NO3-��ת�����ڼ���������NH4+������������NO3-���ܷ�Ӧ���ӷ���ʽΪ___��
���̢�Ϊ���������̣���һ�������µķ�ˮ�м���״���CH3OH��ʵ��HNO3��NO2-��N2��ת������lmol NO2-��ȫת��ΪN2��ת�Ƶĵ�����Ϊ___��
��3������������úȼ�ղ����ķ���SO2�Ȼ�Դ��������Ⱦ��
��Ϊ��ֹ��ҵúȼ�ղ���SO2������ȼú�м���CaCO3��״�������������IJ�����������ʯ�ࡣ����Ӧ�Ļ�ѧ����ʽΪ____��
��ij��ȤС���ȡ�õ�������Ʒ����pH�ⶨ�����ŵļ�����ƣ��õ��������ݣ�pHԽС������Խǿ����
ʱ��/h | ��ʼ | 8 | 16 | 24 | 32 | 40 | 48 |
pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
��ˮpH�仯����Ҫԭ����___���û�ѧ����ʽ��ʾ����
��ij���ữ������ʹ��һ�ֺ�����Ϊ25%�Ļ�����ʯ��FeS2��Ϊԭ�ϡ���ȡ2�ָÿ�ʯ�����Ƶ�98%��Ũ����___�֣���������������96%SO2ת��ΪSO3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ����
A. ��0.1mol/LCH3COOH��Һ�м�������ˮ����Һ��c(H+)/c(CH3COOH)��С
B. ��CH3COONa��Һ��20��������30�棬��Һ��c(CH3COO-)/c(CH3COOH)��c(OH��)����
C. �������м��백ˮ�����ԣ���Һ��c(NH4+)/c(Cl��)��1
D. ��AgCl��AgBr�ı�����Һ�м�����������������Һ��c(Cl��)/c(Br��)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ϡHCl��Һ�μӵ���Ũ�ȵ�����AOH��Һ�У���û��Һ��pH��![]() �Ĺ�ϵ��ͼ��ʾ������a���ʾδ������ʱ�����ݣ�e���ʾHCl��AOHǡ����ȫ��Ӧʱ�����ݡ�����˵���������( )
�Ĺ�ϵ��ͼ��ʾ������a���ʾδ������ʱ�����ݣ�e���ʾHCl��AOHǡ����ȫ��Ӧʱ�����ݡ�����˵���������( )
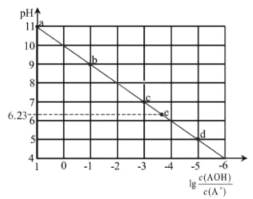
A.�����£�A+��ˮ��ƽ�ⳣ��Ϊ1.0��10-10
B.��d��Һ�У�c(Cl-)> c(AOH)>c(A+)
C.��c ��Һ�е�n(A+)+n(AOH)���ڵ�e��Һ�е�n(Cl-)
D.��e��Һ��ˮ�������H+Ũ��Ϊ10-6.23 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� NA Ϊ�����ӵ�������ֵ������˵������ȷ����
A.1mol CH4 �� Cl2 �ڹ����·�Ӧ���ɵ�CH3Cl����������NA
B.100 g CaCO3 �� KHCO3 �Ĺ��������к��е���������Ϊ NA
C.һ��Ũ�ȵ������þ��Ӧ������ 11.2L(��״��)���壬ת�Ƶ�����Ϊ NA
D.6.4g SO2 ����ˮ�γɵ������У�SO2��H2SO3��HSO![]() �� SO
�� SO![]() ������֮��Ϊ 0.1NA
������֮��Ϊ 0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ��þ�������ͼ��ʾ���缫����Ϊ����þ�����������Ļ���̿�����ҺΪKOHŨ��Һ������˵��������ǣ� ��
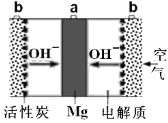
A.����ܷ�ӦʽΪ��2Mg��O2��2H2O��2Mg(OH)2
B.������ӦʽΪ��O2+4e��+4OH��=2H2O
C.����̿���Լӿ�O2�������ϵķ�Ӧ����
D.���ӵ��ƶ�������a�����·��b
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com