
| A. | 胶体化学可用于制备纳米材料 | |
| B. | 钛合金主要用于尖端领域 | |
| C. | 压电陶瓷可实现化学能与电能的转化 | |
| D. | 稀土元素大大改善合金性能被称为冶金工业的维生素 |
分析 A.胶体分散质粒度介于1-100nm之间;
B.依据钛及其合金性质稳定,耐腐蚀解答;
C.压电陶瓷可实现机械能与电能的转化
D.在合金中加入适量稀土金属,就能大大改善合金的性能.
解答 解:A.胶体分散质粒度介于1-100nm之间,可以用于制造纳米材料,故A正确;
B.钛及其合金性质稳定,耐腐蚀,常用于飞机、火箭、导弹、人造卫星等,故B正确;
C.压电陶瓷可实现机械能与电能的转化,故C错误;
D.在合金中加入适量稀土金属,就能大大改善合金的性能,所以稀土元素被称为冶金工业的维生素,故D正确;
故选:C.
点评 本题考查了材料的用途,明确材料的成分及性质是解题关键,注意胶体本质特征,注意对相关知识的积累.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
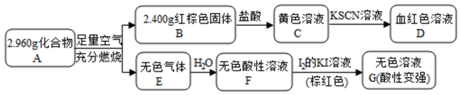
 . 该反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑.
. 该反应的离子方程式为Fe3S4+6H+=3Fe2++S+3H2S↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知:25℃时Ksp(BaSO4)=1.0×10-10.该温度下,CaSO4悬浊液中,c(Ca2+)与c(SO42-)的关系如图所示,下列叙述正确的是( )
已知:25℃时Ksp(BaSO4)=1.0×10-10.该温度下,CaSO4悬浊液中,c(Ca2+)与c(SO42-)的关系如图所示,下列叙述正确的是( )| A. | 向a点的溶液中加入等物质的量固体Na2SO4或Ca(NO3)2,析出的沉淀量不同 | |
| B. | a、b、c、d四点对应的体系中,d点体系最稳定 | |
| C. | 升高温度后,溶液可能会由a点转化为b点 | |
| D. | 反应Ba2+(aq)+CaSO4(s)?BaSO4(s)+Ca2+(aq)的平衡常数K=9×104 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量铁在1molCl2中燃烧时转移电子数为2NA | |
| B. | 2L0.1mol•L-1氯化钾溶液中阴离子所带电荷数为NA | |
| C. | 1L0.1mol•L-1的Na2CO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| D. | 标准状况下,体积各为2.24L的HCl和NH3混合气体中含有的共价键数为0.25NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
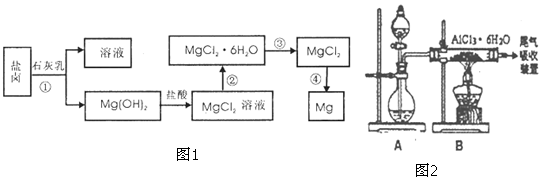
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的单质在自然界只有一种核素 | |
| B. | 元素C、D、E的简单离子的半径依次减小 | |
| C. | A、E分别与C形成的化合物中含有一种相同类型的化学键 | |
| D. | 这几种元素可能形成的简单离子中E的简单离子的还原性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
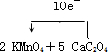
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com