
ЁОЬтФПЁПИЪАБЫсбЧЬњ[(NH2CH2COO)2Fe]ЪЧвЛжжВЙЬњЧПЛЏМСЃЌЙуЗКгУгкШБЬњадЦЖбЊЕФдЄЗРКЭжЮСЦЁЃФГбЇЯАаЁзщдкЪЕбщЪвРћгУжБНгКЯГЩЗЈжЦИїИЪАБЫсбЧЬњЁЃгаЙиЮяжЪаджЪШчЯТЫљЪОЃК
ИЪАБЫс( NH2CH2COOH) | ФћУЪЫс | ИЪАБЫсбЧЬњ |
взШмгкЫЎЃЌЮЂШмгкввДМЁЂ | взШмгкЫЎКЭввДМЃЌ | взШмгкЫЎЃЌ |
СНадЛЏКЯЮя | гаЧПЫсадКЭЛЙдад | ФбШмгкввДМ |
ЪЕбщЙ§ГЬМАзАжУЭМШчЯТЃЈМаГжКЭМгШШвЧЦївбЪЁТдЃЉЃК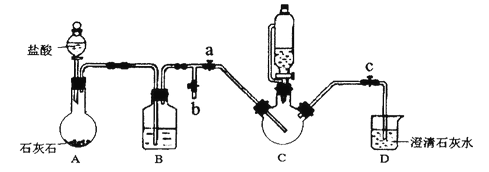
IЃЎКЯГЩЃКдкCжаМгШы0.10molИЪАБЫсЁЂ0.05molСђЫсбЧЬњЁЂЩйСПФћУЪЫсКЭ200mLЫЎЃЌРћгУCO2НЋCзАжУжаЕФПеЦјХХОЛЃЌШЛКѓдк40ЁцКуЮТЬѕМўЯТгУДХСІНСАшЦїВЛЖЯНСАшЃЌВЂгУКубЙЕЮвКТЉЖЗЯђCжаЕЮМг6molЁЄL-1NaOHШмвКЕїНкpHЕН6зѓгвЃЌЪЙЗДгІЮяГфЗжЗДгІЁЃ
IIЃЎЗжРыЃКМгШыЮоЫЎввДМЃЌСЂМДГіЯжАзЩЋГСЕэЁЃНЋГСЕэНјааЙ§ТЫЁЂЯДЕгЃЌЪеМЏТЫдќЁЃ
ЂѓЃЎЬсДПЃКНЋТЫдќШмНтгкЪЪСПЕФеєСѓЫЎжаЃЌШЛКѓНсОЇЁЂЙ§ТЫЃЌНЋДПЛЏКѓЕФВњЦЗЗХШыецПеИЩдяЯфжаИЩдяКѓГЦжиЁЃ
ЛиД№ЯТСаЮЪЬтЃК
(1)BзАжУЕФзїгУЪЧ______________ЃЛ
(2)ФмжЄУїCзАжУжаПеЦјХХОЛЕФЯжЯѓЪЧ______________ЃЛЯђCжаЕЮМгNaOHШмвКжЎЧАгІИУЭЃжЙЕЮМгбЮЫсЃЌЧвЙиБежЙЫЎМа____________ЃЌДђПЊжЙЫЎМа________
(3)ЁАКЯГЩЁБжаМгШыФћУЪЫсЕФзїгУЪЧ______________ЃКЧыаДГіКЯГЩИЪАБЫсбЧЬњЕФЛЏбЇЗНГЬЪН_________ЁЃ
(4)МгШыввДМЕФФПЕФЪЧ________ЃЛЁАЬсДПЁБЪБгУЕФНсОЇЗНЗЈЮЊ________________
(5)ЭЈЙ§ВтСПЕУжЊЃКЕШХЈЖШ(NH2CH2COO)2Fe ШмвКЕМЕчФмСІдЖаЁгкFeSO4ШмвКЁЃБЉТЖдкПеЦјжаЃЌ(NH2CH2COO)2FeШмвКБШFeSO4ШмвКФбБЛбѕЛЏЃЌЧыЗжЮідвђЮЊ________
(6)ШєВњЦЗжЪСПЮЊagЃЌдђВњТЪЮЊ________ %ЁЃ
ЁОД№АИЁП Г§ШЅCO2жаЕФHClЦјЬх DжаШмвКГіЯжЛызЧ a b ФћУЪЫсОпгаЛЙдадЃЌПЩвдЗРжЙFe2+БЛбѕЛЏ 2NH2CH2COOH + FeSO4 + 2NaOH =(NH2CH2COO)2Fe + Na2SO4 + 2H2O МѕЩйИЪАБЫсбЧЬњЕФШмНтСПЃЌДйЪЙЦфНсОЇЮіГіЁЃ еєЗЂХЈЫѕЁЂРфШДНсОЇ(ЛђРфШДНсОЇ) гЩВтСПНсЙћжЊИЪАБЫсбЧЬњЪЧШѕЕчНтжЪЃЌдкШмвКжаЕчРыВњЩњЕФFe2+ХЈЖШаЁЃЌЙЪВЛвзБЛбѕЛЏ ![]() ЃЈЛђ9.8aЃЉ
ЃЈЛђ9.8aЃЉ
ЁОНтЮіЁП(1)гУбЮЫсгыЪЏЛвЪЏЗДгІжЦБИЕФCO2жаЛьгаHClЦјЬхЃЌашвЊГ§ШЅHClЃЌЗРжЙЦфИЩШХЪЕбщНсЙћЁЃ(2)ЕБCO2ХХОЛCзАжУжаПеЦјНјШыDзАжУКѓЃЌЛсгыГЮЧхЕФЪЏЛвЫЎЗДгІГіЯжЛызЧЯжЯѓЃЌЫљвдЕБDжаГіЯжЛызЧМДЫЕУїCжаПеЦјвбБЛХХОЛЁЃдкНјааCзАжУжаЕФКЫаФЗДгІЧАЃЌгІЭЃжЙЭЈШыCO2ЦјЬхЃЌЫљвдашвЊЭЃжЙЕЮМгбЮЫсЃЌВЂЙиБежЙЫЎМаaЃЌДђПЊжЙЫЎМаbЁЃвђЮЊCзАжУашвЊдкМгШШЬѕМўЯТНјааЗДгІЃЌЙЪВЛФмЙиБежЙЫЎМаcЃЌЗРжЙбЙЧПЙ§ДѓГіЯжЪТЙЪЁЃ(3)дкжЦБИИЪАБЫсбЧЬњЙ§ГЬжаЪМжевЊЗРжЙFeSO4БЛбѕЛЏЃЌЫфШЛвбгУCO2ХХГ§СЫзАжУжаЕФПеЦјЃЌЕЋгЩЬтФПжаЕФвбжЊаХЯЂПЩжЊЃЌФћУЪЫсОпгаЛЙдадЃЌПЩШЗБЃFeSO4ВЛБЛбѕЛЏЁЃКЯГЩИЪАБЫсбЧЬњЕФЛЏбЇЗНГЬЪН2NH2CH2COOH + FeSO4 + 2NaOH =(NH2CH2COO)2Fe + Na2SO4 + 2H2OЃЛ(4)гЩЬтФПвбжЊаХЯЂПЩжЊЃЌИЪАБЫсбЧЬњФбШмгкввДМЃЌЫљвдМгШыввДМЕФФПЕФЪЧМѕЩйИЪАБЫсбЧЬњЕФШмНтСПЃЌДйЪЙЦфИќЖрЕФНсОЇЮіГіЁЃЁАЬсДПЁБИЪАБЫсбЧЬњЪБгУЕФНсОЇЗНЗЈЮЊеєЗЂХЈЫѕЁЂРфШДНсОЇ (ЛђРфШДНсОЇ)ЁЃ(5)ИљОнЕШХЈЖШ(NH2CH2COO)2FeШмвКЕМЕчФмСІдЖаЁгкFeSO4ШмвКПЩжЊИЪАБЫсбЧЬњЪЧШѕЕчНтжЪЃЌдкШмвКжаЫќЕчРыВњЩњЕФFe2+ХЈЖШаЁЃЌЙЪВЛвзБЛбѕЛЏЁЃ(6)0.1molЕФИЪАБЫсКЭ0.05molЕФСђЫсбЧЬњРэТлЩЯЩњГЩ0.05molЕФИЪАБЫсбЧЬњЃЌРэТлЩЯПЩВњЩњИЪАБЫсбЧЬњЃК204gmol-1ЁС0.05mol =10.2gЃЌШєВњЦЗжЪСПЮЊagЃЌдђВњТЪЮЊ![]()
![]() ЁЃ
ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкЛЏбЇМќЕФЫЕЗЈе§ШЗЕФЃЈ ЃЉ
A.жЛДцдкгкЗжзгжЎМф
B.ЯрСкдзгМфЧПСвЕФЯрЛЅзїгУ
C.жЛДцдкгкРызгжЎМфЁЂ
D.ЯрСкЗжзгМфЕФЯрЛЅзїгУ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПХЈЖШЮЊ2.00 mol/LЕФбЮЫсШмвК1LЃЌгћЪЙЦфХЈЖШБфЮЊ4.00mol/LЃЌЯТСаЗНЗЈПЩааЕФЪЧЃЈ ЃЉ
A. еєЗЂЕє0.5LЫЎ B. БъПіЯТЭЈШы44.8L HClЦјЬх
C. НЋШмвКМгШШеєЗЂХЈЫѕжС0.5L D. МгШы10mol/LбЮЫс0.6LЃЌдйНЋШмвКЯЁЪЭжС2L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГДЮЪЕбщашгУ480mLЁЂ0.5mol/L ЕФЯЁСђЫсЃЌФГЭЌбЇгУ98%ЕФХЈСђЫсЃЈІб=1.84g/cm3ЃЉ НјааХфжЦЃЌЧыЛиД№ЯТСаЮЪЬт:
ЃЈ1ЃЉ ЪЕбщашвЊЕФВЃСЇвЧЦїГ§СЫЩеБЃЌНКЭЗЕЮЙмЁЂСПМђЁЂВЃСЇАєЃЌЛЙашвЊ__________ЃЛ
ЃЈ2ЃЉМЦЫу: ашгУСПЭВСПШЁХЈСђЫсЕФЬхЛ§ЮЊ__________ mLЃЛ
ЃЈ3ЃЉ ХфжЦЙ§ГЬЃК
ЂйгУСПЭВСПШЁЫљашЕФХЈСђЫс
ЂкНЋХЈСђЫсЛКЛКзЂШыЪЂгаЪЪСПеєСѓЫЎЕФЩеБжаЃЌБпМгБпНСАшЃЌРфШДжСЪвЮТ
ЂлгУВЃСЇАєв§СїНЋЩеБжаЕФШмвКзЊвЦЕНвбОМьТЉЕФКЯЪЪЙцИёЕФШнСПЦПжа
ЂмЯДЕгЩеБКЭВЃСЇАє2~3 ДЮЃЌЯДЕгвКвВзЂШыШнСПЦПжаЃЌЧсЧсвЁЖЏШнСПЦПЃЌЪЙШмвКЛьКЯОљдШ
ЂнЯђШнСПСїжаМгШыеєСѓЫЎЃЌдкОрРыПЬЖШ1ЁЋ2cm ЪБЃЌШЛКѓЖЈШн
ЂоИЧКУЦПШћЃЌЗДИДЩЯЯТЕпЕЙЃЌвЁдШЃЛ
ЂпНЋХфжЦКУЕФШмвКзЊвЦжСЪдМСЦПжаД§гУЁЃ
ЩЯЪіВНжшжавЛЖЈгУЕННКЭЗЕЮЙмЕФга__________ЃЈЬюађКХЃЉ;
ШєВНжшЂнЖЈШнЪБМгЫЎГЌЙ§ПЬЖШЯпЃЌгІИУШчКЮДІжУ:___________ЁЃ
ЃЈ4ЃЉ дкКсЯпЩЯЬюаДЯТСаИїжжЧщПіЖдЫљХфжЦШмвКХЈЖШЕФгАЯьЃЈбЁЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЛђЁАЮогАЯьЁБЃЉ.
ЂйЫљгУЕФХЈСђЫсГЄЪБМфЗХжУдкУмЗтВЛКУЕФШнЦїжа______ЃЛ
ЂкгУСПМђСПШЁХЈСђЫсЪБбіЪгвКУц______ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТЃЌгУ0.10 molЁЄL-1HClШмвКЕЮЖЈ20 mL 0.050 molЁЄL-1Na2CO3КЭ0.025 molЁЄL-1NaHCO3ЛьКЯШмвКЃЌЕУГіШчЭМЫљЪОЕФЕЮЖЈЧњЯпЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
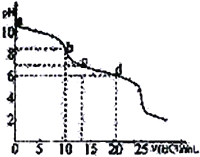
A. aЕуШмвКЯдМюадЕФжївЊдвђЃКCO32-+H2O![]() HCO3-+CH-
HCO3-+CH-
B. bЕуШмвКжаЃКc(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. cЕуШмвКжаЃКc(Na+)=c(HCO3-)+2c(CO32-)+ c(Cl-)
D. dЕуШмвКжаЃКc(Na+)> c(Cl-)> c(HCO3-)>c(H+)>c(OH-)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊ4NH3ЃЋ5O2 ![]() 4NOЃЋ6H2O(g)ЃЌШєЗДгІЫйТЪЗжБ№гУv(NH3)ЁЂv(O2)ЁЂv(NO)ЁЂv(H2O)[molЁЄLЃ1ЁЄminЃ1]БэЪОЃЌдђе§ШЗЕФЙиЯЕЪЧ( )
4NOЃЋ6H2O(g)ЃЌШєЗДгІЫйТЪЗжБ№гУv(NH3)ЁЂv(O2)ЁЂv(NO)ЁЂv(H2O)[molЁЄLЃ1ЁЄminЃ1]БэЪОЃЌдђе§ШЗЕФЙиЯЕЪЧ( )
AЃЎ![]() v(NH3)ЃНv(O2) BЃЎ
v(NH3)ЃНv(O2) BЃЎ![]() v(O2)ЃНv(H2O)
v(O2)ЃНv(H2O)
CЃЎ![]() v(NH3)ЃНv(H2O) DЃЎ
v(NH3)ЃНv(H2O) DЃЎ![]() v(O2)ЃНv(NO)
v(O2)ЃНv(NO)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПИљОнЫљбЇЮяжЪЗжРржЊЪЖЃЌЛиД№ЯТСаЮЪЬтЁЃгаЯТСа10жжЮяжЪ
ЂйCH3CH2CH3ЁЁЂкCH2==CH2ЁЁЂл![]() Ђм
Ђм ![]() ЂнCH3CH2CH2OHЁЁЂоCH3CHO ЂпCuSO4ЁЄ5H2OЁЁЂрFeЁЁЂсCH3COOH ЂтCH3COONa
ЂнCH3CH2CH2OHЁЁЂоCH3CHO ЂпCuSO4ЁЄ5H2OЁЁЂрFeЁЁЂсCH3COOH ЂтCH3COONa
(1)ЪєгкЮоЛњЛЏКЯЮяЕФЪЧ _______ЁЃ
(2)ЪєгкЬўЕФЪЧ_______ЁЃ
(3)ЪєгкЭщЬўЕФЪЧ______ЃЌЪєгкЫсЕФЪЧ______ЁЃ
(4)ЪєгкгаЛњЛЏКЯЮяЕФЪЧ_______ ЁЃЪєгкЬўЕФбмЩњЮяЕФЪЧ_______ ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЗДгІЃКN2(g)+O2(g)![]() 2NO(g),ЁїH=+180.50 kJЁЄmol-1ЃЛЁїS=247.7 JЁЄmol-1ЁЄK-1ЁЃШєИУЗДгІдквЛУмБеШнЦїжаНјааЃЌШєВЛПМТЧЮТЖШЖдИУЗДгІьЪБфЕФгАЯьЃЌдђЯТСаЫЕЗЈжае§ШЗЕФЪЧЃЈ ЃЉ
2NO(g),ЁїH=+180.50 kJЁЄmol-1ЃЛЁїS=247.7 JЁЄmol-1ЁЄK-1ЁЃШєИУЗДгІдквЛУмБеШнЦїжаНјааЃЌШєВЛПМТЧЮТЖШЖдИУЗДгІьЪБфЕФгАЯьЃЌдђЯТСаЫЕЗЈжае§ШЗЕФЪЧЃЈ ЃЉ
A. ФмЪЙИУЗДгІЮяжаЛюЛЏЗжзгЪ§КЭЛюЛЏЗжзгАйЗжЪ§ЭЌЪБдіДѓЕФЗНЗЈжЛФмЪЧЪЙгУДпЛЏМС
B. ЕНДяЦНКтзДЬЌЪБЃЌv(N2)=2v(NO)
C. дк1000ЁцЪБЃЌДЫЗДгІФмздЗЂНјаа
D. вЛЖЈЮТЖШЯТЃЌИУЗДгІДяЕНЦНКтзДЬЌКѓЃЌдіМгN2ЕФХЈЖШЃЌЛЏбЇЗДгІЦНКтГЃЪ§БфДѓ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЩшCЃЋCO2==2COЃQ1ЃЌЗДгІЫйТЪЮЊv1ЃЛN2ЃЋ3H2==2NH3ЃЋQ2ЃЌЗДгІЫйТЪЮЊv2ЃЌЖдгкЩЯЪіЗДгІЃЌЕБЮТЖШЩ§ИпЪБЃЌv1КЭv2ЕФБфЛЏЧщПіЮЊ
A.ЭЌЪБМѕаЁB.ЭЌЪБдіДѓC.v1діДѓЃЌv2МѕаЁD.v1МѕаЁЃЌv2діДѓ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com