
【题目】已知4NH3+5O2 ![]() 4NO+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[mol·L-1·min-1]表示,则正确的关系是( )
4NO+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)[mol·L-1·min-1]表示,则正确的关系是( )
A.![]() v(NH3)=v(O2) B.
v(NH3)=v(O2) B.![]() v(O2)=v(H2O)
v(O2)=v(H2O)
C.![]() v(NH3)=v(H2O) D.
v(NH3)=v(H2O) D.![]() v(O2)=v(NO)
v(O2)=v(NO)
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.核外电子排布完全相同的两种粒子,其化学性质一定相同
B.难失电子的原子,一定具有强氧化性
C.离子化合物和共价化合物中都可能含有非极性键
D.共价化合物溶水电离过程中,共价键未被破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下HF的电离常数Ka=3.3×10-4 ,CaF2的溶度积常数Ksp=1.46×10-10。在该温度下取浓度为0.31 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合。下列说法正确的是
A. 该温度下,0.31 mol·L-1的HF溶液的pH=2
B. 升高温度或增大浓度,HF的电离平衡常数都将增大
C. 两溶液混合不会产生沉淀
D. 向饱和的CaF2溶液中加入少量CaCl2固体后,溶度积常数Ksp一定比之前减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知某纯碱试样中含有杂质NaCl,为了确定试样中纯碱的质量分数,可测定其在化学反应中生成CO2的质量,实验装置如下(铁架台及夹持仪器均已省略)。
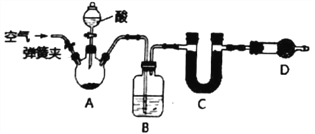
完成下列填空:
(1)B装置中的试剂是_____________,作用是_____________________________。
(2)D装置的作用是___________________________________。
II.测定试样中纯碱质量分数的某次实验步骤如下:①将10.000g纯碱试样放入A中 ②称量C(U型管+碱石灰,下同),质量为l05.160g ③使用分液漏斗滴加足量的酸,使充分反应 ④打开A的弹簧夹,缓缓鼓入一定量的空气 ⑤再次称量C ⑥重复步骤④和⑤,最后得到C的质量为109.l66g。
(3)步骤③中,滴加的酸最好选用________。
a、浓硝酸 b、稀盐酸 c、浓硫酸 d、稀硫酸
当看到____________________现象时即可进行第④步操作。
(4)步骤⑥的目的是_______________________________________________。
(5)由实验数据可知,试样中纯碱的质量分数为_________________(保留3位小数)。
(6)甲同学用上述装置测定某试样中纯碱的质量分数,结果偏高,请帮助他找出造成实验误差的原因。_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甘氨酸亚铁[(NH2CH2COO)2Fe]是一种补铁强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组在实验室利用直接合成法制各甘氨酸亚铁。有关物质性质如下所示:
甘氨酸( NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇、 | 易溶于水和乙醇, | 易溶于水, |
两性化合物 | 有强酸性和还原性 | 难溶于乙醇 |
实验过程及装置图如下(夹持和加热仪器已省略):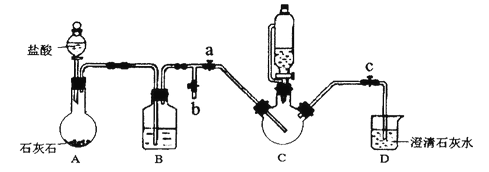
I.合成:在C中加入0.10mol甘氨酸、0.05mol硫酸亚铁、少量柠檬酸和200mL水,利用CO2将C装置中的空气排净,然后在40℃恒温条件下用磁力搅拌器不断搅拌,并用恒压滴液漏斗向C中滴加6mol·L-1NaOH溶液调节pH到6左右,使反应物充分反应。
II.分离:加入无水乙醇,立即出现白色沉淀。将沉淀进行过滤、洗涤,收集滤渣。
Ⅲ.提纯:将滤渣溶解于适量的蒸馏水中,然后结晶、过滤,将纯化后的产品放入真空干燥箱中干燥后称重。
回答下列问题:
(1)B装置的作用是______________;
(2)能证明C装置中空气排净的现象是______________;向C中滴加NaOH溶液之前应该停止滴加盐酸,且关闭止水夹____________,打开止水夹________
(3)“合成”中加入柠檬酸的作用是______________:请写出合成甘氨酸亚铁的化学方程式_________。
(4)加入乙醇的目的是________;“提纯”时用的结晶方法为________________
(5)通过测量得知:等浓度(NH2CH2COO)2Fe 溶液导电能力远小于FeSO4溶液。暴露在空气中,(NH2CH2COO)2Fe溶液比FeSO4溶液难被氧化,请分析原因为________
(6)若产品质量为ag,则产率为________ %。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下的密闭容器中发生反应:C(s)+CO2(g)=2CO(g).下列说法不正确的是( )
A.将碳块磨成粉末可加快反应速率
B.增加碳的质量可加快反应速率
C.升高温度可加快反应速率
D.容器体积不变时,向容器中充入氦气,反应速率不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法标出下列反应中电子转移的方向和数目:_____________。
MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
此反应中,还原剂是 _______,氧化剂是 ________;_____元素被氧化,__元素被还原。由此可知,氧化还原反应的实质是__________________________________________。根据你的理解再写一个常见的氧化还原反应的化学方程式: _______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个1L的密闭容器中,加入2molA和1molB进行如下反应:2A(g)+2B(g)![]() 3C(?)+D(?)。反应一段时间后达到平衡,测得生成0.6molC,且反应前后压强之比为15∶11(相同温度下测量),则下列说法正确的是( )
3C(?)+D(?)。反应一段时间后达到平衡,测得生成0.6molC,且反应前后压强之比为15∶11(相同温度下测量),则下列说法正确的是( )
A. 该反应的化学平衡常数K约为0.043
B. 增加C的物质的量,B的平衡转化率不变
C. 增大该体系的压强,平衡正向移动,化学平衡常数增大
D. A的平衡转化率是40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气。某校研究性学习小组拟设计下列实验验证这一事实。

(1)该小组设计了如上图所示的实验装置,检查该装置气密性的操作是______________________。
(2)若1.30g锌粒完全溶解,氢氧化钠洗气瓶增重0.64g(烧瓶中残留气体忽略不计,下同),则圆底烧瓶中发生反应的化学方程式为________________________________。
(3)是否使用橡胶管,对实验结果___________(填“有”或“无”) 影响。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com