
【题目】下列关于碱金属元素的说法正确的是( )
①原子结构的相同点是最外层电子数相同,都为1
②原子结构的不同点是随核电荷数的增加,电子层数增多,原子半径增大
③具有相似的化学性质,都是活泼金属
④都具有强还原性,在化合物中显![]() 价
价
⑤化学性质有差别,从Li到Cs,失电子能力逐渐增强
A.①③④B.①③⑤C.②④⑤D.①②③④⑤
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基。I可以用E和H在一定条件下合成:

已知以下信息:① A的核磁共振氢谱表明其只有一种化学环境的氢;
②R—CH=CH2![]() R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
R—CH2CH2OH;③化合物F苯环上的一氯代物只有两种;④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
请回答下列问题:
(1)A的化学名称为______________。
(2)D的结构简式为_____________。
(3)E的分子式为_________________。
(4)F生成G的化学方程式为________________________,该反应类型为__________。
(5)I的结构筒式为____________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:
①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,符合以上条件的同分异构体共有___________种。
J的一种同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变)发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。测得H2的物质的量随时间变化如图所示(图中字母后的数字表示对应的坐标)。该反应在8~10 min内CO2的平均反应速率是
CH3OH(g)+H2O(g) ΔH<0。测得H2的物质的量随时间变化如图所示(图中字母后的数字表示对应的坐标)。该反应在8~10 min内CO2的平均反应速率是

A. 0.5 mol·L-1·min-1B. 0.1 mol·L-1·min-1
C. 0 mol·L-1·min-1D. 0.125 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ToC下,向体积为2 L的恒容密闭容器中通入NO2和O2,发生反应:4NO2(g)+O2(g)![]() 2N2O5(g)ΔH<0,部分实验数据如下表。下列说法不正确的是
2N2O5(g)ΔH<0,部分实验数据如下表。下列说法不正确的是
时间/s | 0 | 5 | 10 | 15 |
n(NO2)/mol | 8.00 | n1 | n2 | 4.00 |
n(O2)/mol | 2.00 | 1.25 | 1.00 | n3 |
A. 5s内NO2的平均反应速率为0.3 mol/(Ls)
B. 若10 s时,再向容器中充入2 mol N2O5(g),则新平衡下,NO2的体积分数将增大
C. 若5 s 时,改在绝热恒容下达平衡,新平衡下的平衡常数比原平衡的小
D. ToC,该反应的平衡常数为0.125,反应物的平衡转化率均为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是亚硝酸根离子与钠离子组成的工业盐,具有咸味,其水溶液呈碱性.亚硝酸钠有毒,含有工业盐的食品对人体危害很大,有致癌性.加热到320℃以上则分解,生成氧气,氮气和氧化钠,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2.
(1)人体正常的血红蛋白含有Fe2+.若误食NaNO2,则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是___________________________(填序号).
A.亚硝酸盐被还原 B.维生素C是氧化剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是氧化剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是_________________(填序号).
A.测定这两种溶液的pH B.用筷子蘸取固体品尝味道
C.加强热收集气体检验 D.用HNO3酸化的AgNO3鉴别
(3)亚硝酸钠受热分解的化学反应方程式为:4NaNO2![]() 2N2↑+3O2↑+2Na2O
2N2↑+3O2↑+2Na2O
①从氧化还原反应角度分析,该反应说明NaNO2具有_____________________.(填氧化性、还原性或者既有氧化性又有还原性)
②该反应中的还原产物为______________________(写名称)
③若反应中转移3mol电子,得到Na2O的质量为________________g.
(4)己知Cl2具有强氧化性,能将溶液中的NO2﹣氧化为NO3﹣同时生成盐酸,请写出NaNO2溶液中通入Cl2的离子反应方程式____________________________________________________________________________.
(5)某工厂废液中,含2%~5%的NaNO2,直接排放会造成污染,NH2Cl能使NaNO2转化为不引起二次污染的N2,反应的化学方程式为______________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L的恒容密闭容器中加入![]() 和一定量的CO后,发生反应:
和一定量的CO后,发生反应:![]() ,CO和
,CO和![]()
![]() 的物质的量随时间的变化如下表表示:则下列说法错误的是( )
的物质的量随时间的变化如下表表示:则下列说法错误的是( )
| 0 | 3 | 10 | 12 |
| 2 | 1 |
|
|
| 0 | 1 |
|
|
A.在![]() 内,用
内,用![]() 表示的平均反应速率为
表示的平均反应速率为![]()
B.在该条件下,上述反应的平衡常数为3
C.反应达平衡时,![]()
![]() 的体积分数为
的体积分数为![]()
D.要增大反应速率且增大![]()
![]() 在混合物中的体积分数,可采用压缩体积,增大体系压强的措施
在混合物中的体积分数,可采用压缩体积,增大体系压强的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z在周期表中位置关系如图所示
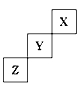
(1)X元素的名称是___________。
(2)Y在元素周期表中的位置是__________,它形成单质的化学式是_________。
(3)Z元素的原子结构示意图为__________。写出Z单质与铁反应的化学反应方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能量是人类生存基础,因此化学反应与能量关系一直是研究热点,贯穿于生活和生产各个领域 .
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为_______
(2)化学反应中放出的热能(焓变),△H与反应物和生成物的键能E有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=-185kJ/mol, E(H-H)=436kJ/mol,E(Cl-Cl)=243kJ/mol。
则E(H-Cl)=___________
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,已知:
2Cu(s)+![]() O2(g)=CuO(s) △H=-169kJ.mol-1.
O2(g)=CuO(s) △H=-169kJ.mol-1.
C(s)+![]() O2(g)=CO(g) △H=-110.5kJ.mol-1
O2(g)=CO(g) △H=-110.5kJ.mol-1
2Cu(s)+O2(g)=2CuO(s) △H=-314kJ.mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu和CO的热化学方程__________
(4)如图是N2和H2反应生成2molNH3过程中能量变化示意图
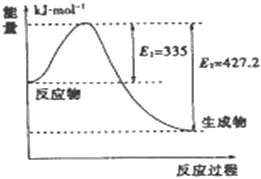
①请计算每生成1moNH3放出热量为___________
②若起始时向容器内放入1moN2和3molH2达平衡后N2的反应体积分数为20%,则反应放出的热量为Q1kJ,则Q1的数值为___________
(5)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是_______

A.氧分子的活化包括O-O键的断裂与C-O键的生成
B.每活化一个氧分子放出0.29eV的能量
C.水可使氧分子活化反应的活化能降低0.42eV
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是

A. 图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的平衡常数与反应温度的关系曲线,说明该反应的ΔH<0
B. 图乙是室温下H2O2催化分解放出氧气的反应中c(H2O2 )随反应时间变化的曲线,说明随着反应的进行H2O2分解速率逐渐减小
C. 图丙是室温下用0.1000 mol·L1NaOH溶液滴定20.00 mL 0.1000 mol·L1某一元酸HX的滴定曲线,说明HX是一元强酸
D. 图丁是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+ )与c(SO42)的关系曲线,说明溶液中c(SO42 )越大c(Ba2+ )越小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com