
【题目】能量是人类生存基础,因此化学反应与能量关系一直是研究热点,贯穿于生活和生产各个领域 .
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为_______
(2)化学反应中放出的热能(焓变),△H与反应物和生成物的键能E有关。
已知:H2(g)+Cl2(g)=2HCl(g) △H=-185kJ/mol, E(H-H)=436kJ/mol,E(Cl-Cl)=243kJ/mol。
则E(H-Cl)=___________
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,已知:
2Cu(s)+![]() O2(g)=CuO(s) △H=-169kJ.mol-1.
O2(g)=CuO(s) △H=-169kJ.mol-1.
C(s)+![]() O2(g)=CO(g) △H=-110.5kJ.mol-1
O2(g)=CO(g) △H=-110.5kJ.mol-1
2Cu(s)+O2(g)=2CuO(s) △H=-314kJ.mol-1
则工业上用炭粉在高温条件下还原CuO制取Cu和CO的热化学方程__________
(4)如图是N2和H2反应生成2molNH3过程中能量变化示意图
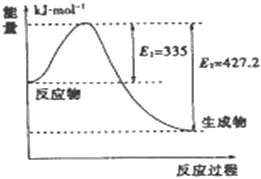
①请计算每生成1moNH3放出热量为___________
②若起始时向容器内放入1moN2和3molH2达平衡后N2的反应体积分数为20%,则反应放出的热量为Q1kJ,则Q1的数值为___________
(5)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是_______

A.氧分子的活化包括O-O键的断裂与C-O键的生成
B.每活化一个氧分子放出0.29eV的能量
C.水可使氧分子活化反应的活化能降低0.42eV
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
【答案】CH3OH(l)+![]() O2(g)═CO2(g)+2H2O (l) △H=-704kJ/mol 432kJ/mol C(s)+2CuO(s)=Cu2O(s)+CO(g)△H=+34.5kJmol-1 46.1kJ 18.44 C
O2(g)═CO2(g)+2H2O (l) △H=-704kJ/mol 432kJ/mol C(s)+2CuO(s)=Cu2O(s)+CO(g)△H=+34.5kJmol-1 46.1kJ 18.44 C
【解析】
依据燃烧热概念是1mol可燃物完全燃烧生成稳定氧化物放出的热量书写热化学方程式,标注物质聚集状态和对应焓变写出;依据反应的焓变△H=反应物键能总和-生成物键能总和计算;依据热化学方程式和盖斯定律计算得到所需热化学方程式;分析图象N2和H2反应生成2mol NH3过程中能量变化示意图计算每生成1mol NH3放出的热量。
(1)16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,32g甲醇即1mol,燃烧生成二氧化碳和液态水放热704kJ,标注物质聚集状态和对应焓变写出热化学方程式为:CH3OH(l)+![]() O2(g)═CO2(g)+2H2O (l) △H=-704kJ/mol;故答案为: CH3OH(l)+
O2(g)═CO2(g)+2H2O (l) △H=-704kJ/mol;故答案为: CH3OH(l)+![]() O2(g)═CO2(g)+2H2O (l) △H=-704kJ/mol;
O2(g)═CO2(g)+2H2O (l) △H=-704kJ/mol;
(2)H2(g)+Cl2(g)═2HCl(g)△H=-185kJ/mol;E(H-H)=436kJ/mol,E(Cl-Cl)=243kJ/mol
△H=反应物键能总和-生成物键能总和得到:-185kJ/mol=436KJ/mol+243KJ/mol-2E(H-Cl)
则E(H-Cl)=432kJ/mol;故答案为:432kJ/mol;
(3)已知:①2Cu(s)+![]() O2(g)=CuO(s) △H=-169kJ.mol-1
O2(g)=CuO(s) △H=-169kJ.mol-1
②C(s)+![]() O2(g)=CO(g) △H=-110.5kJ.mol-1
O2(g)=CO(g) △H=-110.5kJ.mol-1
③2Cu(s)+O2(g)=2CuO(s) △H=-314kJ.mol-1
用炭粉在高温条件下还原CuO制取Cu2O和CO的化学方程式为C(s)+2CuO(s)=Cu2O(s)+CO(g),该反应可以是②-③-![]() ×①,反应的焓变是-110.5kJmol-1-(-314kJmol-1)-
×①,反应的焓变是-110.5kJmol-1-(-314kJmol-1)-![]() ×(-169kJmol-1)=+34.5kJmol-1,
×(-169kJmol-1)=+34.5kJmol-1,
故答案为:C(s)+2CuO(s)=Cu2O(s)+CO(g)△H=+34.5kJmol-1。
(4)①图象分析可知,N2和H2反应生成2mol NH3过程中能量变化示意图可知反应放热427.2KJ-335KJ=92.2kJ,每生成1mol NH3放出热量46.1kJ;故答案为:46.1kJ;
②如图是N2和H2反应生成2mol NH3过程中能量变化示意图,反应焓变△H=335kJ/mol-427.2kJ/mol=-92.2kJ/mol,
N2(g)+3H2(g)=2NH3(g)△H=-92.2kJ/mol
1 3 0
0.2 0.6 0.4
生成0.4mol氨气放热=![]() ×92.2KJ=18.44kJ;故答案为:18.44;
×92.2KJ=18.44kJ;故答案为:18.44;
(5)A、根据图象分析,氧分子活化过程O-O键断裂,生成C-O键,所以氧分子的活化是O-O的断裂与C-O键的生成过程,故A正确;
B、由图可知,反应物的总能量高于生成物的总能量,因此每活化一个氧分子放出0.29eV的能量,故B正确;
C、化能反应过程中存在多步反应的活化能,整个反应的活为活化能较大者,根据能量图分析,整个反应的活化能为活化能较大者,则没有水加入的反应活化能为E=0.75eV,有水加入的反应的活化能为E=0.57eV,所以水可使氧分子活化反应的活化能降低0.75eV-0.57eV=0.18eV,故C错误;
D、活化氧可以快速氧化二氧化硫,而炭黑颗粒可以活化氧分子,因此炭黑颗粒可以看作大气中二氧化硫转化为三氧化硫的催化剂,故D正确;
答案为C。


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,含少量碳及二氧化硅)为原料制备的流程如下:

(1)废铁渣进行“粉碎”的目的是_____。
(2)①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为_____。
②酸浸时,通入O2的目的是_____。
(3)滤渣的主要成分为____(填化学式)。
(4)“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;在酸性条件下,再用K2Cr2O7标准溶液滴定Fe2+(Cr2O72-![]() 被还原为Cr3+),该滴定反应的离子方程式为_____。
被还原为Cr3+),该滴定反应的离子方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碱金属元素的说法正确的是( )
①原子结构的相同点是最外层电子数相同,都为1
②原子结构的不同点是随核电荷数的增加,电子层数增多,原子半径增大
③具有相似的化学性质,都是活泼金属
④都具有强还原性,在化合物中显![]() 价
价
⑤化学性质有差别,从Li到Cs,失电子能力逐渐增强
A.①③④B.①③⑤C.②④⑤D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合元素周期表,回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图 1 中用实线补全元素周期表 的边界____________
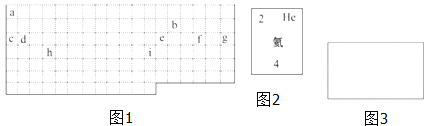
(2)表中所列元素,属于短周期元素的有____________;属于主族元素的有____________;g 元素位于第____________ 周期____________ 族;i 元素位于第____________ 周期____________族.
(3)元素 f 是第_______周期、第_______ 族元素,请在如图 3 所示的方框中按 氦元素(图 2)的式样写出该元素的原子序数、元素符号、元素名称、相对原子 质量_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.标准状况下,22.4 LCCl4含有的分子数为NA
B.标准状况下,aL氧气和氮气的混合气体含有的分子数约为![]()
C.46g NO2和N2O4的混合气体中含有的原子数为6NA
D.56gFe与足量的盐酸反应,转移的电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中离子方程式及其评价均合理的是( )
选项 | 化学反应及离子方程式 | 评价 |
A | 氧化亚铁溶于稀硝酸FeO+2H+=Fe2++H2O | 碱性氧化物与酸反应生成盐和水,正确 |
B | 向亚硫酸铵溶液中加少量氢氧化钡溶液Ba2++SO | 复分解反应,有沉淀生成,正确 |
C | 含nmolFeBr2的溶液中通入nmolCl2完全反应:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 氧化还原反应离子方程式满足元素守恒、电子守恒、电荷守恒,正确 |
D | 氯化铁溶液中滴入硫氰化钾溶液:Fe3++3SCN-=Fe(SCN)3 | 复分解反应,无气体生成,无沉淀生成,不正确 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液里Ca2+的浓度一般采用mgcm-3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
[配制KMnO4标准溶液]如图是配制100mLKMnO4标准溶液的过程示意图。
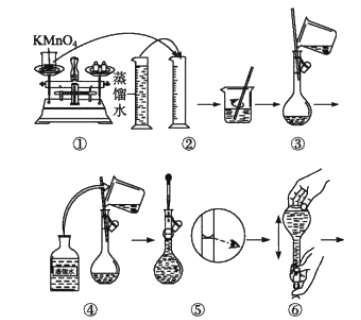
(1)根据图示判断,其中不正确的操作有___(填序号)。
(2)其中确定100mL溶液体积的容器是___(填名称)。
(3)如果忘记洗涤烧杯,所配制的溶液浓度将___;如果定容时仰视,所配制的溶液浓度将___(填“偏大”或“偏小”)。
[测定血液样品中Ca2+的浓度]抽取血样40.00mL,经过上述处理后得到草酸,再用0.020molL-1KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗24.00mLKMnO4溶液。
(4)请书写草酸与KMnO4溶液反应的离子方程式:___。
(5)经过计算,血液样品中Ca2+的浓度为___mgcm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿![]() 主要成份为
主要成份为![]() ,还含有
,还含有![]() 、
、![]() 等杂质
等杂质![]() 为主要原料生产红矾钠晶体
为主要原料生产红矾钠晶体![]() ,其主要工艺流程如图:
,其主要工艺流程如图:
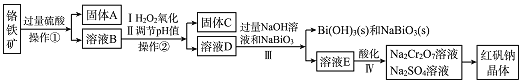
已知:![]() 在碱性条件下能将
在碱性条件下能将![]() 氧化为
氧化为![]() 。
。
![]() 固体A为 ______。
固体A为 ______。
![]() 实验室中操作
实验室中操作![]() 的名称为_____________。
的名称为_____________。
![]() 固体C中含有的物质是
固体C中含有的物质是![]()
![]() 和
和![]() ,则
,则![]() 的作用是 ______ 。
的作用是 ______ 。
已知:![]() ,
,![]() ,当
,当![]() 时
时![]() 开始沉淀.室温下,Ⅱ中需调节溶液pH范围为 ___
开始沉淀.室温下,Ⅱ中需调节溶液pH范围为 ___ ![]() 杂质离子浓度小于
杂质离子浓度小于![]() 视为沉淀完全
视为沉淀完全![]() 。
。
![]()
![]() Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是 ______
Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是 ______ ![]() 结合化学方程式回答
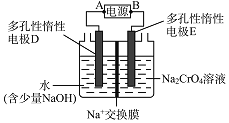
结合化学方程式回答![]() ;工业上也可设计如图示装置,用锂离子电池
;工业上也可设计如图示装置,用锂离子电池![]() 为难电离锂碳化合物
为难电离锂碳化合物![]() 为电源,电解
为电源,电解![]() 溶液制取
溶液制取![]() ,该装置工作时E电极的名称是 ___ 极;电源的A极的电极反应式为 ______
,该装置工作时E电极的名称是 ___ 极;电源的A极的电极反应式为 ______ ![]() 当电解过程中转移了
当电解过程中转移了![]() 电子时,理论上右侧溶液的质量减少 ______g。
电子时,理论上右侧溶液的质量减少 ______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
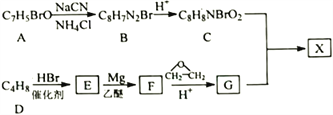
【题目】治疗癌症的有机小分子酯类药物X被批准使用。以芳香族化合物A为主要原料合成X的路线如下:
已知:
①核磁共振氢谱显示A有3种化学环境的氢,E只有1种化学环境的氢;
②![]()
③![]()
回答下列问题:
(1)A的名称是______________________;G中官能团名称是____________________。
(2)C在一定条件下反应生成高分子化合物,该反应的化学方程式为:__________________________。
(3)D生成E的反应类型为_____________________。
(4)X的结构简式为_____________________。
(5)已知:同一个碳原子若连有两个—OH时,易转化成![]() 。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
①苯环上有两个取代基;
②能发生银镜反应,且在碱性条件下水解的两种产物也能发生银镜反应。
(6)参照上述合成路线和信息,用乙烯、乙醚、环氧乙烷为原料(其他无机试剂任选)合成1,6-己二酸_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com