
 某校化学研究性学习小组设计如下实验方案,测定放置已久的NaHCO3样品中Na2CO3的质量分数.填写下列空白.
某校化学研究性学习小组设计如下实验方案,测定放置已久的NaHCO3样品中Na2CO3的质量分数.填写下列空白.
| ||
| 9.7g |


科目:高中化学 来源: 题型:
| A、乙烯的结构简式CH2CH2 |
| B、Na2O2中氧元素的化合价为-2 |
C、Cl-的结构示意图: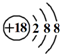 |
| D、乙烷的结构简式:CH3CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O、S、Na的原子半径依次减小 |
| B、LiOH、KOH、CsOH的碱性依次增强 |
| C、HF、NH3、SiH4的稳定性依次增强 |
| D、HCl、HBr、HI的还原性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、共价化合物中可能含有离子键 |
| B、最外层有2个电子的原子一定在ⅡA族 |
| C、离子化合物中可能含共价键 |
| D、H2O的稳定性很强是因为其分子间能形成氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如表所示,
用0.1320mol/L的HCl溶液滴定未知浓度的NaOH溶液,实验数据如表所示,| 实验编号 | 待测NaOH溶液体积/mL | HCl溶液体积/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 24.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2和NH4Cl反应 |
| B、钢铁生锈 |
| C、H2与CuO高温反应 |
| D、乙醇与O2的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将Cl2通入溴化亚铁溶液:2Br-+Cl2═Br2+2Cl- |
| B、用稀硫酸吸收氨气:NH3+H+═NH4+ |
| C、AlCl3溶液中加入过量的氨水:Al3++4NH3?H2O═AlO2-+4NH4+ |
| D、碳酸氢钠和稀硫酸反应:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 结构及性质 | ||
| A | 原子最外层电子数是内层电子总数的
| ||
| B | B是常见化肥的主要元素,单质常温下呈气态 | ||
| C | 单质被誉为“信息革命的催化剂”,是常用的半导体材料 | ||
| D | 通常情况下,D没有正化合价,A、B、C、E都能为D形成化合物 | ||
| E | 与D可以形成原子个数比分别为2:1,1:1的两种液体化合物X和Y |
查看答案和解析>>
科目:高中化学 来源: 题型:


| Ni△ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com