
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
A. 常温常压下,56g丙烯与环丁烷的混合气体中含有4NA个碳原子
B. 7.8g 苯中含有的碳碳双键数目为0.3NA
C. 常温常压下,1.8g重氢甲基(—CD3)中含有的电子数为NA
D. 10g质量分数为46%的乙醇水溶液含有的氢原子总数为0.6NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】2-硝基-1,3-苯二酚由间苯二酚先磺化,再硝化,后去磺酸基生成。原理如下:
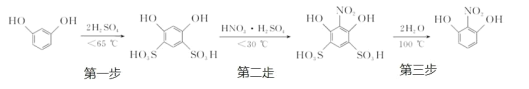
部分物质的相关性质如下:
名称 | 性状 | 熔点/℃ | 水溶性(常温) |
间苯二酚 | 白色针状晶体 | 110.7 | 易溶 |
2-硝基-1,3-苯二酚 | 桔红色针状晶体 | 87.8 | 难溶 |
制备过程如下:
第一步:磺化。称取一定质量的间苯二酚,碾成粉末放入烧瓶中,慢慢加入适量浓硫酸并不断搅拌,控制温度在一定范围内反应 15 min(如图 1)。
第二步:硝化。待磺化反应结束后将烧瓶置于冷水中,充分冷却后加入“混酸”,控制温度继续搅15 min。第三步:蒸馏。将硝化反应混合物的稀释液转移到圆底烧瓶 B 中,然后用图 2 所示装置进行水蒸气蒸馏,收集馏出物,得到 2-硝基-1,3-苯二酚粗品。
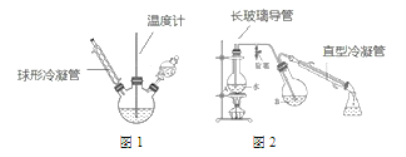
请回答下列问题:
(1)磺化步骤中控制温度最合适的范围为(填字母)________。
a.30 ℃~60 ℃ b.60 ℃~65 ℃ c.65 ℃~70 ℃ d.70 ℃~100 ℃
(2)酚羟基邻对位的氢原子比较活泼,均易被取代,请分析第一步磺化引入磺酸基基团(-SO3H)的作用是_______________________。
(3)硝化步骤中制取“混酸”的具体操作是______________________。
(4)下列说法正确的是_______________。
a 直型冷凝管内壁中可能会有红色晶体析出
b 图 2 中的冷凝管能用图 1 中的冷凝管代替
c 烧瓶A中长玻璃管起稳压作用,既能防止装置中压强过大引起事故,又能防止压强过小引起倒吸。
(5)蒸馏步骤中,水蒸气蒸馏的作用是__________________。可通过________(填操作)进一步提纯 2-硝基-1,3-苯二酚。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,11.2LCHC13中含有的氯原子数目为1.5NA
B.10.0g质量分数为46%的乙醇溶液与足量钠反应产生的H2数目为0.05NA
C.常温常压下,124gP4中含σ键数目为4NA
D.向1L1mol·L-1NH4Cl溶液中加入氨水至中性,溶液中![]() 数目为NA
数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的表达正确的是( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的价电子轨道表示式:![]()
C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物结构如图,下列说法中正确的是![]()

A. 该物质的化学式为C15H8O8BrCl
B. 该物质能与![]() 溶液发生显色反应
溶液发生显色反应
C. 1mol该物质最多能与3mol溴水发生加成反应
D. 一定条件下,1mol该物质最多能与8molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸盐与钴(Ⅲ)形成的一种配合物[Co(NH3)5NO2]Cl2的制备流程如下:
CoCl2·6H2O![]() [Co(NH3)5Cl]Cl2
[Co(NH3)5Cl]Cl2![]() [Co(NH3)5NO2]Cl2
[Co(NH3)5NO2]Cl2
(1)Co2+基态核外电子排布式为___。
(2)配合物[Co(NH3)5Cl]Cl2中与Co3+形成配位键的原子为___(填元素符号);配离子[Co(NH3)5NO2]2+的配体中氮原子的杂化轨道类型为___。
(3)NO![]() 的空间构型为___,与它互为等电子体的分子为___(写化学式)。
的空间构型为___,与它互为等电子体的分子为___(写化学式)。
(4)H2O2与H2O可以任意比例互溶,除因为它们都是极性分子外,还因为___。
(5)1mol[Co(NH3)5Cl]Cl2中含有σ键的数目为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用于治疗阿尔茨海默病的某种药物中间体H的合成路线如图所示:
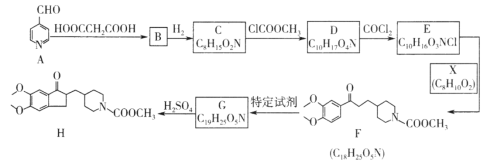
已知:i.![]()
ii.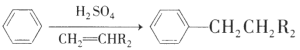
(1)A中含氧官能团的名称是___________;B→C的反应类型是______________。
(2)G的结构简式是___________________。
(3)E→F的化学方程式是______________________。
(4)芳香化合物Y是X的同分异构体,1molY可与2molNaOH反应,Y共有__________种(不含立体结构),其中核磁共振氢谱为4组峰,峰面积比为1:6:2:1的结构简式是______________________。
(5)设计由乙醇和HOOCCH2COOH制备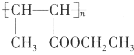 的合成路线(无机试剂任选)。__________
的合成路线(无机试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题。
(1)氧化剂______,还原剂________
(2)氧化产物______,还原产物_______
(3)氧化剂与还原剂的物质的量之比:_________________________
(4)用单线桥的方法表示该反应的电子转移情况。________________________
(5)用双线桥的方法表示该反应的电子转移情况。_________________________
(6)当有8mol NH3参加反应时,转移的电子数目为__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com