
ЁОЬтФПЁПЪЕбщЪвХфжЦ500mL0.2molЁЄL-1ЕФNa2SO4ШмвКЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЬюаДЯТСаЪЕбщВйзїВНжшжаЕФПеАзДІЃК
A.дкЬьЦНЩЯГЦШЁ___gNa2SO4ЙЬЬхЃЌАбЫќЗХдк___жаЃЌгУЪЪСПЕФеєСѓЫЎШмНтЃЛ
B.АбжЦЕУЕФШмвКаЁаФЕибизХ___зЂШы___жаЃЛ
C.МЬајЯђШнСПЦПжаМгШыеєСѓЫЎжСвКУцРыШнСПЦПОБПЬЖШЯпЯТ1ЁЋ2cmЪБЃЌИФгУ___аЁаФЕЮМгеєСѓЫЎжСШмвКАМвКУцзюЕЭДІгыПЬЖШЯпЫЎЦНЯрЧаЃЛ
D.гУЩйСПеєСѓЫЎЯДЕгЩеБФкБкКЭВЃСЇАє2ЁЋ3ДЮЃЌУПДЮЯДЕгвКвВаЁаФзЊШыШнСПЦПжаЃЌВЂЧсЧсвЁдШЃЛ
E.ИЧКУЦПШћЃЌЗДИДЩЯЯТЕпЕЙЃЌвЁдШЁЃ
ЃЈ2ЃЉЕкЃЈ1ЃЉЬтжаВйзїВНжшЕФе§ШЗЫГађЪЧ(ЬюБъКХ)___ЁЃ
ЃЈ3ЃЉЯТСаЧщПіжаЃЌЛсЪЙЫљХфШмвКХЈЖШЦЋИпЕФЪЧ___(ЬюБъКХ)ЁЃ
a.ШмНтНСАшЪБгаВПЗжвКЬхНІГі
b.МгеєСѓЫЎЪБЃЌВЛЩїГЌЙ§СЫПЬЖШЯп
C.дкЖЈШнЪБЃЌИЉЪгПЬЖШЯп
d.ШнСПЦПЪЙгУЧАФкБкеДгаЫЎжщ
ЁОД№АИЁП14.2 ЩеБ ВЃСЇАє 500mLШнСПЦП НКЭЗЕЮЙм ABDCE c
ЁОНтЮіЁП
(1)AЃЎвРОнn=CVЁЂm=nMМЦЫуашвЊШмжЪЕФжЪСПЃЛЙЬЬхжаЩеБжаШмНтЃЛ
BЃЎАбШмвКзЊШыШнСПЦПЪБвЊгУВЃСЇАєв§СїЃЛ
CЃЎгУНКЭЗЕЮЙмЯђШнСПЦПжаМгвКЬхЪБЃЌФмзМШЗМгвКжСПЬЖШЯпЃЛ
(2)ШмвКХфжЦВйзїВНжшгаЃКГЦСПЁЂШмНтЁЂвЦвКЁЂЯДЕгЁЂЖЈШнЁЂвЁдШЕШВйзїЃЛ
(3)ЗжЮіВйзїЖдШмвКЮяжЪЕФСПЁЂШмвКЬхЛ§ЕФгАЯьЃЌИљОнc=![]() ЗжЮіВйзїЖдЫљХфШмвКХЈЖШЕФгАЯьЁЃ
ЗжЮіВйзїЖдЫљХфШмвКХЈЖШЕФгАЯьЁЃ
(1)AЃЎ500L 0.2mol/LNa2SO4ШмвККЌгаШмжЪЕФЮяжЪЕФЮяжЪЕФСПЮЊЃК0.2mol/LЁС0.5L=0.1molЃЌЫљвдашвЊgNa2SO4ЙЬЬхЕФжЪСПЪЧ0.1molЁС142g/mol=14.2gЃЛГЦСПКУЕФСђЫсФЦЙЬЬхЗХдкЩеБжаШмНтЃЛ
BЃЎАбШмвКзЊШыШнСПЦПЪБвЊгУВЃСЇАєв§СїЃЌЫљвдАбжЦЕУЕФШмвКаЁаФЕибизХВЃСЇАєзЂШы500mLЕФШнСПЦПжаЃЛ
CЃЎгУНКЭЗЕЮЙмЯђШнСПЦПжаМгвКЬхЪБЃЌФмзМШЗМгвКжСПЬЖШЯпЃЌдђЯђШнСПЦПжаМгШыеєСѓЫЎжСвКУцРыШнСПЦПОБПЬЖШЯпЯТ1ЁЋ2cmЪБЃЌИФгУНКЭЗЕЮЙмаЁаФЕЮМгеєСѓЫЎжСШмвКАМвКУцзюЕЭДІгыПЬЖШЯпЫЎЦНЯрЧаЃЛ
(2)ШмвКХфжЦВйзїВНжшгаЃКГЦСПЁЂШмНтЁЂвЦвКЁЂЯДЕгЁЂЖЈШнЁЂвЁдШЕШВйзїЃЌдђВйзїВНжшЕФе§ШЗЫГађЪЧABDCEЃЛ
(3)aЃЎШмНтНСАшЪБгаВПЗжвКЬхНІГіЃЌдђСђЫсФЦЕФЮяжЪЕФСПМѕаЁЃЌЫљвдХфжЦХЈЖШЦЋЕЭЃЌЙЪaВЛбЁЃЛ
bЃЎМгеєСѓЫЎЪБЃЌВЛЩїГЌЙ§СЫПЬЖШЯпЃЌШмвКЕФЬхЛ§ЦЋДѓЃЌЪЙХфжЦШмвКХЈЖШЦЋЕЭЃЌЙЪbВЛбЁЃЛ
cЃЎдкЖЈШнЪБЃЌИЉЪгПЬЖШЯпЃЌШмвКЕФЬхЛ§ЦЋаЁЃЌЪЙХфжЦШмвКХЈЖШЦЋИпЃЌЙЪcбЁЃЛ
dЃЎШнСПЦПЪЙгУЧАФкБкеДгаЫЎжщЃЌЖдШмжЪКЭШмМСЖМЮогАЯьЃЌЫљвдХфжЦХЈЖШВЛБфЃЌЙЪdВЛбЁЃЛ
ЙЪД№АИЮЊЃКcЁЃ


 бЇЖјгХЯЮНгНЬВФФЯОЉДѓбЇГіАцЩчЯЕСаД№АИ
бЇЖјгХЯЮНгНЬВФФЯОЉДѓбЇГіАцЩчЯЕСаД№АИ аЁбЇПЮЬУзївЕЯЕСаД№АИ
аЁбЇПЮЬУзївЕЯЕСаД№АИ Н№ВЉЪПвЛЕуШЋЭЈЯЕСаД№АИ
Н№ВЉЪПвЛЕуШЋЭЈЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГгаЛњЮяMЕФЧђЙїФЃаЭШчЭМЫљЪОЃК
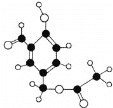
(1)ЧыаДГіЮяжЪMЕФЗжзгЪН_______КЌбѕЙйФмЭХУћГЦ_________
(2)MдквЛЖЈЬѕМўЯТЃЌПЩвдЗЂЩњЫЎНтЗДгІЃЌЩњГЩAЁЂBСНжжЮяжЪ(ЫќУЧЕФЯрЖдЗжзгжЪСПЙиЯЕAЃОB)ЁЃBПЩвдгУвдЯТЗНЗЈжЦЕУЃКX![]() Y
Y![]() Z
Z![]() W
W![]() BЁЃЦфжаWФмЗЂЩњвјОЕЗДгІЁЃдђIЪєгк________ЗДгІ(ЬюЗДгІРраЭ)
BЁЃЦфжаWФмЗЂЩњвјОЕЗДгІЁЃдђIЪєгк________ЗДгІ(ЬюЗДгІРраЭ)
(3)аДГіЗДгІЂђЕФЛЏбЇЗНГЬЪНЃК_____ЁЃЗДгІЂѓЕФЛЏбЇЗНГЬЪНЃК________ЁЃ
(4)1molAЗжБ№гыNaЁЂNaOHШмвКЗДгІЃЌЫљгУNaЁЂNaOHЮяжЪЕФСПЕФзюДѓжЕжЎБШЪЧ_______ЁЃ
(5)AгаЖржжЭЌЗжвьЙЙЬхЃЌЗћКЯЯТСаШ§ИіМўЕФЭЌЗжвьЙЙЬхга_______жжЃЌЦфжаЗжзгНсЙЙжажЛгаСљжжЧтдзгЕФНсЙЙМђЪНЮЊ__________
a.ЛЗЩЯжЛгаСНИіШЁДњЛљ
b.гыFeCl3ШмвКЯдзЯЩЋЃЛ
c.ФмЗЂЩњвјОЕЗДгІЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЊШЗШЯC6H5OHЁЂH2CO3ЁЂCH3COOHЕФЫсадЧПШѕЃЌФГЭЌбЇЩшМЦСЫШчЯТЭМЫљЪОзАжУЃЌвЛДЮЪЕбщМДПЩДяЕНФПЕФ(ВЛБибЁгУЦфЫћЫсадЮяжЪ)ЁЃ
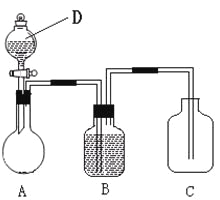
ЧыОнДЫЪЕбщЛиД№ЯТСаЮЪЬтЃК
(1)вЧЦїDЕФУћГЦЪЧ____________ЃЌЫљЪЂЗХЕФЪдМСгІЮЊ___________(ЬюЛЏбЇЪН)ЃЛ
(2)дкЩеЦПжазАФГПЩШмаде§бЮШмвКЃЌдђAжаЗДгІЕФРызгЗНГЬЪНЪЧ______________ЃЛ
(3)зАжУBжаЫљЪЂЕФЪдМСЪЧ_____________ЃЌЦфзїгУЪЧ___________________ЃЛ
(4)зАжУCжаЫљЪЂЕФЪдМСЪЧ________ЃЌCжаЗДгІЕФЛЏбЇЗНГЬЪНЪЧ____________ЃЛ
(5)ИљОнИУЪЕбщПЩвдЕУГіC6H5OHЁЂH2CO3ЁЂCH3COOHетШ§жжЮяжЪЕФЫсадЧПШѕЫГађЮЊ
______________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏКЯЮяHInдкЫЎШмвКжавђДцдквдЯТЕчРыЦНКтHIn(aqЃЌКьЩЋ) ![]() HЃЋ(aq)+ InЃ(aqЃЌЛЦЩЋ)ЙЪПЩзїЫсМюжИЪОМСЁЃХЈЖШЮЊ0.02mol/LЕФЯТСаШмвКЃКЂй бЮЫс Ђк ЪЏЛвЫЎ Ђл NaClШмвК Ђм NaHSO4ШмвК Ђн NaHCO3ШмвК Ђо АБЫЎЃЌЦфжаФмЪЙжИЪОМСЯдКьЩЋЕФЪЧ
HЃЋ(aq)+ InЃ(aqЃЌЛЦЩЋ)ЙЪПЩзїЫсМюжИЪОМСЁЃХЈЖШЮЊ0.02mol/LЕФЯТСаШмвКЃКЂй бЮЫс Ђк ЪЏЛвЫЎ Ђл NaClШмвК Ђм NaHSO4ШмвК Ђн NaHCO3ШмвК Ђо АБЫЎЃЌЦфжаФмЪЙжИЪОМСЯдКьЩЋЕФЪЧ
A. ЂмЂнB. ЂлЂнC. ЂйЂмD. ЂкЂо
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЃЌЕБMg(OH)2ЙЬЬхдкЫЎШмвКжаДяЕНЯТСаЦНКтЪБЃКMg(OH)2(s)![]() Mg2+(aq)+2OH-(aq)ЃЌШєЪЙЙЬЬхMg(OH)2ЕФСПМѕЩйЃЌЖјЧвc(Mg2+)ВЛБфЃЌПЩВЩШЁЕФДыЪЉЪЧЃК
Mg2+(aq)+2OH-(aq)ЃЌШєЪЙЙЬЬхMg(OH)2ЕФСПМѕЩйЃЌЖјЧвc(Mg2+)ВЛБфЃЌПЩВЩШЁЕФДыЪЉЪЧЃК
A. МгMgCl2B. МгH2OC. МгNaOHD. МгHCl
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAЪЧвЛжжКьзиЩЋН№ЪєбѕЛЏЮяЃЛBЁЂDЪЧН№ЪєЕЅжЪЃЛJЪЧвЛжжФбШмгкЫЎЕФАзЩЋЛЏКЯЮяЃЌЪмШШвзЗжНтЁЃ
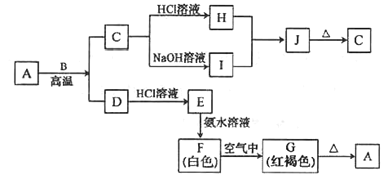
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉAЁЂEЁЂJЁЂGЕФЛЏбЇЪНЗжБ№ЮЊ___ЁЂ___ЁЂ___ЁЂ___ЁЃ
ЃЈ2ЃЉCзЊЛЏЮЊIЕФРызгЗНГЬЪНЮЊ___ЁЃ
ЃЈ3ЃЉHКЭIЗДгІЩњГЩJЕФРызгЗНГЬЪНЮЊ___ЁЃ
ЃЈ4ЃЉШчКЮМьбщEШмвКжаДѓСПДцдкЕФбєРызг?___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГгаЛњЮяAКЌЬМ76.6%ЃЌЧт6.4%ЃЌбѕ17%ЃЌЫќЕФЯрЖдЗжзгжЪСПдМЮЊМзЭщЕФ5.9БЖЃЌЧѓИУгаЛњЮяЕФЗжзгЪН___________ЁЃдкГЃЮТЯТЃЌИУгаЛњЮяПЩгыфхЫЎЗДгІЩњГЩАзЩЋГСЕэЃЌ0.5molЧЁКУгы1.5molBr2зїгУЃЌОнДЫШЗЖЈИУгаЛњЮяЕФНсЙЙМђЪН_____________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП(1)0.3molЕФЦјЬЌИпФмШМСЯввХ№Эщ(B2H6)дкбѕЦјжаШМЩеЃЌЩњГЩЙЬЬЌЕФШ§бѕЛЏЖўХ№КЭвКЬЌЫЎЃЌЗХГі649.5kJШШСПЃЌЦфШШЛЏбЇЗНГЬЪНЮЊ________ЁЃ
(2)ГЌвєЫйЗЩЛњдкЦНСїВуЗЩааЪБЃЌЮВЦјжаЕФNOЛсЦЦЛЕГєбѕВуЁЃПЦбЇМве§дкбаОПРћгУДпЛЏММЪѕНЋЮВЦјжаЕФNOКЭCOзЊБфГЩCO2КЭN2ЃЌЛЏбЇЗНГЬЪНЮЊЃК![]() ЃЌЮЊСЫВтЖЈдкФГжжДпЛЏМСзїгУЯТЕФЗДгІЫйТЪЃЌдкФГЮТЖШЯТгУЦјЬхДЋИаЦїВтЕУВЛЭЌЪБМфЕФNOКЭCOХЈЖШШчБэЃК
ЃЌЮЊСЫВтЖЈдкФГжжДпЛЏМСзїгУЯТЕФЗДгІЫйТЪЃЌдкФГЮТЖШЯТгУЦјЬхДЋИаЦїВтЕУВЛЭЌЪБМфЕФNOКЭCOХЈЖШШчБэЃК
ЪБМф/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/ molЁЄL-1 | 1.00ЁС10-3 | 4.50ЁС10-4 | 2.50ЁС10-4 | 1.50ЁС10-4 | 1.00ЁС10-4 | 1.00ЁС10-4 |
c(CO)/molЁЄL-1 | 3.60ЁС10-3 | 3.05ЁС10-3 | 2.85ЁС10-3 | 2.75ЁС10-3 | 2.70ЁС10-3 | 2.70ЁС10-3 |
ЧыЛиД№ЯТСаЮЪЬтЃК
ЂйЧА2sФкЕФЦНОљЗДгІЫйТЪІд(N2)ЃН____ЃЛ
ЂкЩЯЪіЬѕМўЯТЃЌИУЗДгІЕФЦНКтГЃЪ§ЮЊ____ЃЛ
ЂлЩЯЪіЬѕМўЯТЃЌВтЕУФГЪБПЬЗДгІЬхЯЕжаИїЮяжЪЕФЮяжЪЕФСПХЈЖШОљЮЊ0.01mol/LЃЌдђДЫЪБЗДгІДІгк___зДЬЌЁЃ(ЬюЁАЦНКтЁБЛђЁАЯђгвНјааЁБЛђЁАЯђзѓНјааЁБ)
(3)ЪЕбщЪвГЃгУ0.10mol/L KMnO4БъзМЫсадШмвКРДВтЖЈH2C2O4бљЦЗЕФДПЖШ(БъзМвКЕЮД§ВтвК)ЃЌЦфЗДгІдРэЮЊЃК5H2C2O4+2MnO4-+6H+=10CO2Ёќ+2Mn2++8H2OЁЃ
ЂйKMnO4БъзМвКгІзАдк____(ЬюЁАЫсЪНЁБЛђЁАМюЪНЁБ)ЕЮЖЈЙмЃЛ
ЂкЧхЫЎЯДОЛЕЮЖЈЙмКѓжБНгзАШыБъзМвКЃЌдђВтЖЈНсЙћЛс____ЃЛ(ЬюЁАЦЋДѓЁБЛђЁАЦЋаЁЁБЛђЁАВЛБфЁБ)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛКуЮТЁЂКуШнЕФУмБеШнЦїжаДцдкЛЏбЇЦНКтЃКH2(g)ЃЋI2(g) ![]() 2HI(g)ЃЌвбжЊH2КЭI2ЕФЦ№ЪМХЈЖШОљЮЊ0.10molL-1,ДяЕНЦНКтзДЬЌЪБHIЕФХЈЖШЮЊ0.16molL-1ЁЃШєH2КЭI2ЕФЦ№ЪМХЈЖШОљБфЮЊ0.20molL-1ЃЌдђЦНКтЪБH2ЕФХЈЖШЮЊЃЈ ЃЉ
2HI(g)ЃЌвбжЊH2КЭI2ЕФЦ№ЪМХЈЖШОљЮЊ0.10molL-1,ДяЕНЦНКтзДЬЌЪБHIЕФХЈЖШЮЊ0.16molL-1ЁЃШєH2КЭI2ЕФЦ№ЪМХЈЖШОљБфЮЊ0.20molL-1ЃЌдђЦНКтЪБH2ЕФХЈЖШЮЊЃЈ ЃЉ
A. 0.16molL-1 B. 0.08 molL-1 C. 0.04 molL-1 D. 0.02molL-1
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com