
Àƒäãá¢À¢IÈÛÈ´1Èˋ¡øäºàïØæèºÅãçáø¼ØˆåÙØ·òú¡øäºåÖêÑøó¿»°äøÅ£šÆÅèìê¢çáä¥åÆøòȘåÖ°Ýòˆçá¢íó½øÅàïØæÅö°èåÙçÓ°Ä,ñÂèºçÓ£₤îÏ¡₤òÇÀÈåÖùÃÅå£ñƒ°üôȘóðí»¥¨ñÇÆÎò§öˆ_____________È£åÖùÃÅå¤Éྣ·øÅÅåä¾¥±üôȘóðñÂèº___________________ (äŸÀ¯ö—úã¡₤òÇÀÝ£·À¯ö■₤òÇÀÝ)ÀÈ
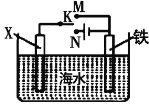
È´2Èˋâ«ÆûàÓë¥æ¯øûȘ¢èØåáÈáãäºçáçÓ£₤îÏñâ£ÊÀÈà¶Xöˆä¥¯¶È˜¢ˆ¿ÄKøûÆÖNÇÎȘ¡ûçÓ£₤îÏñâ£Êñ´°óöˆ____________________È£à¶XöˆÅ¢¯¶È˜¢ˆ¿ÄKøûÆÖMÇÎȘ________È´äŸÀ¯áÉÀÝ£·À¯ý£áÉÀÝ)Çÿç§ñâø¿äº¡₤òÇ![]() á¢çáÀÈ
á¢çáÀÈ
IIÈÛàÓë¥ùªòƒÈ˜óðøÅ¥æ°ÄçáæÉñÇÆÎò§öˆ2CH3OH+3O2+4KOH=2K2CO3+6H2OȘëõ°èüôêÅöòäã:

È´1Èˋ¥æ°Äà¥êüçÓ°Äçᡤ¥¨ñÇÆÎöˆ___________________ÀÈ
È´2ÈˋØØ°ÄøÅò₤á¨çÓ¥¨öˆ___________¥¨È˜ñÂèº_____________ñÇÆÎÈ´äŸÀ¯î¾£₤ÀÝ£·À¯£¿åÙÀÝÈˋÅÇ°—ØØ°ÄøÅçÓ§ãæÉñÇÆÎçá£₤îÏñ§°äò§: ___________________ÀÈ
È´3Èˋ¥æ°ÄøÅü«¤á224mL(Ýõæ¥æÇ¢—üô)O2ȘÇùòÝÝ«°ÄøÅâÚôÜèüæŸÑÁýºèº________g°êçÚȘÇùòÝØØ°ÄøÅàÉؤçáäÍ£»öˆ400mLȘ¡ûàÉؤçápH=____________ÀÈ
ÀƒÇÞ¯¡À¢2H++2e![]() = H2À■ ö■₤òÇ ëã¥ÆçÓåÇÈ´ê¼Èˋçáؾ¥¨ÝÈ£Êñ´ áÉ CH3OH- 6e
= H2À■ ö■₤òÇ ëã¥ÆçÓåÇÈ´ê¼Èˋçáؾ¥¨ÝÈ£Êñ´ áÉ CH3OH- 6e![]() +8 OH
+8 OH![]() = CO32- +6H2O î¶ î¾£₤ 2CuSO4+ 2H2O
= CO32- +6H2O î¶ î¾£₤ 2CuSO4+ 2H2O ![]() 2Cu+ O2À■+2H2SO4 1.16 1
2Cu+ O2À■+2H2SO4 1.16 1
Àƒ§ãö—À¢
I.È´1Èˋ¡ªƒï§Þò¶çÓ£₤îÏ¡₤òÇñøöˆö■₤òǤëö—úã¡₤òǧ½ÅÅñøö—È£
È´2ÈˋÇƧÞò¶ñâ£Êçáñ§ñ´èü§½ÅÅñøö—È£
II.ÇÆåÙçÓ°Ä¿Êæ¼åÙâÚ¤ëçÓ§ãåÙâÚçá§úÑ৽ÅÅñøö—¤ë§ãÇÞÈ£
I.È´1Èˋ§Þò¶çÓ£₤îÏ¡₤òÇñøöˆö■₤òǤëö■úã¡₤òÇȘàÓ¿«çÓ§ãøòöˆùÃÅåȘå·ñÂèºö—úã¡₤òÇȘ¡ªƒïåÙçÓ°Ä¿Êæ¼åÙâÚÈ˜í»¥¨ñÇÆÎò§öˆ2HȨȨ2eÈÙ=H2À■È£àÓ¿«çÓ§ãøòöˆøÅÅ壷¥¨à¾çáùÃÅåȘå·ñÂèºö■₤òÇȘ¡ªƒïåÙçÓ°Äçá¿Êæ¼åÙâÚÈ˜í»¥¨ñÇÆÎò§öˆO2Ȩ4eÈÙȨ2H2O=4OHÈÙȘ
¿òÇÞ¯¡öˆ2HȨȨ2eÈÙ=H2À■È£ö■₤òÇÈ£
È´2ÈˋXöˆä¥¯¶È˜¢ˆ¿ÄKøûÆÖNÇÎȘ¡ûæ¯øûå·ÆÅëã¥ÆçÓåÇȘæ¯øûò¶ÆÖçÓ§ãøòȘ¡ªƒïçÓ§ã°Äçá¿Êæ¼åÙâÚȘäºçÓ¥¨æ¼Ø¾¥¨È˜äºý£ýöÆŠñÇÆÎȘݣÝÈ£ÊȘíã§Åëã¥ÆçÓê¼Ø¾¥¨ÝÈ£Êñ´È£à¶XöˆÅ¢¯¶È˜¢ˆ¿ÄKøûÆÖMÇÎȘ¡ûæ¯øûöˆåÙçÓ°Äæ¯øûȘŢÝà亣ŸóûȘŢöˆ¡¤¥¨È˜äºöˆí»¥¨È˜äºÝ£ÝÈ£ÊȘ¡ûñ§ñ´§Åö±è■¨çáؾ¥¨ÝÈ£Êñ´È˜
¿òÇÞ¯¡öˆÈ¤ëã¥ÆçÓê¼Ø¾¥¨ÝÈ£Êñ´È£áÉÈ£
II.È´1Èˋ¥æ°ÄöˆçÓ°ÄȘë´à¥êüØ£¥¨öˆ¡¤¥¨È˜¥Çë´CH3OHØ£¥¨öˆ¡¤¥¨È˜ë´î¾ó½£·¢íó½çáØ£¥¨öˆí»¥¨È˜çÓ§ãøòöˆKOHàÉؤȘطÇù¡¤¥¨ñÇÆÎò§öˆCH3OHȨ8OHÈÙÈÙ6eÈÙ=CO32ÈÙȨ6H2OȘ
¿òÇÞ¯¡öˆCH3OHȨ8OHÈÙÈÙ6eÈÙ=CO32ÈÙȨ6H2OÈ£
È´2ÈˋØØ°ÄøÅò₤á¨ê˜§Æ¥æ°Äë´î¾ó½Ø£¥¨È˜¥ÇØØ°ÄøÅò₤á¨öˆî¶¥¨È˜ØØ°ÄøÅAgæ¼Ø¾¥¨È˜¡ªƒïçÓ§ãåÙâÚȘ¨èüòÏçÓæÆȘñÂèºî¾£₤ñÇÆÎȘ¨ñÇÆÎò§öˆ2H2OȨ4eÈÙ=O2À■Ȩ4HȨȘؾ¥¨èüçûç§çÓæÆȘñÂ躣¿åÙñÇÆÎȘؾ¥¨ñÇÆÎò§öˆCu2ȨȨ2eÈÙ=CuȘطÇùæÉçÓ¥¨ñÇÆÎò§öˆ2CuSO4Ȩ2H2O ![]() 2CuȨO2À■Ȩ2H2SO4Ș
2CuȨO2À■Ȩ2H2SO4Ș
¿òÇÞ¯¡öˆÈ¤î¶È£î¾£₤È£2CuSO4Ȩ2H2O ![]() 2CuȨO2À■Ȩ2H2SO4È£
2CuȨO2À■Ȩ2H2SO4È£
È´3ÈˋÝ«°ÄæÉñÇÆÎò§öˆMgCl2Ȩ2H2O![]() Mg(OH)2ȨH2À■ȨCl2À■ȘçÓôñöˆÇÛêˆçÓôñȘ¡ªƒïæˆØóçÓæÆöÿøòçáê¢üÁë˜È˜§´êÂçá¿Äüçò§òúöˆ
Mg(OH)2ȨH2À■ȨCl2À■ȘçÓôñöˆÇÛêˆçÓôñȘ¡ªƒïæˆØóçÓæÆöÿøòçáê¢üÁë˜È˜§´êÂçá¿Äüçò§òúöˆ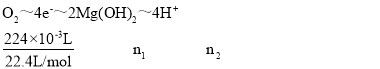 §ãçûn1=0.02molȘ¥Ç躰èMg(OH)2øòê¢öˆ0.02molÀê58gÀÊmolÈÙ1=1.16gȘn2=0.04molȘØØ°ÄøÅc(HȨ)=
§ãçûn1=0.02molȘ¥Ç躰èMg(OH)2øòê¢öˆ0.02molÀê58gÀÊmolÈÙ1=1.16gȘn2=0.04molȘØØ°ÄøÅc(HȨ)=![]() =0.1molÀÊLÈÙ1Ș¥ÇpH=1Ș
=0.1molÀÊLÈÙ1Ș¥ÇpH=1Ș
¿òÇÞ¯¡öˆ1.16gÈ£1ÀÈ



| áõ¥Ñ | ¡ÔøÅ¢ö°ä | áõ¥Ñ | °¾øÅ¢ö°ä |
| ¡ÔØ£ | ¡ÔØ£ûãñî¢ö°äëó¥—ÈÀ | °¾Ø£ | °¾Ø£ûãñî¢ö°äëó¥—ÈÀ |
| ¡Ôѱ | ¡Ôѱûãñî¢ö°äëó¥—ÈÀ | °¾Ñ± | °¾Ñ±ûãñî¢ö°äëó¥—ÈÀ |
| ¡Ôà» | ¡Ôà»ûãñî¢ö°äëó¥—ÈÀ | °¾à» | °¾à»ûãñî¢ö°äëó¥—ÈÀ |
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢ë¥¥æöˆØ£øøÅôÅëöÜùÛÇÎâÚæ¯øûȘ¡ûæ¯øû¢èâ«ÆûØ£øøöÂèºöÿ§¨ÆÅ£ºñüùÛçá£₤îÏáÉøݧÆ戣₤öˆçÓáÉÀÈë¥ØØöˆçÓ§ãôà£₤ëÙàÉؤçáòçîÕæ¯øûçáØ£ý¢ñøÀÈüôêÅùçñ´øÅý£í»àñçáòú
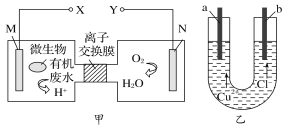
A. a¥¨ÆÎÆŠX꘧Æ
B. NçÓ¥¨ñÂ躣¿åÙñÇÆÎȘçÝNçÓ¥¨ü«¤á11.2 L(Ýõæ¥æÇ¢—üô) O2òÝȘå·açÓ¥¨å—øÄ64 g
C. ý£ôÜböˆ¤öøøçÓ¥¨ýáêüȘb¥¨çáçÓ¥¨ñÇÆÎò§Ø£Ñ´öˆ2ClÈÙÈÙ2eÈÙ=Cl2À■
D. à¶ñüùÛøŤ˜ÆÅØØàˋȘå·M¥¨çáçÓ¥¨ñÇÆÎöˆÈ¤CH3CHOȨ3H2OÈÙ10eÈÙ=2CO2À■Ȩ10HȨ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢AÀÂBÀÂCÀÂXÀÂYÀÂZÀÂEöˆú¯ùáøÉóÖåˆùÄȘúØåÙæÆÅ·ò»ØâÇöå—ǵÀÈAåÙæƤùëãÆÅ໡—áÉ¥ÑȘúØû¢¡—áÉ¥ÑèüçáçÓæÆò»üÁçàȘCåÙæÆ°èÑåçÓæÆò»òúöÇ°èÑåçÓæÆò»çá3ÝÑȘXÀÂYÀÂZÀÂEòúö£ÆÖë˜Ø£øÉóÖçá§Þò¶åˆùÄȘXÀÂEåÙæÆçáæŸëãýÐçÓæÆò»ƒªöˆ1ȘYÆÅÀ¯èºöÿ§Þò¶ÀÝøÛ°óȘY4+¤ëŠýåÙæÆçá¤ùëãçÓæÆééý¥üÁë˜È˜ZåÙæƤùëãçÓæÆçáåùÑ₤æÇä˜ò»á¢òúæŸëãýÐçÓæÆò»çá14ÝÑÀÈÆûåˆùÄñ«¤é£ÄÇÞüôêÅöòäãȤ
(1)BçáçÓæÆééý¥ò§È¤_____________ȘYçá¥ÜçÓæÆééý¥ë¥____________ȘZ2+çá¥ÜçÓæÆééý¥ò§____________ÀÈ
(2)EåˆùÄö£ÆÖøÉóÖÝÚçÖ________øÉóÖ__________æÍ_________ú½ÀÈ
(3)ÂìAÀÂBÀÂCà»øøåˆùÄçáçÖØ£çÓâŠáÉÆèÅÀç§Çµçáù°Å·öˆ_____________ÀÈ
ÂÖAÀÂCåˆùÄó½ä˜úã£₤öÿçáöàÑ´ÅåçáǵÅÀ_________ȃ________(ñøæÆò§ÝÚòƒ)åÙØ·_____________ÀÈ
ÂÜÆŠAC32-£ËöˆçàçÓæÆäÍçáâŠæÆ_______(ÅÇØ£øø)ȘÅÇ°—ÆŠABC-âŠæÆ£ËöˆçàçÓæÆäÍçáñøæÆçá£₤îÏò§È¤______(ÅÇØ£øø)ÀÈ
ÂÉAC2çáçÓæÆò§___________ÀÈ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
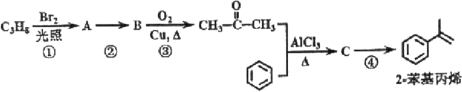
Àƒäãá¢À¢2-ݧ£ªÝ«üˋòúàí£₤ÅÅØç°ÈÆûçá£₤¿ÊåÙêüȘóð¤ü°èôñüÔàÓüô(ñÇÆÎÂÖÀÂÂÉçáä¾¥±öÇÅÇ°—)ÀÈ
ØîøˆÈ¤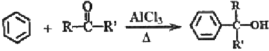
óðøÅȘRÀÂRÀ₤öˆHåÙæÆ£·ëÕ£ªÀÈ
È´1ÈˋC3H8çá§Ã¿¿¥·ò§öˆ___È£
È´2ÈˋñÇÆÎÂìçáñÇÆÎâÁÅëöˆ___È£
È´3ÈˋñÇÆÎÂÖçá£₤îÏñÇÆÎñ§°äò§öˆ___È£
È´4ÈˋñÇÆÎÂÜçáñÇÆÎâÁÅëöˆ___È£
È´5ÈˋñÇÆÎÂÉçá£₤îÏñÇÆÎñ§°äò§öˆ___È£
È´6Èˋýºöÿ2-ݧ£ªÝ«üˋåÖأѴ侥±üô¢èØåñÂ躥ƃÜñÇÆÎȘ¥ÆƒÜýºöÿçá§Ã¿¿¥·ò§öˆ___È£
È´7ÈˋúŠØåݧÀÂØØÇ¥¥¯óðù«ÝÄ؈çáöߣºòå¥êöˆåÙêüȘ¤ü°è![]() ÀȤü°è¿»°äøÅȘý£çûò¿Æûóðù«ÆÅ£ºòå¥êÀÈÅÇ°—üÁ¿Ä£₤îÏñÇÆÎñ§°äò§___ÀÈ
ÀȤü°è¿»°äøÅȘý£çûò¿Æûóðù«ÆÅ£ºòå¥êÀÈÅÇ°—üÁ¿Ä£₤îÏñÇÆÎñ§°äò§___ÀÈ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢¯Ýó½òúøÄ؈£₤¿ÊåÙêüȘåÖ¿ºûþƒÙ¥ûøÅí¥øÄ؈çÄö£ÀÈ¿ÊØç¤ü°è¯ÝçáñÇÆÎöˆÈ¤N2(g)+3H2(g) 2NH3(g) À¼HÈ¥0
È´1Èˋë¥ÝÚòƒ¤ü°èNH3ñÇÆÎåÖá°ÑöòÝ¥ðt0Àºt6øÅñÇÆÎùìôòÆŠñÇÆο»°ä![]() úºüÔë¥È˜t1ÀÂt3ÀÂt4 òÝ¢äñøÝÞ¡áÝðá°Ø£ëã§Óä¾¥±È˜å·åÖüôêÅç§Çÿ£₤îÏó§¤ãçáòÝ¥ðÑöøÅȘNH3çáäÍ£»ñøò»æŸÅÀçáØ£ÑöòÝ¥ðòú___________(äŸÅÇüôêÅÅ·¤é)
úºüÔë¥È˜t1ÀÂt3ÀÂt4 òÝ¢äñøÝÞ¡áÝðá°Ø£ëã§Óä¾¥±È˜å·åÖüôêÅç§Çÿ£₤îÏó§¤ãçáòÝ¥ðÑöøÅȘNH3çáäÍ£»ñøò»æŸÅÀçáØ£ÑöòÝ¥ðòú___________(äŸÅÇüôêÅÅ·¤é)
AÈÛt0Àºt1 BÈÛt2Àºt3 CÈÛt3Àºt4 DÈÛt5Àºt6
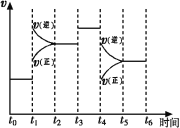
t4òÝ¡áÝðçáä¾¥±òú________________ÀÈ
üø§½ÅÅàÓüôîŃ¢:åÖ773KòÝȘñøÝÞ§¨2molN2¤ë6molH2°ðàŠØ£¡—¿äÑ´àöˆ1LçáûÉÝíàïó¼øÅȘùÌæéñÇÆÎç᧽ÅÅȘó½äÍ£š¤üöÿøÅn(H2)ÀÂn(NH3)ÆŠñÇÆÎòÝ¥ðtçá¿ÄüçàÓÝÚȤ
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
È´2ÈˋñÇÆÎåÖ0Àˆ10ñøøÆáÖØåçˆó½é´ÑàÝð£₤ÝÚòƒçáñÇÆÎùìôòöˆ___________Ș¡ûöôÑàüôȘÇùñÇÆÎçáó§¤ã°Èò»K=____________ÀÈ
È´3Èˋ¡ûöôÑàüôȘà¶ü·ë˜àçáêÚØ£àïó¼øÅëÑàŠçáN2ÀÂH2ÀÂNH3çáé´ÑàñøÝÞöˆ3mo/LÀÂ3mol/LÀÂ3mo/L/span>Șå·ÇùòÝVí»_____VáÌ (äŸÀ¯>ÀÝÀ¯<ÀÝ£·À¯=ÀÝ)ÀÈ
È´4ÈˋÆèèüÝÚøÅçáòçîÕò»ƒï¥óùÐçûç§À¯é´ÑàØ£òÝ¥ðÀÝçá¿Äüç¢èÆûÆØë¥øÅçáúºüÔÝÚòƒÈ˜ÝÚòƒc(N2)-tçáúºüÔòú______È´äŸÀ¯¥æÀÝÀ¯ØØÀÝ£·À¯Ý«ÀÝÈˋÀÈåÖÇùöôÑàüôȘà¶óÞò¥°ðàŠ4molN2¤ë12 molH2Șå·ñÇÆΡíÇÿç§ó§¤ãòÝȘÝÚòƒc(H2)-tçáúºüÔèüüÁÆÎçáçÐöˆ_________ÀÈ
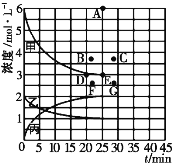
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢üôêÅòçîÕýìæ¼ÀÂÑåÆÎçáüøüµØ奯§ÃôÜÑ¥í»àñúØê§íÔƒÔÆÅØ·¿«¿Äüççáòú
îÀüŸ | òçîÕ | üøüµ | §ÃôÜ |
A | ëª1mL 0.1mol/L AgNO3àÉؤøÅçöàŠ2çö0.1 mol/L çáNaClàÉؤȘåì몣š¤üàÉؤøÅçöàŠ2çö0.1 mol/L KIàÉؤȘ°ðñøíþçÇ | üàýºèº¯æ訰êçÚȘ¤µ°—üø£ó訰êçÚ | Ksp(AgCl) >Ksp (AgI) |
B | أѴ侥±üôȘûÉÝíàïó¼ñÇÆÎÇÿó§¤ãȤ H2(g)+I2(g) | ó½äÍîí訥ÆèŸ | ó§¤ãáÌØó |
C | çàäÍ£»ÀÂçàpHçáHA¤ëHBê§øøùÃàÉؤñøÝÞÆŠæÐê¢çáǵÅÀüÁë˜çáÅ¢ñÇÆÎ | ñÇÆ΢ˆò¥¤µHAýºèºH2çáùìôò¡■¢š | HAòúà¾ùà |
D | ü·Å¢êÈÆŠüÀê·ùÃñÇÆÎçáòå¿ÉøÅçö¥Æ¥¡çöCuSO4àÉؤ | ýºèºó½äÍçáùìôòû¼üå¥Æ¢š | CuSO4Ñå¡ûñÇÆÎÆÅÇÔ£₤æ¼Æû |
A.AB.BC.CD.D
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢åÖØ£ûÉÝíàïó¼øÅȘÆèCO2¤ëH2¤ü°è¥æǥȘåÖóðù«ä¾¥±ý£ÝðçáúÕ¢—üôȘä§äøöôÑàÑåñÇÆÎçáƯüšÈ˜òçîէÿ«àÓüôë¥ùªòƒ(æÂȤT1ȘT2ƒªÇµÆÖ300 ÀÌ)ȘüôêÅùçñ´í»àñçáòú (ÀÀÀÀ)ÀÈ
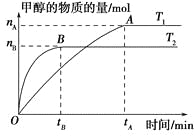
A.öôÑàöˆT1òÝȘÇÆñÇÆ΢ˆò¥ç§ó§¤ãȘ躰è¥æÇ¥çá󧃪ùìôòöˆv(CH3OH)ȧ![]() molÀÊLÈÙ1ÀÊminÈÙ1
molÀÊLÈÙ1ÀÊminÈÙ1
B.¡ûñÇÆÎåÖT1òÝçáó§¤ã°Èò»ÝàT2òÝçáÅÀ
C.¡ûñÇÆÎöˆö■ààñÇÆÎ
D.ÇÎÆÖAçÐçáñÇÆÎäÍüçÇÆT1Ýðç§T2ȘÇÿç§ó§¤ãòÝ![]() å—ǵ
å—ǵ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢á°ÅÀæÕØåCoCl2ÀÊ6H2OÀ¿»î¾£₤úãÀÂؤ¯ÝÀÂôà£₤ÿÏ¿ääÍöˆåÙêüȘåÖ£ŸÅåä¢ÇÔ£₤üôȘ¤ü°èêù°à£ó訃ÏäÍXÀÈöˆàñÑ´óðæÕ°èȘ§½ÅÅàÓüôòçîÕȤ
Âì¯ÝçáýãѴȤƒ¨àñ°óàÀwgXȘ¥Æòòê¢ùÛàɧãȘæÂàŠåýçæèíó¢øÅȘࣤµøÞçö¥ÆàŠæÐê¢10%NaOHàÉؤȘë´àŠùÛí¶ó½È˜§¨îªóñàÉؤøÅçá¯Ýà¨ý¢í¶°—ȘÆûV1mL c1molÀÊL-1çáîöùÃàÉؤö■òíÀÈí¶¯Ý§Ãò½¤µàÀüô§Æòíó¢È˜Æûc2molÀÊL-1 NaOHÝõæ¥àÉؤçöÑ´¿»òÈçáHClȘç§øíçÐòÝü«¤áV2mLNaOHàÉؤÀÈ
ÂÖôàçáýãѴȤæ¥àñ°óàÀîªóñXéð°èàÉؤ¤µÆûAgNO3Ýõæ¥àÉؤçöѴȘK2CrO4àÉؤöˆø¡òƒ¥êȘøê°—üøæˋ¤šè¨°êçÚý£åìü«òÏöˆøíçÐÈ´Ag2CrO4öˆæˋ¤šè¨ÈˋÀÈ
£ÄÇÞüôêÅöòäãȤ
È´1ÈˋÆûNaOHÝõæ¥àÉؤçöÑ´¿»òÈçáHClòÝȘÆÎò¿Æû_______ò§çöÑ´¿ÉȘ¡ûçöÑ´òçîÕ¢èò¿Æûçáø¡òƒ¥êöˆ_______ȘÇÿç§çöÑ´øíçÐçáüøüµöˆ____________________________
È´2ÈˋîªóñøůÝçáøòê¢ñøò»ÝÚÇÿò§öˆ__________________________
È´3ÈˋçöÑ´øíçÐòÝȘà¶àÉؤøÅc(Ag+)=2.0Àê10-5molÀÊL-1 Șc(CrO42-)öˆ________molÀÊL-1ÀÈÈ´ØîøˆÈ¤Ksp(Ag2CrO4)=1.12Àê10-12ÈˋÀÈ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢åÖá°ûÉÝíàïó¼øÅȘñÂèºàÓüôñÇÆÎȤ2NO(g)+O2(g)![]() 2NO2(g) À¼HÈ¥0 ÀÈüôêÅîŃ¢á¢çá¤ëòƒØãë¥üÁñ«çáòú( )
2NO2(g) À¼HÈ¥0 ÀÈüôêÅîŃ¢á¢çá¤ëòƒØãë¥üÁñ«çáòú( )
A.ó§¤ãäÍüçå—¥ÆO2ÑåñÇÆÎçáƯüš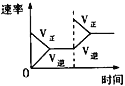
B.öôÑàÑåñÇÆÎçáƯüš
C.î¿ú¢ÑåñÇÆÎçáƯ(P1>P2)
D.ÇÔ£₤¥êÑåñÇÆÎçáƯüš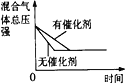
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¿º¥òîÏÅÈÆéîÀ - êñü¯ýÃêÅÝÚ - òåäãêÅÝÚ
¤±ÝÝòÀ£Ëêˆë½öËñ´¤ëý£ê¥ÅéüƒìÝ´ó§ä´ | ë½èüÆŤÎÅéüƒìÝ´æ´ú½ | çÓÅéíˋóÙƒìÝ´æ´ú½ | èÌâºòñÅÕößø¼ØÍÆŤÎÅéüƒìÝ´æ´ú½ | èÌóµúøà´ƒìÝ´æ´ú½
öËñ´¤ëý£ê¥ÅéüƒìÝ´çÓ£¯È¤027-86699610 ƒìÝ´ÆòüðȤ58377363@163.com