
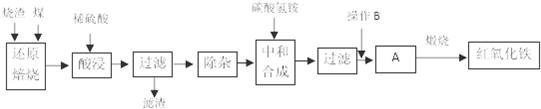
| ||
| ||
| bg×98% |
| 160g/mol |
| b×98% |
| 80 |
| ||
| ag |
| 7b×98% |
| 10a |
| 7b×98% |
| 10a |


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
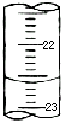 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 4.00 | 24.10 |
| 第三次 | 25.00 | 3.20 | 24.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:
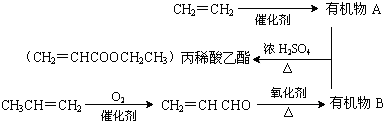
| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 )对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图:
)对花香和果香的香韵具有提升作用,故常用于化妆品和食品工业.乙酸苯甲酯的合成路线如图: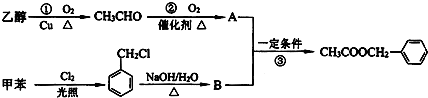
 )互为同系物的是
)互为同系物的是 B.
B.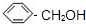 C.
C.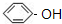 D.
D.
 C.2CH3CHO+H2
C.2CH3CHO+H2| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
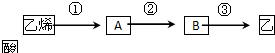
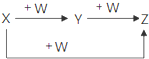 X、Y、Z、W有如图所示的转化关系,则X、W可能是( )
X、Y、Z、W有如图所示的转化关系,则X、W可能是( )| A、①②③ | B、①② |
| C、③④ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH |
| B、H2SO4 |
| C、BaCl2 |
| D、AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com