
【题目】已知:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素。其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;G原子核外最外层电子数与B相同,其余各层均充满。B、E两元素组成化合物B2E的晶体为离子晶体。C、F的原子均有三个能层,C原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;C与F能形成原子数目比为1:3、熔点为190℃的化合物Q。
(1)B的单质晶体为体心立方堆积模型,其配位数为 ;E元素的最高价氧化物分子的立体构型是 。F元素原子的核外电子排布式是 ,F的高价离子与A的简单氢化物形成的配离子的化学式为 .
(2)试比较B、D分别与F形成的化合物的熔点高低并说明理由 。
(3)A、G形成某种化合物的晶胞结构如图所示 。若阿伏伽德罗常数为NA,该化合物晶体的密度为 a g/cm3,其晶胞的边长为 cm。
。若阿伏伽德罗常数为NA,该化合物晶体的密度为 a g/cm3,其晶胞的边长为 cm。
(4)在1.0l×105Pa、t1℃时,气体摩尔体积为53.4 L/mol,实验测得Q的气态密度为5.00g/L,则此时Q的组成为(写化学式) 。
【答案】(共14分)(1)8(2分) 平面三角形(2分) 1s22s22p63s23p5(2分) [Cu(NH3)4]2+(2分)
(2)NaCl的熔点高于SiCl4,因为NaCl是离子晶体,SiCl4是分子晶体。(2分)
(3)![]() (2分) (4)Al2Cl6(2分)
(2分) (4)Al2Cl6(2分)
【解析】试题分析:A、B、C、D、E、F、G七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素。其中A原子在基态时p轨道半充满且电负性是同族元素中最大的,因此A是N。D、E原子核外的M层中均有两个未成对电子,则D的M层为3s23p2,是Si。E的M层为3s2 3p4,是S。B、E两元素组成化合物B2E的晶体为离子晶体,所以B为IA族的金属,B应该是钠元素。G原子核外最外层电子数与B相同,其余各层均充满,且G的原子序数最大,因此G是铜。C、F的原子均有三个能层,因此C、F在第三周期。C的逐级电离能前三个数据接近,第四电离能突变,所以易失去三个电子,为第ⅢA族元素,C是铝。C与F能形成原子数目比为1:3、熔点为190℃的化合物Q ,说明F为-1价,即F为Cl元素,Q是AlCl3。
(1)金属钠的单质晶体为体心立方堆积模型,其配位数为8;E元素的最高价氧化物分子是三氧化硫,其中心原子S原子含有的孤对电子对数=(6-3×2)÷2=0,所以三氧化硫分子的立体构型是平面三角形。根据构造原理可知,Cl元素原子的核外电子排布式是1s22s22p63s23p5;G的高价离子Cu2+与A的简单氢化物NH3形成的配离子的化学式为[Cu(NH3)4]2+。
(2)B、D分别与F形成的化合物分别是氯化钠和四氯化硅。因为NaCl是离子晶体,SiCl4是分子晶体,所以NaCl的熔点高于SiCl4。
(3)根据晶胞的结构可知,N原子在顶点,含有的个数=8×![]() =1个。铜在棱边,含有的个数=12×
=1个。铜在棱边,含有的个数=12×![]() =3个,即化学式为Cu3N。设边长为x cm,则
=3个,即化学式为Cu3N。设边长为x cm,则![]() ×NA=1,解得x=
×NA=1,解得x=![]() 。
。
(4)根据M=ρ×Vm=5.00g/L×53.4L/mol=267,是AlCl3相对分子质量的267÷133.5=2倍,所以其化学式为Al2Cl6。


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】KI+5KIO3+3H2S=3I2+3K2SO4+3H2O,下列说法正确的是
A. 还原产物只有12,氧化产物只有K2SO4 B. 氧化剂和还原剂物质的量之比为5:4
C. 3molH2S可还原5mol的KIO3 D. 2.5molKIO3发生反应,转移25NA个e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25℃、101 kPa)的气体摩尔体积,请回答以下问题。该小组设计的简易实验装置如图所示:

该实验的主要操作步骤如下:
(1)配制80 mL 1.0 mol·L-1的硫酸溶液:
①通过计算,需用量筒量取18mol/L的浓硫酸的体积为__________mL。
②在配置稀硫酸的过程中,所需要的实验仪器有:烧杯、量筒、玻璃棒、__________、________。
③下列操作能造成所配溶液的物质的量浓度偏大的是________。
A.转移溶液时不慎有少量液体洒在容量瓶外面
B.转移前,容量瓶中有少量蒸馏水
C.定容时,眼睛俯视刻度线
D.定容后,上下摇匀后液面下降,补充少量水
(2)用量筒量取25.0mL 1.0 mol·L-1的硫酸溶液加入锥形瓶中;并称取a g己除去表面氧化膜的镁条,并系于铜丝末端,为使H2SO4全部参加反应,a的数值至少为__________;
(3)往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;反应结束后待体系温度恢复到室温,读出量筒中水的体积为VmL。读数时除恢复至室温外,还要注意:___________________,且该步骤应选用______________(填序号)的量筒。
A.100mL B.200 mL C.500 mL D.1000mL
(4)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm=____________(用V表示),若未除去镁条表面的氧化膜,则测量结果____________。(题“偏大”、“ 偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列俗名和化学式不吻合的是
A. 明矾 KAl(SO4)2·12H2O B. 重晶石 BaSO4
C. 熟石膏 2CaSO4·H2O D. 绿矾 CuSO4·5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠跟足量的NaHCO3混合后,在密闭容器中充分加热,排除气体物质后冷却残留的固体物质是
A. Na2O2、Na2CO3 B. NaOH、Na2CO3
C. Na2CO3 D. Na2O2、NaOH、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. 用白磷作包装食品的脱氧剂 B. 食品保鲜膜能减缓食品中水分的蒸发
C. 用液氨作制冷剂冷藏物品 D. 用臭氧对医疗器械进行消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是()
A. 用广范pH试纸测得某溶液的pH为0
B. 可用铁粉鉴别浓硫酸和稀硫酸
C. 蒸馏是分离液态混合物的一种常用方法,广泛应用于石油工业
D. 品红溶液可用于鉴别SO2和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜的配合物A(结构如图)。请回答下列问题:
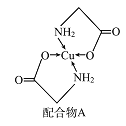


(1)Cu的简化电子排布式为______________ 。
(2)A所含三种元素C、N、O的第一电离能由大到小的顺序为_______________。其中氮原子的杂化轨道类型为________。
(3)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目之比
是__________;N2O与CO2互为等电子体,且N2O分子中O只与一个N相连,则N2O的电子式为_______。
(4)在Cu催化下,甲醇可被氧化为甲醛(HCHO),甲醛分子中H CO的键角___________(选填“大于”、“等于”或“小于”)120°;甲醛能与水形成氢键,请在右图中表示出来___________。
(5)立方氮化硼(如图)与金刚石结构相似,是超硬材料。立方氮化硼晶体内B-N键数与硼原子数之比为___________;结构化学上用原子坐标参数表示晶胞内部各原子的相对位置,上图(右)立方氮化硼的晶胞中,B原子的坐标参数分别有:
![]() 等。则距离上述三个B原子最近且等距的N原子的坐标参数为____________________ 。
等。则距离上述三个B原子最近且等距的N原子的坐标参数为____________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com