
����Ŀ����Ԫ�������Ԫ�ؾ������������γɻ����������ܶࡣ
(1)����������Ԫ�صĵ�һ�����ܴӴ�С��˳��Ϊ__________����Ԫ�����Ԫ�����γ�OF2���ӣ��÷��ӵĿռ乹��Ϊ__________��
(2)���ݵȵ�����ԭ������NO�е�ԭ�ӹ���ӻ�������__________��1 mol O![]() �к��еĦм���ĿΪ__________����
�к��еĦм���ĿΪ__________����
(3)��Ԫ�غ���Ԫ�ؿ��γɶ��ּ�̬�Ľ�����������������Cr2O3��CrO3��CrO5�ȡ�Cr3����̬��������Ų�ʽΪ__________��
(4)�������ʵķ�����O3���ӵĽṹ�����Ƶ���__________��
A��H2O�� B��CO2������ C��SO2������ D��BeCl2
(5)O3�����Ƿ�Ϊ���Է��ӣ�__________��
���𰸡� F>N>O V�� sp 2NA 1s22s22p63s23p63d3 C ��
����������1���ɺ��ع����������֪����Ԫ�صĵ�һ�����ܴ�����Ԫ�أ�С�ڷ�Ԫ�أ��ɼ۲���ӶԻ������ۿ�֪��OF2����������ԭ�ӵļ۲���Ӷ�����4������2�Թ¶Ե��ӣ���ռ乹����V�Ρ���2�����ݵȵ�����ԭ����NO2����CO2��Ϊ�ȵ����壬���ߵĽṹ���ƣ�NO2���е�ԭ�ӵ��ӻ���ʽ��CO2��̼ԭ�ӵ��ӻ���ʽ��ͬ������sp�ӻ���O22����N2(������һ����������������)��Ϊ�ȵ����壬���1molO22������2NA����������3��Cr��ԭ��������24��Cr3����̬��������Ų�ʽΪ1s22s22p63s23p63d3����4��SO2��O3��Ϊ�ȵ����壬���ݼ۲���ӶԻ������۷�����SO2��O3���ӵĽṹ�����ƣ���ѡC����5��SO2��O3��Ϊ�ȵ����壬�ṹ���ƣ����������Ǽ��Է��ӣ�����Ҳ�Ǽ��Է��ӡ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ������ʵ��������������ԭ�����͵��� �� ��
A���ϳɰ���ҵ������ѹǿ����߷�Ӧ���ת����
B������ɫ����ˮ���պ���ɫ��dz
C����H2��I2������HI��ɵ�ƽ����ϵ��ѹ����ɫ����
D���ں���Fe��SCN��2���ĺ�ɫ��Һ�м����ۣ����ã���Һ��ɫ��dz����ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����нṹͼ�У������ǰ������Ԫ�ص�ԭ��ʵ��ԭ��ʵ��ԭ�ӳ�ȥ�������Ӻ�ʣ��IJ��֣���С�ڵ����δ�����γɹ��ۼ����������ӣ����ߴ����ۼ���ʾ������ͼ��F2�����ݸ�ͼ��ʾ�Ľṹ�ص㣬�����й�������ȷ���ǣ�������

A. �����ṹͼ�й�����6��Ԫ�� B. �ס��ҡ���Ϊ�Ǽ��Է��ӣ���Ϊ���Է���
C. ���붡���Է������Ϸ�Ӧ�������ӻ����� D. ��CaCl2��Һ��ͨ����а�ɫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ļ�����������ʵ�飺

��1������X��������________________��
��2������A��___________���ѧʽ����
��3����ҺB�������ӳ�OH- ���__________�������ӷ��ţ�����ҺD�д��ڵĽ�������Ϊ_________�������ӷ��ţ���
��4����������NaOH��Һʱ������Ӧ�����ӷ���ʽΪ��_________������ϡ���ᷢ����Ӧ�����ӷ���ʽΪ��___________________________________________��
��5������ҺD����NaOH��Һ���۲쵽�����İ�ɫ��״����Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ����д������ת���Ļ�ѧ����ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ����Ҫ�İ뵼����ϡ���ҵ���þ��������Ҫ�ɷ�ΪGeS2�����ʲ���Ӧ����ȡGe���乤��������ͼ��ʾ��

�ش��������⣺
��1����ʼ�������������Ŀ����______��
��2�����±��վ������Ļ�ѧ����ʽΪ______��
��3���Ȼ�ԭ��ջӷ�¯�ڷ�Ӧ�Ļ�ѧ����ʽΪ______��
��4���ڳ�������У����¶�Ϊ90�棬pHΪ14ʱ����������CaCl2/Ge�����ȣ��Գ����Ӱ�������ʾ��ѡ����Ѽ�����Ϊ______���10-15����15-20����20-25������������______��
��� | ��������CaCl2/Ge�� | ĸҺ��� ��mL�� | ���˺�Һ���ࣨmg/L�� | ���˺�Һ pH | ������ʣ�%�� |
1 | 10 | 500 | 76 | 8 | 93.67 |
2 | 15 | 500 | 20 | 8 | 98.15 |
3 | 20 | 500 | 2 | 11 | 99.78 |
4 | 25 | 500 | 1.5 | 12 | 99.85 |
��5��ij�¶�ʱ������õ���CaGeO3��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵���������______��

a��n����p���Ӧ��Ksp���
b��ͨ����������ʹ��Һ��q��䵽p��
c��q����CaGeO3��������
d������Na2GeO3����ʹ��Һ��n��䵽m��
��6��CaGeO3��ǿ�ᷴӦ�ɵõ�H2GeO3��0.l molL��1��NaHGeO3��ҺpH_____���������=��������7���ж�������______��ͨ������Ƚϣ�����25��ʱ��H2GeO3��Ka1=1.7��10��9��Ka2=1.9��10��13����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܵĻ������ڴ��Բ���������������졢�����Ʊ��ȷ���Ӧ��ʮ�ֹ㷺��
��1�����������ӵĺ�������Ų�ʽΪ______����̬Coԭ�Ӻ���3d�ܼ�����______��δ�ɶԵ��ӡ�Co��Ca��ͬ���ڣ��Һ����������ӹ�����ͬ�����������۷е㶼�ȸƸߣ�ԭ����______��
��2��0.1mol[Co(NO2)6]3���������ĦҼ���Ŀ��______��K3[Co(NO2)6]��K��N��O����Ԫ�صĵ�һ�������ɴ�С��˳����______��
��3���������İ�����̪ݼ���ӵĽṹʽ��ͼ���İ�����̪ݼ��Nԭ�ӵ��ӻ��������Ϊ______��
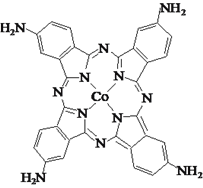
��4��[Co(NH3)6]Cl3�������CoCl2���ڰ�ˮ��ͨ������Ƶã����������������ӵ����幹����______��
��5��һ���ܵĻ����������ʯ������Ĵ������侧���ṹ��ͼ��ʾ����������ÿ��O2�����ڵ�O2����______�������ܵĻ�����Ļ�ѧʽ��______��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˫�ŷ�����ʾ����������ԭ��Ӧ�е���ת�Ƶķ������Ŀ����ָ���������ͻ�ԭ����2KClO3 === 2KCl+3O2�� _______������_____����ԭ��_____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڳ�����pH=1��������Һ���й�������
�ٸ���Һ1mLϡ����100mL��pH=3
�������Һ�м���������pH=13������������Һǡ����ȫ�к�
�۸���Һ������������c(H+)��ˮ�������c(H+)֮��ֵΪ1��10��12
�������Һ�м�����������Ũ�ȵİ�ˮ��������ҺpH=7
������ȷ����
A. �٢� B. �٢� C. �ڢ� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᣨHCOOH����һ�ֿ������Ĵ������ʣ�������������Ӧ��H2��ѭ��ʾ��ͼ���¡�

��1��HCOOH�Ľṹʽ��________��
��2������H2����ͼ�й������H2�Ļ�ѧ����ʽ��________��
��3������H2��
��CO2���ⷨ��
����֪��2HCOOH (l) �� O2 (g) �� 2CO2 (g) �� 2H2O (l) ��H ����510 kJ��mol1
2H2 (g) �� O2 (g) �� 2H2O (l) ��H ����572 kJ��mol1
��CO2 (g) �� H2 (g) �� HCOOH (l) ��H ��________��
�˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K��________��
������ѹǿ��CO2��ƽ��ת�������ߣ�ԭ����________��
��ʹ�ڸ�ѹ���������£�CO2��ƽ��ת����Ҳ���ߣ�Ϊʵ��CO2���������ĸ�Чת�������Բ�ȡ�Ĵ�ʩ��________��
�绯ѧ��ԭ����
��̼�����ε�ˮ��Һ�У�CO2��ԭ�ɼ����ԭ����ͼ1��ʾ��

![]()

![]()
��ͼ1�У������ĵ缫��Ӧʽ��________��
������ͼ1����ͼ2�ķ����������Ӧ���ʵĻ�ѧʽ�����ӷ���_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com