
【题目】金属镍硬而有延展性并具有铁磁性,能够高度磨光和抗腐蚀。下图是一种以含镍废料(主要是NiO,含少量FeO、SiO2等杂质)制备Ni的流程:

已知:室温下难溶物的溶度积数据如下表:
化合物 | Ni(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-15 | 10-15 | 10-38 |
(1)滤渣1的主要成分为_____________(填化学式)。
(2)实验中需用0.8mol/L的稀硫酸800mL,若用98%的浓硫酸(ρ=1.84g·mL-l)来配制,量取浓硫酸
时,需使用的量筒的规格为_________(填序号)。
A.10mL B.20mL C.50mL D.l00tnL
(3)用离子方程式解释加入H2O2的作用:_________________。
(4)滴加氨水调节至pH为_________时,铁刚好沉淀完全;若继续滴加氨水至pH为_____________时,镍开始沉淀(假定Ni2+浓度为0.lmol/L)。若上述过程中没有“氧化”步骤,其后果是_______________。
(5)电解制备镍的反应原理如图所示,则A电极的反应式为2H++2e-=H2↑和___________________。

(6)若用a kg含镍废料(含NiO 80%)制备Ni,最终得到产品b kg,则产率为_____________。
【答案】 SiO2 C 2Fe2++H2O2+2H+=2Fe3++2H2O 3 7 Ni2+和Fe2+分离不开 Ni2++2e=Ni ![]()
【解析】本题考查化学工艺流程,(1)NiO和FeO都是碱性氧化物,SiO2属于酸性氧化物,SiO2不与稀硫酸反应,因此滤渣1的成分是SiO2;(2)实验室没有800mL的容量瓶,应用1000mL的容量瓶,根据稀释前后溶质物质的量或质量不变,因此有1000×10-3×0.8=V(H2SO4)×1.84×98%/98,解得V(H2SO4)=43mL,因此选用大而接近的量筒,即选用50mL的量筒,故选项C正确;(3)酸溶后溶液中含有金属阳离子是Ni2+和Fe2+,Fe2+具有还原性,因此加入H2O2的目的是氧化Fe2+,便于除去铁元素,与H2O2发生的离子反应方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O;(4)铁元素刚好沉淀完全,此时溶液的c(Fe3+)=10-5mol·L-1,根据Ksp=c(Fe3+)×c3(OH-),代入数值,解得c(OH-)=10-11mol·L-1,则c(H+)=10-3mol·L-1,即pH=3,镍元素开始出现沉淀,依据Ksp=c(Ni2+)×c2(OH-),代入数值,c(OH-)=10-7mol·L-1,则c(H+)=10-7mol·L-1,即pH=7;如果没有氧化步骤,Fe2+开始出现沉淀,Ksp=c(Fe2+)×c2(OH-),代入数值,c(OH-)=10-7mol·L-1,则c(H+)=10-7mol·L-1,即pH=7,其结果是. Ni2+和Fe2+分离不开;(5)根据A电极反应式,推出A电极为阴极,根据电解原理,制备金属镍,因此A电极反应式为2H++2e-=H2↑,Ni2++2e-=Ni;(6)理论上产生Ni的质量为a×103×80%×59/75g,合a×80%×59/75kg,产率为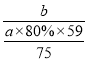 ×100%=
×100%=![]() 。
。


科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离产生的H+的浓度为1×10-5moL/L,则该溶液中的溶质可能是下列物质中的( )
A. HCl B. NaHSO4 C. Na2CO3 D. NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种烃①2-甲基丁烷 ②2,2-二甲基丙烷 ③戊烷 ④丙烷 ⑤丁烷,按沸点由高到低的顺序排列的是( )
A.①>②>③>④>⑤B.②>③>⑤>④>①
C.④>⑤>②>①>③D.③>①>②>⑤>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阴离子Xn﹣含中子N个,X的质量数为A,则ag X的氢化物中含质子的物质的量是( )
A.![]() (N﹣a)mol
(N﹣a)mol
B.![]() (n+A)mol
(n+A)mol
C.![]() (N+n)mol
(N+n)mol
D.![]() (A﹣N+n)mol
(A﹣N+n)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体是一种淡黄色粉末,常用于照相显影剂及制药工业,也是电池材料的制备原料。某化学兴趣小组对草酸亚铁晶体的一些性质进行探究。
(1)甲组同学用如图所示装置测定草酸亚铁晶体(FeC2O4·xH2O)中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为ag。将样品装入石英玻璃管中,再次将装置称重,记为b g。按图连接好装置进行实验。

a.打开K1和K2,缓缓通入N2; b.点燃酒精灯加热; c.熄灭酒精灯;d.冷却至室温;e.关闭K1和K2; f.称重A;g.重复上述操作,直至A恒重,记为cg。
①仪器B的名称是__________ ,通入N2的目的是___________。
②根据实验记录,计算草酸亚铁晶体化学式中的x =____________(列式表示);若实验时a、b次序对调,会使x值______________ (填“偏大” “无影响”或“偏小”)。
(2)乙组同学为探究草酸亚铁的分解产物,将(1)中已恒重的装置A接入图14所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后装置A中残留固体为黑色粉末。

①装置C、G中的澄清石灰水均变浑浊,说明分解产物中有____________(填化学式)。
②装置F中盛放的物质是___________(填化学式)。
③将装置A中的残留固体溶于稀盐酸,无气泡,滴入KSCN溶液无血红色,说明分解产物中A的化学式为________。
④写出草酸亚铁(FeC2O4)分解的化学方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素类药物的作用是抑制凝血因子在肝脏的合成。图是香豆素的一种合成路线:

已知:
(1)A→B的反应类型为______________。
(2)C的化学名称为_______________。
(3)完成下列化学方程式:
①D在一定条件下发生加聚反应:_______________;
② E→香豆素:_________________。
(4)C有多种同分异构体,其中含苯环的共有___________种(不考虑立体异构),这些同分异构体在下列仪器中显示的信(或收据)完全相同,该仪器是____________(填序号)。
A.质谱仪 B.红外光谱仪C.元素分析仪 D.核磁共振仪
(5)已知:同一个碳上连有两个羟基通常不稳定,易脱水形成羰基。以甲苯为取料(其他无机试剂任选) 制备化合物C (目标化合物),请在横线上将合成路线的后半部分补充完整。

____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在有机物的分子中引入羟基官能团的反应类型有:(a)酯化反应(b)取代反应(c)消去反应(d)加成反应(e)水解反应。其中正确的组合有( )
A.(b)(d)(e)B.(d)(e)C.(a)(b)(c)D.(b)(c)(d)(e)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com