
【题目】某校环保兴趣小组在处理污水样品时,需将质量分数为37%的浓盐酸(密度为1.19gcm﹣3)配制成250mL0.1molL﹣1的盐酸溶液。
(1)在如图所示仪器中,配制上述溶液不需要的是______(填图中相应仪器的字母)。除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_______,其作用按使用的先后顺序分别是_______和_______。

(2)根据计算,下列量程或规格中,本实验量筒应使用的是______;容量瓶应使用______(填写相应的序号)。
A.10mL B.100mL C.250mL D.500mL
(3)在量取浓盐酸后,下列操作的先后顺序是______(用编号表示)。
①待稀释的盐酸温度与室温一致后,沿玻璃棒注入所选定规格的容量瓶中
②往容量瓶中小心加蒸馏水至液面接近环形刻度线1cm~2cm处,改用胶头滴管加蒸馏水,使凹液面最低处与瓶颈的环形刻度线相切
③在盛盐酸的烧杯中注入适量蒸馏水,并用玻璃棒搅拌,使其混合均匀
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶
(4)关于容量瓶的使用,下列操作正确的是______(填字母,下同)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1cm~2cm处,改用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1cm~2cm处,改用胶头滴管加蒸馏水至刻度线
E。盖好瓶盖,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(5)若定容后摇匀静置,发现凹液面低于线,此时应该______。
A.直接转移到细口试剂瓶中
B.再用胶头滴管加水,重新定容
C.将此溶液倒掉,重新配制
D.直接储存于容量瓶中
(6)假设配制时其他操作均正确,只出现以下某一情况,试判断所配制的溶液浓度相比于要求的值(即0.1molL﹣1)如何变化。(a.偏高;b.偏低;c.无影响,在下列横线上填相应的字母)。
①容量瓶中有少量蒸馏水______。
②烧杯和玻璃棒没有洗涤2~3次______。
③配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中______。
④若定容时俯视,所配溶液的物质的量浓度______。
【答案】BC滴定管 玻璃棒滴定管玻璃棒AC③①④②AEA无影响偏低偏低偏高
【解析】
(1)操作步骤有计算、量取、稀释、洗涤、定容、摇匀等操作,一般用滴定管量取浓盐酸,在烧杯中稀释(可用量筒量取水加入烧杯),并用玻璃棒搅拌。冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2﹣3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀。所以所需仪器有滴定管、烧杯、玻璃棒、250mL容量瓶、胶头滴管,故不需要的仪器是BC,还需要的仪器是滴定管和玻璃棒,在稀释浓盐酸时先使用滴定管进行量取弄溶液,再用玻璃棒引流加入到容量瓶;
(2)浓盐酸的物质的量浓度为![]() 12.1mol/L,设所需的浓盐酸的体积为VmL,根据溶液稀释定律c浓V浓=c稀V稀可知:12.1mol/L×VmL=250mL×0.1mol/L,解得V=2.1mL,根据大而近的原则,应选用10mL的量筒,答案选A;容量瓶只有一条刻度线,故只能配制和其规格相对应的体积的溶液,故配制250mL的溶液,应选用250mL 容量瓶,答案选C;
12.1mol/L,设所需的浓盐酸的体积为VmL,根据溶液稀释定律c浓V浓=c稀V稀可知:12.1mol/L×VmL=250mL×0.1mol/L,解得V=2.1mL,根据大而近的原则,应选用10mL的量筒,答案选A;容量瓶只有一条刻度线,故只能配制和其规格相对应的体积的溶液,故配制250mL的溶液,应选用250mL 容量瓶,答案选C;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知操作顺序是③①④②;
(4)A、带塞子的容器在使用前均要检查是否漏液,故容量瓶使用前要先检查是否漏液,A正确;
B、容量瓶不能润洗,否则会导致溶质的物质的量偏大,所配溶液的浓度偏高,B错误;
C、容量瓶只适用于配制一定浓度的溶液,比较精密,不能受热,故不能用来溶解固体,C错误;
D、容量瓶只适用于配制一定浓度的溶液,比较精密,不能受热,故不能用来稀释溶液,D错误;
E、定容完成后应摇匀,摇匀时要盖好瓶盖,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,E正确;
答案选AE。
(5)定容摇匀时要颠倒过来摇晃,故在塞子和瓶颈部分会有溶液残留,因此发现凹液面低于线是正常的,不用采取任何补救措施,故直接将溶液装瓶即可,答案选A;
(6)①若容量瓶未干燥即用来配制溶液,对溶液浓度无影响,因为只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响;
②烧杯和玻璃棒没有洗涤2~3次,会导致溶质损失,则浓度偏低;
③配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中,则浓度偏低;
④若定容时俯视,则溶液体积偏小,则所配溶液的物质的量浓度偏高。


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 1mol 的P4O6中含有6 NA个P—O键
B. 0.1mo1H2和0.1molI2于密闭容器中充分反应后,分子总数小于0.2 NA
C. pH=3的CH3COOH溶液中,含有10-3NA个H+
D. 高温下,16.8gFe 与足量的水蒸气反应,失去0.8NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O===O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
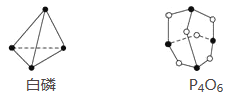
A. 吸收1 638 kJ能量 B. 放出1 638 kJ能量
C. 吸收126 kJ能量 D. 放出126 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用如图的装置制备乙酸乙酯。
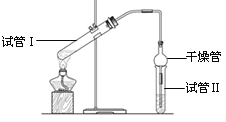
(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:_____________。
(2)请写出用CH3CH218OH制备乙酸乙酯的化学方程式:_____________,反应类型为_______。
(3)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
实验 编号 | 试管Ⅰ中的试剂 | 试管Ⅱ中的试剂 | 有机层的厚度/cm |
A | 2 mL乙醇、1 mL乙酸、 1mL18mol·L-1 浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
B | 2 mL乙醇、1 mL乙酸 | 0.1 | |
C | 2 mL乙醇、1 mL乙酸、 3 mL 2mol·L-1 H2SO4 | 0.6 | |
D | 2 mL乙醇、1 mL乙酸、盐酸 | 0.6 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是______mL和_____mol·L-1 。
②分析实验_________________(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(4)若现有乙酸90g,乙醇138g发生酯化反应得到80g乙酸乙酯,试计算该反应的产率为______________(用百分数表示,保留一位小数)。
II、已知乳酸的结构简式为![]() 。试回答:
。试回答:
①乳酸分子中的官能团有:_____________________________________(写名称);
②乳酸与足量金属钠反应的化学方程式为________________________________;
③已知—COOH不会发生催化氧化,写出加热时,乳酸在Cu作用下与O2反应的化学方程式:________________________________________________;
④腈纶织物产泛地用作衣物、床上用品等。腈纶是由CH2=CH-CN聚合而成的。 写出在催化剂、加热条件下制备腈纶的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%,其余为氧。
(1)X的分子式是________。
(2)X能与金属钠反应放出氢气,则X结构中含有的官能团的名称为________。
(3)X与空气中的氧气在催化剂作用下反应生成了Y,该反应的化学方程式是_________,反应类型为________。
(4)X与高锰酸钾酸性溶液反应可生成Z,在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应生成132 g W,该反应的化学方程式为_________,其中X的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃的锌锰干电池对环境污染很大,工业上可用如下工艺回收正极材料中的金属(部分条件未给出):
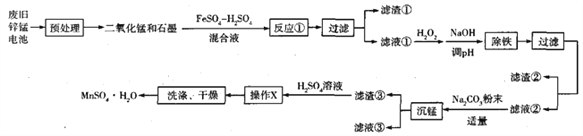
(1)废弃的锌锰干电池对环境的主要危害是__________, ![]() 中
中![]() 的化合价为__________。
的化合价为__________。
(2)锌锰干电池中氯化铵为电解质,其电子式为______________________________。
(3)反应①中氧化剂与还原剂的物质的量之比为______________________________。
(4)该工艺流程中多次用到过滤,实验室中过滤所需要的玻璃仪器有__________。
(5)已知:25℃时, ![]() ,滤液①中加入NaOH溶液至pH=_________时,
,滤液①中加入NaOH溶液至pH=_________时, ![]() 沉淀完全
沉淀完全![]() 时,认为
时,认为![]() 沉淀完全]。
沉淀完全]。
(6)写出“沉锰”过程中生成碱式碳酸锰![]() 的离子方程式为:______________________________________________________________________。
的离子方程式为:______________________________________________________________________。
(7)用硫酸酸化的![]() 浆液可吸收工业废气中的
浆液可吸收工业废气中的![]() 生成
生成![]() ,已知浆液中
,已知浆液中![]() 含量为
含量为![]() ,工业废气中
,工业废气中![]() 含量为
含量为![]() ,
, ![]() 的吸收率可达90%,则处理1000
的吸收率可达90%,则处理1000![]() 工业尾气,可得到
工业尾气,可得到![]() 的质量为__________kg(用含字母的代数式表示)。
的质量为__________kg(用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
A. v正(X)=v逆(Z)
B. 容器内压强不随时间变化
C. 容器内X、Y、Z的浓度之比为l:2:2
D. 单位时间内消耗0.1 mol X的同时生成0.2 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个隔热恒容的密闭容器中进行下列两个可逆反应:甲中:C(s)+H2O(g) ![]() CO(g)+H2(g);乙中:CO(g)+H2O(g)
CO(g)+H2(g);乙中:CO(g)+H2O(g) ![]() CO2(g)+H2(g)。现有下列状态:①混合气体平均相对分子质量不再改变 ②恒温时,气体压强不再改变 ③各气体组分浓度相等 ④反应体系中温度保持不变 ⑤断裂氢氧键反应速率等于断裂氢氢键反应速率的2倍 ⑥混合气体密度不变 ⑦单位时间内,消耗水的质量与生成氢气的质量之比为9∶1 ⑧同一时间内,水蒸气消耗的物质的量等于氢气消耗的物质的量。其中能表明甲、乙容器中反应都达到平衡状态的是
CO2(g)+H2(g)。现有下列状态:①混合气体平均相对分子质量不再改变 ②恒温时,气体压强不再改变 ③各气体组分浓度相等 ④反应体系中温度保持不变 ⑤断裂氢氧键反应速率等于断裂氢氢键反应速率的2倍 ⑥混合气体密度不变 ⑦单位时间内,消耗水的质量与生成氢气的质量之比为9∶1 ⑧同一时间内,水蒸气消耗的物质的量等于氢气消耗的物质的量。其中能表明甲、乙容器中反应都达到平衡状态的是
A. ④⑤⑧ B. ③④⑥ C. ⑥⑦⑧ D. ①②⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com