
【题目】在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是
A. v正(X)=v逆(Z)
B. 容器内压强不随时间变化
C. 容器内X、Y、Z的浓度之比为l:2:2
D. 单位时间内消耗0.1 mol X的同时生成0.2 mol Z
【答案】B
【解析】
在一定条件下,当可逆反应中正反应速率和逆反应速率相等时(但不为0),各种物质的浓度或含量均不再发生变化的状态,是化学平衡状态,据此判断。
A. v正(X)=v逆(Z)中反应速率的方向相反,但不满足反应速率之比是相应的化学计量数之比,反应没有达到平衡状态,A错误;
B. 根据方程式可知,反应前后气体体积是减小的,所以容器内压强不随时间变化说明反应达到平衡状态,B正确;
C. 容器内X、Y、Z的浓度之比为l:2:2不能说明正逆反应速率相等,不一定达到平衡状态,C错误;
D. 单位时间内消耗0.1molX的同时生成0.2molZ中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此关系始终是成立,不能说明反应达到平衡状态,D错误。
答案选B。


科目:高中化学 来源: 题型:
【题目】甲烷、氧气、KOH 溶液可构成燃料电池提供电能。按要求填写:
(1)该电池总反应的离子方程式为___________________________。
(2)通入甲烷的电极为原电池的________极,该电极反应式为:______________________。
(3)电池工作时,正极区域溶液的pH__________(填“增大、减小或不变”)。
(4) 电路中通过3mol 电子转移时,消耗的氧气体积为(标况)_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校环保兴趣小组在处理污水样品时,需将质量分数为37%的浓盐酸(密度为1.19gcm﹣3)配制成250mL0.1molL﹣1的盐酸溶液。
(1)在如图所示仪器中,配制上述溶液不需要的是______(填图中相应仪器的字母)。除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_______,其作用按使用的先后顺序分别是_______和_______。

(2)根据计算,下列量程或规格中,本实验量筒应使用的是______;容量瓶应使用______(填写相应的序号)。
A.10mL B.100mL C.250mL D.500mL
(3)在量取浓盐酸后,下列操作的先后顺序是______(用编号表示)。
①待稀释的盐酸温度与室温一致后,沿玻璃棒注入所选定规格的容量瓶中
②往容量瓶中小心加蒸馏水至液面接近环形刻度线1cm~2cm处,改用胶头滴管加蒸馏水,使凹液面最低处与瓶颈的环形刻度线相切
③在盛盐酸的烧杯中注入适量蒸馏水,并用玻璃棒搅拌,使其混合均匀
④用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部注入容量瓶
(4)关于容量瓶的使用,下列操作正确的是______(填字母,下同)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1cm~2cm处,改用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1cm~2cm处,改用胶头滴管加蒸馏水至刻度线
E。盖好瓶盖,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(5)若定容后摇匀静置,发现凹液面低于线,此时应该______。
A.直接转移到细口试剂瓶中
B.再用胶头滴管加水,重新定容
C.将此溶液倒掉,重新配制
D.直接储存于容量瓶中
(6)假设配制时其他操作均正确,只出现以下某一情况,试判断所配制的溶液浓度相比于要求的值(即0.1molL﹣1)如何变化。(a.偏高;b.偏低;c.无影响,在下列横线上填相应的字母)。
①容量瓶中有少量蒸馏水______。
②烧杯和玻璃棒没有洗涤2~3次______。
③配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中______。
④若定容时俯视,所配溶液的物质的量浓度______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。请回答下列问题:
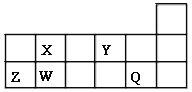
(1)W在周期表中的位置是___________,Y、Z的离子半径由大到小的顺序为___________ (用元素符号表示);由X与氢元素组成四原子化合物的电子式为__________。
(2)下列说法正确的是____________。
a.XY2和WY2都能溶于水生成对应的酸
b.Q的含氧酸的酸性比X的含氧酸的酸性强
c.X的最简单气态氢化物的稳定性大于W的最简单气态氢化物的稳定性
d.由NaOH溶液分别滴入MgQ2、ZQ3溶液中的反应现象可比较Mg和Z金属性的强弱
(3)自来水厂常用QY2对饮用水进行消毒,处理后的水中要求QY2的浓度在0.10~0.80 mg·L-1之间。碘量法可以检测水中QY2的浓度,步骤如下:
操作Ⅰ:取一定体积的水样,加入一定量的碘化钾,再用NaOH溶液调至中性,并加入淀粉溶液,溶液变蓝。
操作Ⅱ:再加入一定量的Na2S2O3溶液。(已知:2S2O![]() +I2=S4O
+I2=S4O![]() +2I-)
+2I-)
操作Ⅲ:然后再加硫酸调节水样pH至1~3。
操作时,不同pH环境中Q元素粒子种类及化合价如图所示:
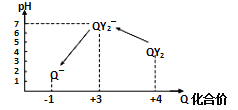
①操作Ⅰ中反应的离子方程式是_________________________。
②确定操作Ⅱ完全反应的现象是_________________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是______________________。
④若水样的体积为1.0 L,在操作Ⅱ中消耗了1.0×10-3mol·L-1的Na2S2O3溶液10 mL,则水样中QY2的浓度是_______________mg·L-1(精确到0.01)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式的反应热表示可燃物的燃烧热的是
A. H2(g)+I2(g)![]() 2HI(g) △H=-9.48 kJ mol-1
2HI(g) △H=-9.48 kJ mol-1
B. CH4(g)+2O2(g)=2H2O(g)+CO2(g) △H =-802.3 kJ mol-1
C. 2CO(g)+O2(g)= 2CO2(g) △H=-566 kJ mol-1
D. H2(g)+ ![]() O2(g)=H2O(l) △H=-285.8 kJ mol-1
O2(g)=H2O(l) △H=-285.8 kJ mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 氯化铁溶液溶解铜片:Fe3++ Cu=Fe2++ Cu2+
B. 氯气与水反应:Cl2 + H2O ![]() 2H+ + Cl-+ ClO-
2H+ + Cl-+ ClO-
C. 硝酸银溶液中加入过量氨水:Ag+ + NH3·H2O=AgOH↓+ NH4+
D. Ca(HCO3)2溶液与少量NaOH溶液反应: Ca2++ HCO3-+ OH-=CaCO3↓+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过以下反应均可获取O2。下列有关说法不正确的是
①光催化分解水制氧气:2H2O(l)=2H2(g) + O2(g) ΔH1=+571.6 kJ·mol-1
②过氧化氢分解制氧气:2H2O2(l)=2H2O(l) + O2(g) ΔH2=-196.4 kJ·mol-1
③一氧化氮分解制氧气:2NO(g)=N2(g) + O2(g) ΔH3=-180.5 kJ·mol-1
A. 反应①是人们获取H2的途径之一
B. 反应②、③都是化学能转化为热能
C. 反应H2O2(l)=H2O(g)+ ![]() O2(g)的ΔH=-98.2 kJ·mol-1
O2(g)的ΔH=-98.2 kJ·mol-1
D. 反应2H2(g)+2NO(g)=N2(g)+2H2O(l)的ΔH=-752.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Yohiaki Nakao报道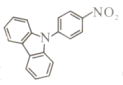 (b)在Pd催化下可发生Buchwald-Hartwig偶联反应。下列说法不正确的是
(b)在Pd催化下可发生Buchwald-Hartwig偶联反应。下列说法不正确的是
A. b的分子式为C18H12N2O2
B. b的一氯代物有4种
C. b可发生取代反应
D. b的所有原子不一定共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com