
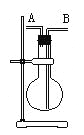
【题目】某学生想利用下图装置(烧瓶位置不能移动)收集下列气体:
① H2②Cl2③CH4④HCl ⑤NH3⑥NO ⑦NO2⑧SO2,
下列操作正确的是
A. 烧瓶是干燥的,由A进气收集①③⑤
B. 烧瓶是干燥的,由B进气收集②④⑥⑦⑧
C. 在烧瓶中充满水,由A进气收集①③⑤⑦
D. 在烧瓶中充满水,由B进气收集⑥
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如图所示:
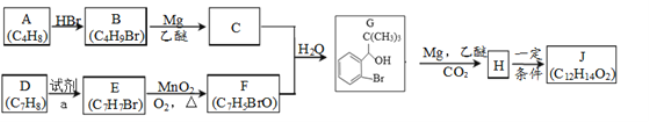
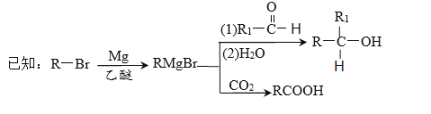
(1)A的名称是_______,E到F的反应类型是___________。
(2)试剂a是________,F中官能团名称是_______。
(3)M组成比F多1个CH2,M的分子式为C8H7BrO,M的同分异构体中:①能发生银镜反应;②含有苯环;③不含甲基。满足上述条件的M的同分异构体共有______种。
(4)J是一种酯,分子中除苯环外还含有一个五元环,J的结构简式为__________。H在一定条件下还能生成高分子化合物K,H生成K的化学方程式为________。
(5)利用题中信息写出以乙醛和苯为原料,合成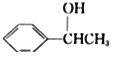 的路线流程图(其它试剂自选)。________。
的路线流程图(其它试剂自选)。________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液导电能力越强,电导率越大。常温下用0.1000 mol/L 盐酸分别滴定10.00 mL浓度均为0.1000 mol/L的NaOH溶液和二甲胺[ (CH3)2NH]溶液( 二甲胺在水中电离与氨相似,已知在常温下Kb[(CH3)2NH·H2O] =1.6×10-4),利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
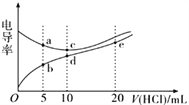
A. 盐酸滴定二甲胺实验中选择酚酞做指示剂比选甲基橙误差更小
B. d点溶液中:c(H+)<c(OH-)+c[(CH3)2NH2+]
C. a 点溶液与d点的溶液混合后的溶液中:c[(CH3)2NH2+]<c[(CH3)2NH·H2O]
D. b、c、e.三点的溶液中,水的电离程度最大的是e点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中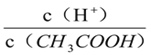 减小
减小
B. 将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C. 向盐酸中加入氨水至中性,溶液中![]() >1
>1
D. 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中不![]() 变
变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种物质,它们的相互转化关系如下图(反应条件略,有些反应的产物和反应的条件没有全部标出)。已知A、B、E是单质,其中A着火只能用干燥的沙土灭火,B在常温下为气体,C俗名称为烧碱,D为无色无味液体。

(1)写出A、B、F的化学式 A______ B ______ F ______。
(2)写出A和D反应生成B和C的化学方程式_____________。若生成3mol的B,则转移的电子数目为_______________ 。
(3)写出E与C、D反应生成的B和F离子方程式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如下图所示,下列说法不合理的是

A. 能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
B. 装置C的作用是吸收SO2尾气,防止污染空气
C. 为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去
D. 为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方法不正确的是(括号内为杂质)
A. NO(NO2)通过H2O溶液 B. CO2(HCl)通过饱和NaHCO3溶液
C. Fe(Al)盐酸溶液 D. Cl2(HCl) 饱和食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应:Fe2O3+2Al![]() Al2O3+2Fe。
Al2O3+2Fe。
(1)________元素的化合价升高,则该元素的原子________电子,被________(填“氧化”或“还原”);而________元素的化合价降低,则该元素的原子________电子,被________(填“氧化”或“还原”)。
(2)该反应中Fe2O3发生了________反应,Al发生了________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.100mol·L-1的NaOH溶液分别滴定均为20.00mL0.100mol·L-1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是

A. I表示的是滴定醋酸的曲线
B. pH =7时,滴定醋酸消耗的V(NaOH)>20.00mL
C. V(NaOH)= 20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D. V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com