
����Ŀ���о�SO2��NOx�ȶԸ��ƿ�������������Ҫ���壮
��1��NOx������β���е���Ҫ��Ⱦ��֮һ����NOx���γ����꣬��NO2�γɵ������к��е���Ҫ������ ��
����������������ʱ�ĸ��»�����N2��O2��Ӧ����Ӧ�Ļ�ѧ����ʽ�� ��
��2��Ϊ����SO2���ŷţ�����ȡһЩ��Ч��ʩ�����ں���ú�м�����ʯ�ҿ�����������ã�ȼ�չ����У���Ԫ��ת���������̬�Ļ�����û�����Ļ�ѧʽ�� ��
�����������У����������������е�SO2����������ţ���
a��Na2CO3 b��H2SO4 c��NaHSO3 d��NH3H2O
��3��ȡij��������������ˮ�����Ƴɴ���Һ���������������Ӽ���Ũ�������
���� | K+ | Na+ | NH4+ | H+ | SO | NO | Cl�� |
Ũ��/molL��1 | 4��10��6 | 6��10��6 | 2��10��5 | a | 4��10��5 | 3��10��5 | 2��10��5 |
���ݱ������ݼ��㣺a=mol/L��
���𰸡�
��1��H+��NO ![]() ��N2+O2�T2NO
��N2+O2�T2NO
��2��CaSO4��ad
��3��1��10��4
���������⣺��1����NOx���γ����꣬��NO2�γɵ�����Ϊ���������꣬������Һ�к��е���Ҫ������H+��NO ![]() �����Դ��ǣ�H+��NO
�����Դ��ǣ�H+��NO ![]() ������������������ʱ�ĸ��»�����N2��O2��Ӧ����Ӧ�Ļ�ѧ����ʽ��N2+O2�T2NO�� ���Դ��ǣ�N2+O2�T2NO����2������ȼú�м�����ʯ�ҿ�����������ã�SO2�����պ�ת����һ����Ԫ�ص����̬�Ļ�����������ƺͶ�������Ӧ����������ƣ�������Ʊ��������ΰ����ƣ�CaO+SO2+O2=CaSO4 �� ���̬�Ļ�����ΪCaSO4 �� ���Դ��ǣ�CaSO4���ڶ������������������ a��Na2CO3��Һ�������ն������������������ƺͶ�����̼����a��ȷ�� b����������ն�������b���� c��NaHSO3�������ն�������c���� d��NH3H2O�����ն�����������������炙���������泥���d��ȷ�����Դ��ǣ�ad����3����Һ�д��ڵ���غ�c��K+��+c��Na+��+c��NH4+��+c��H+��=2c��SO
������������������ʱ�ĸ��»�����N2��O2��Ӧ����Ӧ�Ļ�ѧ����ʽ��N2+O2�T2NO�� ���Դ��ǣ�N2+O2�T2NO����2������ȼú�м�����ʯ�ҿ�����������ã�SO2�����պ�ת����һ����Ԫ�ص����̬�Ļ�����������ƺͶ�������Ӧ����������ƣ�������Ʊ��������ΰ����ƣ�CaO+SO2+O2=CaSO4 �� ���̬�Ļ�����ΪCaSO4 �� ���Դ��ǣ�CaSO4���ڶ������������������ a��Na2CO3��Һ�������ն������������������ƺͶ�����̼����a��ȷ�� b����������ն�������b���� c��NaHSO3�������ն�������c���� d��NH3H2O�����ն�����������������炙���������泥���d��ȷ�����Դ��ǣ�ad����3����Һ�д��ڵ���غ�c��K+��+c��Na+��+c��NH4+��+c��H+��=2c��SO ![]() ��+c��NO
��+c��NO ![]() ��+c��Cl�������ͼ�����ݼ���õ�������Ũ��c��H+��=1��10��4 mol/L�����Դ��ǣ�1��10��4 ��
��+c��Cl�������ͼ�����ݼ���õ�������Ũ��c��H+��=1��10��4 mol/L�����Դ��ǣ�1��10��4 ��
�����㾫�������ö����������Ⱦ����������Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪SO2����Ⱦ��������Ҫ�к�����֮һ��ֱ��Σ��������������������γ�����pH��5��6���ƻ�ũ���ɭ�֡���ԭ��ʹ����������ǿ�ȵȣ���SO2�Ĺ�ҵ�������뾭���������������ŷŵ������У�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݡ��ο���Ϣ���������п�ѧ��������ǡ�21���͵���Դ������δ����ʯ�͡��Ĺ۵㣮
��1���������������ȼ�յ��Ȼ�ѧ����ʽΪSi��s��+O2��g���TSiO2��s����H=��989.2kJmol��1 �� �йؼ����������±���
��ѧ�� | Si��O | O=O | Si��Si |
����kJmol��1 | x | 498.8 | 176 |
��֪1molSi�к�2molSi��Si����1molSiO2�к�4molSi��O������x��ֵΪ ��
��2���������Ϊһ���ձ�ʹ�õ�������Դ���������ã��������������ص�����˵���У�����Ϊ�������� ��
A.��������䡢���棬�Ӱ�ȫ�Ƕȿ��ǣ�������ѵ�ȼ��
B.�����Դ�ḻ�����ڿ��ɣ��ҿ�����
C.��ȼ�շų�����������ȼ�ղ���Ի�����Ⱦ�̶ȵͣ�������Ч����
D.Ѱ�Ҹ�Ч�´���������ʹ��ӦSiO2+2C ![]() Si+2CO���ڳ����·������ǹ���Դ�������õĹؼ�����
Si+2CO���ڳ����·������ǹ���Դ�������õĹؼ�����
��3����ҵ�Ʊ�����ķ�ӦΪ2H2��g��+SiCl4��g���TSi��s��+4HCl��g����H=+240.4kJmol��1 �� ���ɵ�HClͨ��100mL 1molL��1��NaOH��Һǡ����ȫ�����գ��������Ʊ�����ķ�Ӧ������������ա����ͷš���������ΪkJ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ������������ǣ� �� 
A.ͼ1��ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯
B.ͼ2��ʾ0.1000molL��1NaOH��Һ�ζ�20.00mL0.1000molL��1CH3COOH��Һ���õ��ĵζ�����
C.ͼ3��ʾKNO3���ܽ�����ߣ�ͼ��a����ʾ����Һ��80��ʱKNO3�IJ�������Һ
D.ͼ4 ��ʾij���淴Ӧ����������淴Ӧʱ��仯�����ߣ���ͼ֪tʱ��Ӧ��ת�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵���
A. CaCO3(s) ![]() CaO(s)��CO2(g)��ƽ��ʱ�������������С��һ�룬��ƽ���CO2Ũ����ԭƽ����ͬ
CaO(s)��CO2(g)��ƽ��ʱ�������������С��һ�룬��ƽ���CO2Ũ����ԭƽ����ͬ
B. ����Kw����
C. ���ȵĴ�����Һȥ��Ч������
D. ���º�ѹ����������2NO2![]() N2O4����ͨ��Ar���������ɫ�ȱ�dz������
N2O4����ͨ��Ar���������ɫ�ȱ�dz������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ�����ӵ����ʵ���Ũ�ȴ�С��ϵ��ȷ������ ��
A. �����ʵ���Ũ�ȵ�������Һ����H2CO3 ��Na2CO3 ��NaHCO3 ��(NH4)2CO3������c(CO32-)�Ĵ�С��ϵΪ����>��>��>��
B. pH=2 ��H2C2O4��Һ��pH=12 ��NaOH ��Һ����������c(H+)+c(Na+)=c(OH-)+c(HC2O4-)+c(C2O42-)
C. ��0.2mo/L ��NaHCO3 ��Һ�м�������0.1mo/L ��NaOH ��Һ��c(CO32- )>c(HCO3-)>c(OH-)>c(H+)
D. �����£���Ũ�ȵ�CH3COOH��CH3COONa ��Һ�������ϣ���Һ��pH<7��c(CH3COOH)+c(OH-)>c(H+)+c(Na+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں���NaBr��NaI����Һ��ͨ������Cl2��Ȼ�����Һ���ɣ��������ù������գ����ʣ���������( )
A.NaCl��NaBrB.NaCl��I2C.NaClD.NaCl��NaBr��I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʼȲ�����ͬϵ�Ҳ������ͬ���칹����ǣ� ��
A. ���ȼױ��Ͷ��ȼױ� B. һ�ȼ���Ͷ�������
C. �����Ӳ֬�� D. ���Ǻ���ѿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������н������¿��淴Ӧ��M��g��+N��g��P��g��+2L���ڲ�ͬ��������P�İٷֺ���P%�ı仯�����ͼ����÷�Ӧ�� �� 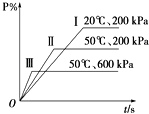
A.����Ӧ���ȣ�L�ǹ���
B.����Ӧ���ȣ�L������
C.����Ӧ���ȣ�L������
D.����Ӧ���ȣ�L�ǹ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ1.43gNa2CO3xH2O����ˮ���10mL��Һ��Ȼ����ε���ϡ����ֱ��û������ų�Ϊֹ����ȥ����2.0mL�����ռ���112mL CO2����״�������Լ��㣺
��1��CO2�����ʵ���
��2��Na2CO3xH2O�����ʵ�����
��3��x��ֵ��
��4������ϡ��������ʵ�Ũ�ȣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com