
【题目】据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点.
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)═SiO2(s)△H=﹣989.2kJmol﹣1 , 有关键能数据如下表:
化学键 | Si﹣O | O=O | Si﹣Si |
键能kJmol﹣1 | x | 498.8 | 176 |
已知1molSi中含2molSi﹣Si键,1molSiO2中含4molSi﹣O键,则x的值为 .
(2)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是 .
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,可以使反应SiO2+2C ![]() Si+2CO↑在常温下发生,是硅能源开发利用的关键技术
Si+2CO↑在常温下发生,是硅能源开发利用的关键技术
(3)工业制备纯硅的反应为2H2(g)+SiCl4(g)═Si(s)+4HCl(g)△H=+240.4kJmol﹣1 , 生成的HCl通入100mL 1molL﹣1的NaOH溶液恰好完全被吸收,则上述制备纯硅的反应过程中(填“吸收”或“释放”)的热量为kJ.
【答案】
(1)460
(2)D
(3)吸收;6.01
【解析】解:(1)已知晶体硅的燃烧热为989.2kJmol﹣1 , 则Si(s)+O2(g)=SiO2(s)△H=﹣989.2kJmol﹣1;1mol晶体硅中含有2molSi﹣Si,1molSiO2中含有4molSi﹣O,1molO2中含有1molO=O,则反应焓变△H=2×176+498.8﹣4x=﹣989.2,解得x=460,
所以答案是:460;(2)A.硅常温下为固体,性质较稳定,便于贮存,较为安全,故A正确;
B.硅在自然界中含量丰富,主要以硅酸盐和二氧化硅的形式存在,且可再生,故B正确;
C.硅作为一种普遍使用的新型能源被开发利用说明燃烧放出的热量大,硅燃烧生成二氧化硅,二氧化硅是固体,容易得至有效控制,故C正确;
D.催化剂只能加快化学反应的速率,不改变反应热,故D错误.
所以答案是:D;(3)通入100mL 1molL﹣1的NaOH溶液恰好反应说明生成的氯化氢为0.1mol,设反应吸收的热量为x.
2H2(g)+SiCl4(g)═Si(s)+4HCl(g)△H=+240.4kJmol﹣1
4 240.4
0.1 x
解得X=6.01kJ,
所以答案是:吸收、6.01.
【考点精析】根据题目的已知条件,利用反应热和焓变的相关知识可以得到问题的答案,需要掌握在化学反应中放出或吸收的热量,通常叫反应热.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组按照下列流程进行“由镁铝合金制备硫酸铝晶体”的实验如图1.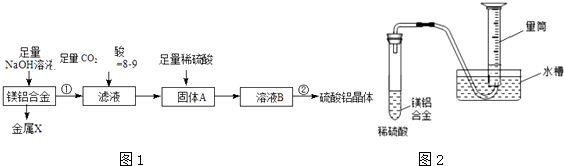
(1)写出硫酸铝在水中的电离方程式 ,
(2)镁铝合金中加NaOH溶液的离子反应方程式为 , 滤液中通入足量CO2的化学方程式
(3)操作②包含的步骤有蒸发浓缩、、过滤、干燥.
(4)金属X在CO2中燃烧的化学方程式
(5)该兴趣小组为测定镁铝合金中各组成的质量分数,设计如图2装置,则需要测定的数据(温度、压强除外)有、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol两种气体烃组成的混合气完全燃烧后得3.36L(标况)CO2和3.6g水蒸气,对于组成判断正确的是( )
A.一定有甲烷
B.一定有乙烯
C.一定有乙炔
D.一定有乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式是: 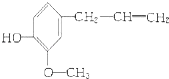 该物质不应有的化学性质是( ) ①可以燃烧
该物质不应有的化学性质是( ) ①可以燃烧
②可以跟溴加成
③可以将KMnO4酸性溶液还原
④可以跟NaHCO3溶液反应
⑤可以跟NaOH溶液反应
⑥可以发生消去反应.
A.①③
B.③⑥
C.④⑥
D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三种溶液,进行如下操作: ![]()
则甲、乙、丙三种溶液可能是( )
A.BaCl2、H2SO4、MgCl2
B.CaCl2、HNO3、AgNO3
C.CaCl2、HNO3、NaCl
D.BaCl2、HCl、Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写及解释均正确的是
A. 0.1mol/L 的 Na2S溶液中 c(S2-)<0.1mol/L 的原因:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
B. 实验室制备氢氧化铁胶体:Fe3++3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
C. 水中加入NaOH:H2O+H2O![]() H3O++OH-加入NaOH,消耗溶液中的H3O+平衡右移
H3O++OH-加入NaOH,消耗溶液中的H3O+平衡右移
D. 在碳酸钠溶液中通入CO2气体,CO32-+H2O![]() HCO3-+OH-,CO2 消耗OH- 促使平衡正向移动
HCO3-+OH-,CO2 消耗OH- 促使平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合题。
(1)反应Fe(s)+CO2(g)FeO(s)+CO(g)△H1 , 平衡常数为K1;反应Fe(s)+H2O(g)FeO(s)+H2(g)△H2 , 平衡常数为K2 . 在不同温度时K1、K2的值如表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
①反应 CO2(g)+H2(g)CO(g)+H2O(g)△H,平衡常数K,则△H=(用△H1和△H2表示),K=(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)CO(g)+H2O(g)是反应(填“吸热”或“放热”).
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图所示:
①该条件下反应的平衡常数为;
②下列措施中能使平衡时 ![]() 增大的是(填序号)
增大的是(填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是(填字母).
a.容器中压强不变 b.气体的密度不再改变c.v正(CO2)=v逆(CO) d.c(CO2)=c(CO) e.容器内气体总物质的量不变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同温度下,0.01molL﹣1 NaOH溶液和0.01molL﹣1的盐酸相比,下列说法正确的是( )
A.由水电离出的[H+]相等
B.由水电离出的[H+]都是1.0×10﹣12 molL﹣1
C.由水电离出的[OH﹣]都是0.01 molL﹣1
D.两者都促进了水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究SO2、NOx等对改善空气质量具有重要意义.
(1)NOx是汽车尾气中的主要污染物之一.①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有 .
②汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是 .
(2)为减少SO2的排放,常采取一些有效措施.①在含硫煤中加入生石灰可以起到固硫的作用,燃烧过程中,硫元素转化成其最高价态的化合物,该化合物的化学式是 .
②下列物质中,可用于吸收烟气中的SO2的是(填序号).
a.Na2CO3 b.H2SO4 c.NaHSO3 d.NH3H2O
(3)取某空气样本用蒸馏水处理制成待测液,其中所含的离子及其浓度如表:
离子 | K+ | Na+ | NH4+ | H+ | SO | NO | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣6 | 2×10﹣5 | a | 4×10﹣5 | 3×10﹣5 | 2×10﹣5 |
根据表中数据计算:a=mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com