
【题目】有甲、乙、丙三种溶液,进行如下操作: ![]()
则甲、乙、丙三种溶液可能是( )
A.BaCl2、H2SO4、MgCl2
B.CaCl2、HNO3、AgNO3
C.CaCl2、HNO3、NaCl
D.BaCl2、HCl、Na2CO3
【答案】D
【解析】解:A.碳酸钠可以和氯化钡反应得到碳酸钡沉淀,但是碳酸钡和硫酸反应生成硫酸钡,沉淀不溶解,故A错误;B.碳酸钠可以和CaCl2反应得到碳酸钙沉淀,碳酸钙沉淀溶于HNO3得到硝酸钙溶液,但是硝酸钙溶液和AgNO3之间不会发生反应,故B错误;
C.碳酸钠可以和CaCl2反应得到碳酸钙沉淀,碳酸钙沉淀溶于HNO3得到硝酸钙溶液,但是硝酸钙溶液和NaCl之间不会发生反应,故C错误;
D.碳酸钠可以和氯化钡反应得到碳酸钡沉淀,碳酸钡沉淀溶于HCl得到氯化钡溶液,氯化钡溶液会和碳酸钠之间反应生成碳酸钡沉淀,故D正确.
故选D.
白色沉淀与过量乙反应生成气体,则乙为酸,沉淀为碳酸钡或碳酸钙,因沉淀溶解,则乙不能为硫酸,气体为二氧化碳,溶液可为硝酸盐或氯化物,与丙反应生成白色沉淀,丙可为硫酸钠、碳酸钠等,以此解答该题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】化学与人类生活生产密切相关,下列说法不正确的是
A. 工厂可用静电除尘与胶体性质无关
B. 可用钢瓶贮存液氯或浓硫酸
C. 氢氧化铝是医用中和剂中的一种,可使胃液浓度降低,起到中和胃酸的作用。
D. 矿物脱硫脱硝可有效防止酸雨。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物与生产、生活密切相关。下列说法不正确的是
A.天然气的主要成分是甲烷B.棉花的主要成分是淀粉
C.酒精类饮料中含有乙醇D.牛奶中含有蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点.
(1)晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)═SiO2(s)△H=﹣989.2kJmol﹣1 , 有关键能数据如下表:
化学键 | Si﹣O | O=O | Si﹣Si |
键能kJmol﹣1 | x | 498.8 | 176 |
已知1molSi中含2molSi﹣Si键,1molSiO2中含4molSi﹣O键,则x的值为 .
(2)假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不妥当的是 .
A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B.硅的来源丰富,易于开采,且可再生
C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制
D.寻找高效新催化剂,可以使反应SiO2+2C ![]() Si+2CO↑在常温下发生,是硅能源开发利用的关键技术
Si+2CO↑在常温下发生,是硅能源开发利用的关键技术
(3)工业制备纯硅的反应为2H2(g)+SiCl4(g)═Si(s)+4HCl(g)△H=+240.4kJmol﹣1 , 生成的HCl通入100mL 1molL﹣1的NaOH溶液恰好完全被吸收,则上述制备纯硅的反应过程中(填“吸收”或“释放”)的热量为kJ.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32﹣、SO42﹣、NO3﹣中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( ) 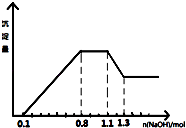
A.溶液中的阳离子只有H+、Mg2+、Al3+可能含有Fe3+
B.溶液中一定不含CO32﹣和NO3﹣ , 一定含有SO42﹣
C.溶液中c(NH4+)=0.3 mol/L
D.c(H+):c(Al3+):c(Mg2+)=1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1mol X(g)和2mol Y(g)发生反应:X(g)+mY(g) ![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1mol Z(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A. m=2 B. 第二次平衡时,Z的浓度为0.4mol/L
C. X与Y的平衡转化率之比为1:1 D. 两次平衡的平衡常数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中粒子的物质的量浓度大小关系正确的是( )
A. 等物质的量浓度的下列溶液:①H2CO3 ②Na2CO3 ③NaHCO3 ④(NH4)2CO3,其中c(CO32-)的大小关系为:②>④>③>①
B. pH=2 的H2C2O4溶液与pH=12 的NaOH 溶液等体积混合:c(H+)+c(Na+)=c(OH-)+c(HC2O4-)+c(C2O42-)
C. 向0.2mo/L 的NaHCO3 溶液中加入等体积0.1mo/L 的NaOH 溶液:c(CO32- )>c(HCO3-)>c(OH-)>c(H+)
D. 常温下,等浓度的CH3COOH与CH3COONa 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(H+)+c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com