
【题目】在含3molNaHSO3的溶液中加入含a mol NaIO3的溶液充分反应(不考虑I2+I-![]() I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如右图所示,下列说法不正确的是
I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如右图所示,下列说法不正确的是
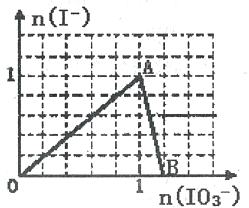
A. 还原性HSO3->I-,氧化性:IO3->SO42- >I2
B. 当a=1时,溶液中n(I2):n(I-)=3:5
C. AB段,反应的离子方程式为:IO3-+5I-+ 6H+ =3I2+3H2O
D. l<a<1.2时,溶液中SO42-与I-的物质的量之比为3:(6-5a)
【答案】A
【解析】A、0~1时溶液中I-浓度增大,发生的反应是IO3-+3HSO3-=I-+3SO42-+3H+,根据氧化剂的氧化性强于氧化产物的氧化性,还原剂的还原性强于还原产物的还原性,IO3-中I的化合价降低,作氧化剂,HSO3-中S的化合价升高,HSO3-作还原剂,即氧化性:IO3->SO42-,还原性:HSO3->I-,n(IO3-)=1以后,发生离子反应方程式为:IO3-+5I-+6H+=3I2+3H2O,氧化性IO3->I2,SO42-化合价没有变化,无法判断SO42-的氧化性与I2氧化性强弱,故说法错误;B、当a=1时,溶液中n(I-)=1mol,溶液中含有n(IO3-)=0.1mol,然后发生IO3-+5I-+6H+=3I2+3H2O,IO3-完全反应,消耗n(I-)=0.5mol,生成n(I2)=0.3mol,溶液中n(I-)=0.5mol,因此n(I2):n(I-)=0.3:0.5=3:5,故说法正确;C、根据选项A的分析,故说法正确;D、n(SO42-)=3mol,A点时溶液中n(IO3-)=(a-1)mol,n(I-)=1mol,1~1.2时,剩余n(I-)=[1-5(a-1)]mol=(6-5a)mol,因此n(SO42-):n(I-)= 3:(6-5a),故说法正确。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+CuSO4+2NH3H2O═Cu4O(PO)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的电子排布式:____________;与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有____________(填元素符号)。
(2)PO43-的空间构型是____________。
(3)P、S元素第一电离能大小关系为__________________,原因为__________________。
(4)NH3·H2O分子中NH3与H2O之间氢键表示为____________。(填序号)
A.N-H…O B.O-H…N C.H-N…H D.H-O…H
(5)氨基乙酸铜分子结构如图,碳原子的杂化方式为____________,基态碳原子核外电子有____________个空间运动状态。
![]()
(6)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1mol该配合物中含有的π键的数目为______________。
(7)铜晶体为面心立方最密堆积,配位数为_______________,铜的原子半径为127.8pm,NA表示阿伏伽德罗常数的值,列出晶体铜的密度计算式______________g/cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按题给要求填空
(1)写出以乙炔为原料制备聚氯乙烯反应方程式(无机物不限)
① 。
② 。
(2)分子式为C6H12 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为_________________,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为___________________。
(3)1分子某烷烃含有50个电子,该烷烃只能由一种结构的炔烃加氢得到,则该烷烃的结构简式为 或 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某50 mL溶液中可能含有H+、Na+、Mg2+、Al3+、SO42-、NH4+离子,当向该溶液中加入5 mol/L的NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积v(NaOH)变化关系如下图所示。
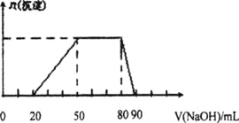
A.原溶液中一定含有的阳离子是H+、Mg2+、Al3+、SO42-
B. 原溶液中Al3+的浓度为lmol/L
C. 原溶液中NH4+的物质的量为0.4 mol
D. 当加入的NaOH溶液的体积为90mL时,反应后溶液中的离子只有Na+和SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( )
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2
②用NO2、NO、O2的物质的量浓度变化表示的反应速率比为2∶2∶1的状态
③混合气体的颜色不再改变的状态
④混合气体的密度不再改变的状态
⑤混合气体的平均摩尔质量不再改变的状态
⑥混合气体的压强不再改变的状态
A. ①②③④ B. ③④⑤⑥ C. ①③⑤⑥ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积为2L的恒温恒容密闭容器中充入2mol SO2和1mol O2,发生反应2SO2(g)+O2(g) ![]() 2SO3(g) △H=-Q kJ·mol-l (Q>O),下列有关说法不正确的是
2SO3(g) △H=-Q kJ·mol-l (Q>O),下列有关说法不正确的是
A. 反应达到平衡时,放出热量为QkJ
B. 若容器的压强不再发生交化,则反应达到平衡
C. 反应过程中c(SO2)+ c(SO3)=1 mol·L-1恒成立
D. 平衡时,SO2、O2的转化率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com