
【题目】铁屑溶于过量的盐酸后,再加入下列物质,会有三价铁生成的是( )
A.稀硫酸
B.硫化钠
C.硝酸锌
D.氯化钙
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O (l) △H=-57.3 KJ·mol-1。分别向1L 0.5mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀硝酸;③稀醋酸,恰好完全反应的热效应分别为△H1、△H2、△H3,下列关系正确的是( )
A.△H1>△H2>△H3 B.△H1<△H2<△H3
C.△H1>△H2=△H3 D.△H1=△H2<△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是( )
A. H+、SO42-、CO32- B. Na+、Cl-、SO42-
C. Ba2+、CO32-、NO3- D. Ca2+、SO42-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是一种重要材料的中间体,结构简式为:(CH3)2CHCOO ![]() CHO。合成M的一种途径如下:
CHO。合成M的一种途径如下:
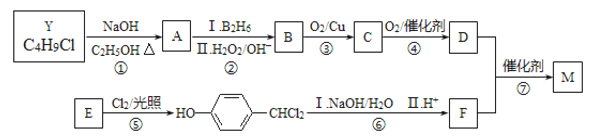
A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:①RCH=CH2 ![]() RCH2CH2OH
RCH2CH2OH
两个羟基连接在同一个碳原子上不稳定,易脱水;
请回答下列问题:
(1)若Y的核磁共振氢谱只有1种峰,则Y的结构简式为____________。
(2)A的名称是____________,由B生成C的反应类型为____________。
(3)M中的官能团有____________ (填官能团名称)。
(4)步骤⑥中反应I的化学方程式为___________________________。
(5)步骤⑦的化学反应方程式是_____________________________。
(6)D的同分异构体中,能在碱性条件下水解的有_______种(不包括立体异构),其中能发生银镜反应的同分异构体的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、二氧化碳、青霉素、硝酸钾、乙醇、氨等“分子”改变过人类的世界。
(1)铁原子在基态时,外围电子排布式为____________。
(2)CO2的电子式为____________,1 mol CO2分子中含有σ键的物质的量为____________。
(3)6-氨基青霉烷酸的结构如图所示:
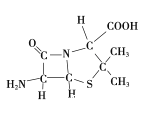
①其中C、N、O原子半径的大小关系为____________,电负性的大小关系为____________;
②其中采用sp3杂化的原子有C、____________。
(4)硝酸钾中NO3-的空间构型为____________,写出与NO3-互为等电子体的一种由前二周期元素原子构成的非极性分子化学式____________。
(5)乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是____________。
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若两个最近的Fe原子间的距离为a cm,则该晶体的密度计算式为____________g/cm3(用NA表示阿伏加德罗常数)。
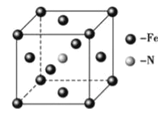
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用右图装置,完成很多电化学实验。下列有关此装置的叙述中,不正确的是
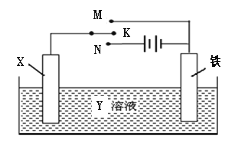
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+![]() O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
O2(g)=H2O(l) ΔH3=-285.8 kJ/mol
则2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为
A.-870.3 kJ/mol B.-571.6 kJ/mol
C.+787.0 kJ/mol D.-488.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含3molNaHSO3的溶液中加入含a mol NaIO3的溶液充分反应(不考虑I2+I-![]() I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如右图所示,下列说法不正确的是
I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如右图所示,下列说法不正确的是
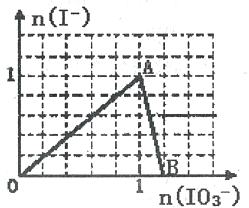
A. 还原性HSO3->I-,氧化性:IO3->SO42- >I2
B. 当a=1时,溶液中n(I2):n(I-)=3:5
C. AB段,反应的离子方程式为:IO3-+5I-+ 6H+ =3I2+3H2O
D. l<a<1.2时,溶液中SO42-与I-的物质的量之比为3:(6-5a)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检测据报道,科学家已成功合成了少量的O4,有关O4的说法正确的是
A. O4的摩尔质量是64 g
B. 相同质量的O4与O3所含原子个数之比为1∶1
C. O4与O2互为同位素
D. O4与O3、O2都是氧元素的同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com