
����Ŀ�����淴Ӧ��2NO2![]() 2NO��O2������̶����ܱ�������,�ﵽƽ��״̬�ı�־��( )
2NO��O2������̶����ܱ�������,�ﵽƽ��״̬�ı�־��( )
�ٵ�λʱ��������n molO2��ͬʱ����2n molNO2
����NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʱ�Ϊ2��2��1��״̬
�ۻ���������ɫ���ٸı��״̬
�ܻ��������ܶȲ��ٸı��״̬
�ݻ�������ƽ��Ħ���������ٸı��״̬
��������ѹǿ���ٸı��״̬
A. �٢ڢۢ� B. �ۢܢݢ� C. �٢ۢݢ� D. ȫ��
���𰸡�C
������������λʱ��������n mol O2��ͬʱ����2n molNO2��˵����Ӧv��=v�棬�ﵽƽ��״̬��������ȷ�������۷�Ӧ�Ƿ�ﵽƽ��״̬����Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�����˵���ﵽƽ��״̬����������������������ɫ���ٸı䣬˵��NO2�����Ũ�Ȳ��䣬�ﵽƽ��״̬��������ȷ�������۷�Ӧ�Ƿ�ﵽƽ��״̬�����������������䣬������������䣬���Ի��������ܶ�ʼ�ղ��䣬����˵���ﵽƽ��״̬��������������Ӧǰ������Ļ�ѧ������֮�Ͳ���ȣ����ﵽƽ��ʱ����������ʵ������䣬���������ƽ��Ħ���������ٸı䣬�ﵽƽ��״̬��������ȷ������Ӧǰ������Ļ�ѧ������֮�Ͳ���ȣ����ﵽƽ��ʱ�������ѹǿ���䣬�ﵽƽ��״̬��������ȷ����ѡC��


 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���������ˮ��Һ���ܴ����������( )
A. H+��SO42-��CO32- B. Na+��Cl-��SO42-
C. Ba2+��CO32-��NO3- D. Ca2+��SO42-��K+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��
��CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ��H1��-870��3 kJ/mol
��C(s)+O2(g)=CO2(g) ��H2��-393��5 kJ/mol
��H2(g)+![]() O2(g)=H2O(l) ��H3��-285��8 kJ/mol
O2(g)=H2O(l) ��H3��-285��8 kJ/mol
��2C(s)+2H2(g)+O2(g)=CH3COOH(l)�ķ�Ӧ��Ϊ
A��-870��3 kJ/mol B��-571��6 kJ/mol
C��+787��0 kJ/mol D��-488��3 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں�3molNaHSO3����Һ�м��뺬a mol NaIO3����Һ��ַ�Ӧ(������I2+I-![]() I3-)��������Һ�е�I-�����NaIO3�����ʵ����Ĺ�ϵ��������ͼ��ʾ������˵������ȷ����
I3-)��������Һ�е�I-�����NaIO3�����ʵ����Ĺ�ϵ��������ͼ��ʾ������˵������ȷ����
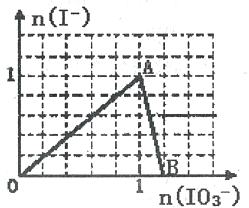
A. ��ԭ��HSO3->I-�������ԣ�IO3->SO42- >I2
B. ��a=1ʱ����Һ��n(I2)��n(I-)=3��5
C. AB�Σ���Ӧ�����ӷ���ʽΪ��IO3-+5I-+ 6H+ =3I2+3H2O
D. l<a<1.2ʱ����Һ��SO42-��I-�����ʵ���֮��Ϊ3��(6-5a)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����ҵ��ͨ�����·ֽ�FeSO4�ķ����Ʊ�Fe2O3����ѧ����ʽΪ��2FeSO4 ![]() Fe2O3+ SO3�� + SO2��Ϊ����FeSO4���·ֽ�IJ����������ʵ�飺
Fe2O3+ SO3�� + SO2��Ϊ����FeSO4���·ֽ�IJ����������ʵ�飺
����FeSO4���·ֽ���������壬��FeSO4���·ֽ����������ͨ����ͼװ���С�

�� װ��A�Թܿ�ѡ�õ��Լ���_________�����ţ���
a. ˮ b. BaCl2��Һ c. Ba(NO3)2��Һ d. Ba(OH)2��Һ
�� װ��C�������Ƿ�ֹβ����Ⱦ�������Թ���Ӧ������Լ���_________________��
�� ��װ��B�Թ�����Һ��Ϊ����KMnO4��Һ�����Թ۲쵽��Һ��ɫ��ȥ����Ӧ�����ӷ���ʽΪ__________________________ ��
��2����ҵ����һ���¶Ⱥʹ�����������NH3��NO2��ԭ����N2��ijͬѧ��ʵ�����ж�NH3��NO2��Ӧ������̽����

��ʵ���ҿ�����A��B��Cװ����ȡ�����������Cװ�ã����װ������ƿ��ʢ�ŵ��Լ�Ϊ________��д���ƣ�����Ӧ�Ļ�ѧ����ʽ��_____________________��
�� Ԥ�ռ�һƿ����İ�����ѡ����ͼ�е�װ�ã��������ռ���β������װ������˳������Ϊ������װ�á�_____________________������ĸ��ʾ��
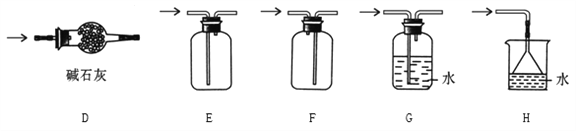
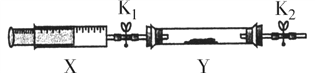
�� �������ռ�����NH3����ע����X�У�Ӳ�ʲ�����Y�м�����������������NO2�������ü���K1��K2�кã�����һ���¶��°���ͼװ�ý���ʵ�顣��K1���ƶ�ע����������ʹX�е����建��ͨ��Y���У�Y�ܹ۲쵽��ʵ��������____________________ ����Ӧ�Ļ�ѧ����ʽΪ ______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС������H2C2O4��Һ������KMnO4��Һ��Ӧ��̽������������ѧ��Ӧ���ʵ�Ӱ�족��ʵ��ʱ���ȷֱ���ȡ������Һ��Ȼ�����Թ���Ѹ����Ͼ��ȣ���ʼ��ʱ��ͨ���ⶨ��ɫ����ʱ�����жϷ�Ӧ�Ŀ�������С����������µķ�����
��� | H2C2O4��Һ | ����KMnO4��Һ | �¶�/�� | ||
Ũ��/ molL��1 | ���/mL | Ũ��/ molL��1 | ���/mL | ||
�� | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
�� | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
��1����֪��Ӧ��H2C2O4ת��ΪCO2�ݳ���KMnO4ת��ΪMnSO4������£�ÿ����89.6L CO2���壬ת�� mol ���ӡ�д��H2C2O4������KMnO4��Һ��Ӧ�����ӷ���ʽ��
��2��̽���¶ȶԻ�ѧ��Ӧ����Ӱ���ʵ������ �����ţ���ͬ������̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ����Ӱ���ʵ������ ����ʵ��ͨ���ⶨ ���жϷ�Ӧ�Ŀ�����
��3��ʵ��ٲ��KMnO4��Һ����ɫʱ��Ϊ40s�����Ի��ǰ����Һ�����С�仯�����ʱ����ƽ����Ӧ����v��KMnO4��=_______________ molL��1min��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������������ܹ��������·�Ӧ��
MnO![]() ��H2C2O4��H����Mn2����CO2����H2O(δ��ƽ)��4mL0.001mol��L��1KMnO4��Һ��2mL0.01mol��L��1H2C2O4��Һ,�о���Ӧ���¶ȡ���Ӧ���Ũ������������ضԻ�ѧ��Ӧ���ʵ�Ӱ�졣�ı�����������ʾ��
��H2C2O4��H����Mn2����CO2����H2O(δ��ƽ)��4mL0.001mol��L��1KMnO4��Һ��2mL0.01mol��L��1H2C2O4��Һ,�о���Ӧ���¶ȡ���Ӧ���Ũ������������ضԻ�ѧ��Ӧ���ʵ�Ӱ�졣�ı�����������ʾ��
��� | 10%�������/mL | �¶�/�� | �������� |
�� | 2 | 20 | |
�� | 2 | 20 | 10�α���MnSO4��Һ |
�� | 2 | 30 | |
�� | 1 | 20 | 1 mL����ˮ |
(1)�÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ________��
(2)ʵ���͢�ɵó��Ľ��ۣ�Ӱ�컯ѧ��Ӧ���ʵ�������_______������о��¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ��,ʹ��ʵ����___________(����ʾ)��
(3)ʵ����м���1 mL����ˮ��Ŀ����_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݱ�������ѧ���ѳɹ��ϳ���������O4���й�O4��˵����ȷ����
A. O4��Ħ��������64 g
B. ��ͬ������O4��O3����ԭ�Ӹ���֮��Ϊ1��1
C. O4��O2��Ϊͬλ��
D. O4��O3��O2������Ԫ�ص�ͬ���칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ҵ�л�������������ˮ�������������������������ŷš�
��1����ҵ����NaHSO3��ԭ���������������£������Է�ˮ�м���NaHSO3ʹCr2O72- ��ԭ��ΪCr3+��Ȼ�������ʯ�ҵ��ڷ�ˮ��pH��ʹCr3+��ȫ������
�� д��NaHSO3��Cr2O72-��Ӧ�����ӷ���ʽ��__________________________________��
����֪25��ʱKsp[Cr(OH)3]=6.4��10-31������ȥ��ˮ��Cr3+��ʹ��Ũ��С��1��10-5 molL-1����ʱ��Һ�е�c(H+)<_________molL-1
��2����ˮ�и�Ԫ����Ũ�ȵIJⶨ�������£���һ������Cr2O72-��Cr3+�����Է�ˮ���м�������(NH4)2S2O8��Һ��Cr3+������Cr2O72-����г�ȥ������(NH4)2S2O8���ټ��������KI��Һ��Cr2O72-��I-��ȫ��Ӧ������Cr3+��I2���Ե���Ϊָʾ������Na2S2O3����Һ�ζ����յ㡣�ⶨ���������ʵ�ת����ϵ���£�Cr3+ ![]() Cr2O72-
Cr2O72- ![]() I2
I2 ![]() S4O62-
S4O62-
���������������У�������в�������ⶨ�ĸ�Ԫ����Ũ�Ȼ�________��ѡ�ƫ����ƫС�����䡱����
��ȷ��ȡ��Cr2O72-��Cr3+�����Է�ˮ��100.00 mL�������������ⶨ��ˮ���и�Ԫ����Ũ�ȣ�����0.01000 molL-1��Na2S2O3����Һ13.50 mL������÷�ˮ�и�Ԫ����Ũ�ȣ���mg��L-1��ʾ����д��������̡�_____________________________________________________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com