
【题目】某实验小组学习过氧化钠与水的反应时,向滴有酚酞的水中加入过氧化钠,发现溶液先变红后褪色,对此产生兴趣并进行研究。
(1)写出Na2O2与水反应的化学方程式:______。
(2)甲同学查阅资料:红色褪去的原因是H2O2在碱性条件下氧化了酚酞。
①甲同学通过实验证实了Na2O2与水反应所得溶液中有较多的H2O2:取少量反应所得溶液,加入试剂______(填化学式),有气体产生。
②甲同学利用3% H2O2溶液、酚酞试液、1mol·L-1 NaOH溶液,证实了碱性条件是必需的。
操作 | 现象 | |
实验1 | 向2mL 3%H2O2溶液中加入3滴酚酞试液,振荡,静置5min,再加入5滴1mol·L-1 NaOH溶液 | 观察到______。 |
(3)为了更深入地了解该原理,甲同学继续查阅资料,发现H2O2溶液中相关微粒的物质的量分数X(i)与溶液pH的关系如图所示。
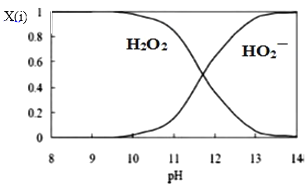
据此,甲同学设计实验2继续研究:
操作 | 现象 | |
实验2 | i.配制20mL 3%H2O2与NaOH的混合溶液,调节pH分别为10~14。 ii.滴入3滴酚酞试液,搅拌后静置,记录酚酞完全褪色的时间 | 得到如图所示实验结果:
|
甲同学由此提出假设I:溶液褪色的主要原因是酚酞被HO![]() 氧化,请结合化学反应速率和化学平衡的相关知识解释此假设:_____。
氧化,请结合化学反应速率和化学平衡的相关知识解释此假设:_____。
(4)乙同学查阅资料,发现酚酞(以H2L表示)在不同pH条件下存在多种结构之间的变化:
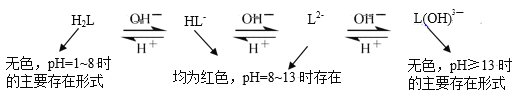
由此提出,甲同学实验2中pH13时红色褪去的原因还存在假设II:_____。
(5)针对假设I、II,小组同学设计了如下实验:
试剂加入顺序 | 现象 | |
实验3 | i.烧杯中加入10mL 2mol·L-1 NaOH溶液、8mL H2O ii.加入3滴酚酞试液 | 溶液变红,然后褪色 |
iii.搅拌、静置后加入2mL 30% H2O2溶液 | _____ | |
iv.向褪色后的溶液中加入盐酸调节pH至12 | 溶液变红,然后褪色 | |
实验4 | i.烧杯中加入10mL 2mol·L-1 NaOH溶液、8mL H2O ii.加入2mL 30% H2O2溶液 iii.搅拌、静置后加入3滴酚酞试液 | 溶液变红,然后褪色 |
iv.向褪色后的溶液中加入盐酸调节pH至12 | 不变红 |
①与L2-和HL-相比较,L(OH)![]() 比前两者更_____被氧化(填“难”或“易”)。
比前两者更_____被氧化(填“难”或“易”)。
②实验3中调节pH至12,溶液变红然后褪色的原因是:_____。
③根据实验得出结论:甲同学实验2中pH13时红色褪去的主要原因是_____(填“假设I”或“假设II”),请依据实验现象阐述理由:_____。
【答案】2Na2O2+2H2O = 4NaOH+O2↑ MnO2 红色褪色 H2O2![]() H+ + HO
H+ + HO![]() ,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO
,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO![]() 浓度增大,酚酞被HO
浓度增大,酚酞被HO![]() 氧化速率增大 溶液褪色的主要原因是酚酞以L(OH)3形式存在 溶液变红,然后褪色 难 酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO
氧化速率增大 溶液褪色的主要原因是酚酞以L(OH)3形式存在 溶液变红,然后褪色 难 酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO![]() 氧化而褪色 假设I 根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO
氧化而褪色 假设I 根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO![]() 氧化而褪色
氧化而褪色
【解析】
Na2O2与水反应生成氢氧化钠和水,反应实质是生成了双氧水,双氧水在二氧化锰催化剂作用下快速反应生成气体;溶液褪色提出假设,并对提出的假设进行用实验来验证。
⑴Na2O2与水反应生成氢氧化钠和水,其化学方程式:2Na2O2+2H2O = 4NaOH+O2↑;故答案为:2Na2O2+2H2O = 4NaOH+O2↑;
⑵①甲同学通过实验证实了Na2O2与水反应所得溶液中有较多的H2O2,利用双氧水在二氧化锰催化剂作用下迅速反应放出大量气泡,因此取少量反应所得溶液,加入试剂MnO2,有气体产生;故答案为:MnO2;
②甲同学利用3% H2O2溶液、酚酞试液、1mol·L-1 NaOH溶液,证实了碱性条件是必需的,实验1在碱性条件下反应,得到的现象为红色褪色;故答案为:红色褪色;
⑶甲同学由此提出假设I:溶液褪色的主要原因是酚酞被HO![]() 氧化,H2O2
氧化,H2O2![]() H++ HO
H++ HO![]() ,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO
,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO![]() 浓度增大,酚酞被HO
浓度增大,酚酞被HO![]() 氧化速率增大;故答案为:H2O2
氧化速率增大;故答案为:H2O2![]() H++ HO
H++ HO![]() ,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO
,加入NaOH溶液,消耗电离出的氢离子,平衡正向移动,HO![]() 浓度增大,酚酞被HO
浓度增大,酚酞被HO![]() 氧化速率增大;
氧化速率增大;
⑷由此提出,甲同学实验2中pH>13时红色褪去的原因还存在假设II:溶液褪色的主要原因是酚酞以L(OH)3形式存在;故答案为:溶液褪色的主要原因是酚酞以L(OH)3形式存在。
⑸根据实验3和实验4对比得出实验3中iii.搅拌、静置后加入2mL 30% H2O2溶液,溶液pH小于13,溶液变为红色,后酚酞被HO![]() 氧化而褪色,因此现象为溶液变红,然后褪色;故答案为:溶液变红,然后褪色;
氧化而褪色,因此现象为溶液变红,然后褪色;故答案为:溶液变红,然后褪色;
①根据实3和实验4分析,实验3中酚酞主要以L2和HL-形式存在,加双氧水,溶液变红,然后褪色,再加盐酸调节pH至12,溶液变红,然后褪色,而实验4盐酸调节pH至12,不变红,说明L(OH)![]() 比前两者更难被氧化;故答案为:难;
比前两者更难被氧化;故答案为:难;
②实验3中调节pH至12,溶液变红然后褪色的原因是:酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO![]() 氧化而褪色;故答案为:酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO
氧化而褪色;故答案为:酚酞在pH =12时,溶液由于NaOH而呈红色,后来酚酞在pH=12时被HO![]() 氧化而褪色。
氧化而褪色。
③根据实验得出结论:甲同学实验2中pH>13时红色褪去的主要原因是假设I,根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO![]() 氧化而褪色;故答案为:假设I;根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO
氧化而褪色;故答案为:假设I;根据酚酞在不同pH值的存在状态及颜色,排除pH>13酚酞以L(OH)3形式存在而褪色,则说明褪色是由于酚酞被HO![]() 氧化而褪色。
氧化而褪色。


科目:高中化学 来源: 题型:
【题目】下表中实验操作、现象以及所得出的结论都正确的是![]()
选项 | 实验操作 | 实验现象 | 实验结论 |
A | 向盛有 | 先出现白色沉淀,后出现黄色沉淀 |
|
B | 将适量 | 一支试管出现白色沉淀,另一支试管无明显现象 | 出现的白色沉淀是 |
C | 取少量 | 产生白色沉淀 |
|
D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y可能是 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3A(g)+B(g)![]() 2C(g)+3D(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g)+3D(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A.v(A)=0.9 mol·L-1·min-1B.v(B)=0.2mol·L-1·min-1
C.v(C)=0.5mol·L-1·min-1D.v(D)=1.0mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() Fe全部溶于200mL一定浓度的硝酸溶液中,得到标准状况下的气体
Fe全部溶于200mL一定浓度的硝酸溶液中,得到标准状况下的气体![]() ,又测得反应后溶液中
,又测得反应后溶液中![]() 的浓度为
的浓度为![]() 设反应前后溶液体积的变化忽略不计
设反应前后溶液体积的变化忽略不计![]() 。下列说法不正确的是
。下列说法不正确的是![]()
A.![]() 气体是NO
气体是NO
B.反应后Fe全部转化为![]()
C.反应后的溶液中![]()
D.反应后的溶液最多还能再溶解![]() Fe
Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与社会生活密切相关,下列说法正确的是( )
A.军舰船底镶嵌锌块作正极,以防船体被腐蚀
B.汽车尾气中NO和CO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢
C.金属冶炼过程是金属离子得电子变成金属单质的氧化过程
D.PM2.5颗粒![]() 微粒直径约为2.5×106m)分散在空气中形成气溶胶
微粒直径约为2.5×106m)分散在空气中形成气溶胶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组探究![]() 气体还原
气体还原![]() 、
、![]() ,他们使用的药品和装置如图所示,下列说法正确的是()
,他们使用的药品和装置如图所示,下列说法正确的是()
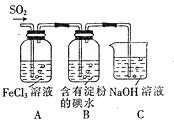
A.![]() 是
是![]() 气体与
气体与![]() 反应的还原产物
反应的还原产物
B.装置C烧杯中加入少量苯可以防止倒吸
C.表明![]() 的还原性弱于
的还原性弱于![]() 的现象是B中溶液蓝色褪色
的现象是B中溶液蓝色褪色
D.在A中的溶液加入![]() 溶液,则紫红色褪去说明A中
溶液,则紫红色褪去说明A中![]() 与
与![]() 发生了氧化还原反应
发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某烷烃![]() 与烯烃
与烯烃![]() 的混合气体
的混合气体![]() ,其密度为同状况下
,其密度为同状况下![]() 密度的11.2倍,将混合气体通过足量的溴水,溴水增重
密度的11.2倍,将混合气体通过足量的溴水,溴水增重![]() ,回答下列问题:
,回答下列问题:
(1)写出结构简式:![]() ________,
________,![]() ________。
________。
(2)![]() 与丁烯互为________(填“同分异构体”或“同系物”)。
与丁烯互为________(填“同分异构体”或“同系物”)。
(3)写出![]() 与溴水反应的化学方程式:________________。
与溴水反应的化学方程式:________________。
(4)下列有关![]() 的结构或性质的说法正确的是________(填序号)。
的结构或性质的说法正确的是________(填序号)。
A 不能使酸性高锰酸钾溶液褪色,但能使溴的四氯化碳溶液褪色
B 分子中所有原子都在同一平面上
C 分子中有7个单键
D 与![]() 在一定条件下能加成并只得到一种产物
在一定条件下能加成并只得到一种产物
Ⅱ.(5)已知甲苯(![]() )能使酸性
)能使酸性![]() 溶液褪色。某有机物的结构简式为
溶液褪色。某有机物的结构简式为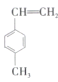 ,下列说法正确的是________(填序号)。
,下列说法正确的是________(填序号)。
A 该有机物使溴水褪色和在催化剂作用下与液溴反应原理一样
B 能用酸性![]() 溶液判断分子中存在碳碳双键
溶液判断分子中存在碳碳双键
C 该有机物在一定条件下与浓硝酸发生反应生成的苯环上的一硝基取代物可能有3种
D ![]() 该有机物在一定条件下最多与
该有机物在一定条件下最多与![]() 发生加成反应
发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有室温下四种溶液,有关叙述不正确的是
编号 | ① | ② | ③ | ④ |
pH | 10 | 10 | 4 | 4 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
A.相同体积③、④溶液分别与 NaOH 完全反应,消耗 NaOH 物质的量:③>④
B.分别加水稀释 10 倍,四种溶液的 pH:①>②>④>③
C.①、④两溶液等体积混合,所得溶液中 c(![]() )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
D.在③溶液中:c(H+)=c(CH3COO-)+c(CH3COOH)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两套实验装置中进行的实验都涉及金属的腐蚀,假设其中的金属块和金属丝都是足量的。下列叙述正确的是( )
Ⅰ Ⅱ
Ⅱ 
A.装置Ⅰ在反应过程中只生成NO2气体
B.装置Ⅱ在开始阶段铁丝只发生析氢腐蚀
C.装置Ⅱ在反应过程中能产生氢气
D.装置Ⅰ在反应结束时溶液中的金属阳离子只有Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com