
【题目】有如图所示A、B、C、D、E五种仪器:
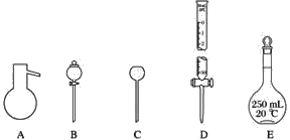
(1)请选择下列仪器名称的序号,填入相应的横线上:
①蒸馏烧瓶 ②碱式滴定管 ③圆底烧瓶 ④长颈漏斗⑤分液漏斗 ⑥酸式滴定管 ⑦容量瓶
A:__________,B:__________,C:__________,D:________,E:________。
(2)上述A~E五种仪器中,使用前必须检漏的有________,组装气体发生器必须液封的是________。
(3)下列仪器中,
![]()
在灼烧固体物质时必须用到的仪器是________________(填名称)。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的原子结构示意图为___________。
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为__________________。
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子。
①Z与H2O2反应,其产物之一是Y的单质,Y的单质的电子式为_____________;Z分子的结构呈____________;
②A的化学式是_____________;
(4)X的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭和导弹上有重要应用),其反应的化学方程式是
____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A. 苯和氯气生成C6H6Cl6的反应是取代反应
B. 乙烯与溴水发生加成反应的产物是CH2CH2Br2
C. 等物质的量的甲烷与氯气反应的产物是CH3Cl
D. 硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要配制0.50 mol·L-1NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、玻璃棒、________、________以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体________g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:

②称量过程中NaCl晶体应放于天平的________(填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是_________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_____________。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.34 g Cu和CuO的混合物加入约12 mol·L-1浓硫酸中,并加热使其完全溶解,然后用NaOH溶液中和过量硫酸,再用水稀释到0.5 L,加入纯铁粉1.85 g,反应后过滤、干燥,得不溶物1.89 g。求置换出的铜的质量及原混合物中铜的质量分数___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法错误的是( )
A. c(H+)为1.0×10-4mol·L-1的醋酸溶液的pH=4
B. 0.1 mol·L-1某酸溶液的pH=1
C. 0.01 mol·L-1氨水的pH<12
D. pH=3的醋酸溶液的浓度大于1.0×10-3mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-)。室温下,将稀盐酸滴加到某一元碱(BOH)溶液中,测得混合溶液的pOH 与微粒浓度的变化关系如图所示。 下列说法错误的是( )

A.若向0.1mol/L BOH溶液中加水稀释,则溶液中c(OH-)/c(BOH) 增大
B.室温下,BOH的电离平衡常数K = 1×10-4.8
C.P点所示的溶液中:c(Cl-) > c(B+)
D.N点所示的溶液中: c(H+) = c(Cl-) + c(OH-) - c(BOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com