
【题目】铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
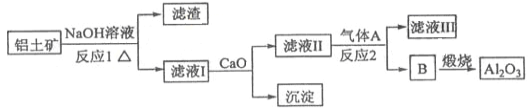
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
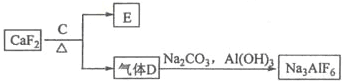
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:
回答下列问题:
(1)写出反应1的化学方程式__________________________;
(2)滤液Ⅰ中加入CaO生成的沉淀是____________,反应2的离子方程式为____________________;
(3)E可作为建筑材料,化合物C是__________,写出由D制备冰晶石的化学方程式____________;
(4)电解制铝的化学方程式是__________________,以石墨为电极,阳极产生的混合气体的成分是__________________。
【答案】(1)2NaOH+SiO2=Na2SiO3+H2O(2分),2NaOH+Al2O3=2NaAlO2+H2O(2分)
(2)硅酸钙沉淀(2分)2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
(3)浓H2SO4;(2分)12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+3CO2+9H2O(2分)
(4)2Al2O3(熔融)![]() 4Al+3O2↑(2分) O2、CO2(或CO)
4Al+3O2↑(2分) O2、CO2(或CO)
【解析】
试题分析:(1)二氧化硅与氢氧化钠反应生成硅酸钠与水,反应方程式为2NaOH+SiO2=Na2SiO3+H2O,氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应方程式为2NaOH+Al2O3=2NaAlO2+H2O。
(2)滤液Ⅰ中含有硅酸钠、偏铝酸钠,加入CaO,生成氢氧化钙,氢氧化钙与硅酸钠反应生成硅酸钙沉淀;由工艺流程可知,B为氢氧化铝,气体A为二氧化碳,滤液Ⅱ主要是偏铝酸钠,偏铝酸钠溶液通入二氧化碳,生成氢氧化铝与碳酸钠,反应方程式为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-。
(3)由工艺流程可知,气体D含有F元素,应是HF,C为浓硫酸;根据元素守恒可知,HF与碳酸钠、氢氧化铝反应生成冰晶石,同时生成二氧化碳、水,反应方程式为12HF+3Na2CO3+2Al(OH)3=2Na3AlF6+ 3CO2+9H2O;
(4)电解熔融的氧化铝生成铝与氧气,反应方程式为2Al2O3(熔融)![]() 4Al+3O2↑,阳极生成氧气,部分氧气可以石墨反应生成二氧化碳、CO,阳极气体有O2、CO2(或CO)。
4Al+3O2↑,阳极生成氧气,部分氧气可以石墨反应生成二氧化碳、CO,阳极气体有O2、CO2(或CO)。


科目:高中化学 来源: 题型:
【题目】已知某种微生物燃料电池工作原理如图所示。下列有关该电池的说法中,正确的是

A.外电路电子从B极移向A极[来
B.溶液中H+由B极区移向A极区
C.电池工作一段时间后B极区溶液的pH减小[
D.A极电极反应式为:CH3COOH - 8e-+ 2H2O = 2CO2 + 8H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2。符合上述转化关系的A、C可能是

①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2
A.只有②③④⑥ B.除①外 C.除⑤外 D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1983年,福瑞堡大学的普林巴克(Prinzbach),合成多环有机分子。如右图的多环有机分子,因其形状像东方塔式庙宇,所以该分子也就称为pagodane(庙宇烷),有关该分子的说法不正确的是( )
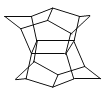
A.分子式为C20H20
B.一氯代物的同分异构体只有两种
C.分子中含有4个亚甲基(—CH2—)
D.分子中含有12个五元碳环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C6H14的各种同分异构体中所含甲基数和它的一氯代物的数目分别是( )[
A.2个甲基,可能生成4种一氯代物
B.3个甲基,可能生成3种一氯代物
C.3个甲基,可能生成5种一氯代物
D.4个甲基,可能生成4种一氯代物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 人的血红蛋白由4条(α、α、β、β)多肽链组成,其中每条α链含氨基酸141个,每条β链含氨基酸146个,则血红蛋白含肽键 ( )
A. 283个 B. 285个 C. 286个 D. 570个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁是常见的水处理剂,工业上制备无水FeCl3的一种工艺如下:
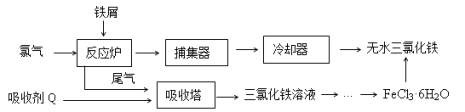
(1)由FeCl3· 6H2O晶体制备无水FeCl3应采取的措施是: 。
(2)六水合氯化铁在水中的溶解度如下:
温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
从FeCl3溶液制得FeCl3·6H2O晶体的操作步骤是:加入少量盐酸、 、 、过滤、洗涤、干燥。
(3)常温下,若溶液的pH控制不当会使Fe3+沉淀,pH=4时,溶液中c(Fe3+)= mol·L-1。(常温下Ksp[Fe(OH)3]=2.6×10-39)。
(4)FeCl3的质量分数通常可用碘量法测定:称取2.300g无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入某一指示剂并用0.1000mol·L-1Na2S2O3溶液滴定用去12.50mL。
已知:I2+2S2O32-=2I-+S4O62-
① 写出加入稍过量的KI溶液反应的离子方程式: 。
② 求样品中氯化铁的质量分数(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com