
【题目】有机物种类繁多,请以你对有机物的认识填空:
(1)下列几组物质中,互为同位素的是__,互为同素异形体的是__,互为同系物的是___,互为同分异构体的是___。
①O2和O3;②35Cl和37Cl;③CH3CH3和CH3CH2CH3;④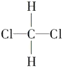 和
和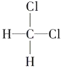 ;⑤CH3(CH2)2CH3和(CH3)2CHCH3;⑥
;⑤CH3(CH2)2CH3和(CH3)2CHCH3;⑥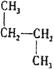 和
和![]() ;⑦
;⑦![]() 和CH3(CH2)3CH3;
和CH3(CH2)3CH3;
(2)下列各烷烃的沸点由高到低的顺序为___(用字母表示)
A.正戊烷 B.异戊烷 C.CH3(CH2)2CH3 D.新戊烷 E.C3H8
(3)聚乙烯可用于制造食品包装袋,由乙烯制备聚乙烯的化学方程式为___。
(4)丙烯中处于同一平面的原子最多有___个,丙烯使溴水褪色,其化学方程式为___,该反应的类型是___。
(5)1mol某烷烃完全燃烧时消耗氧气的物质的量为11mol,其化学式为___,其结构中含有3个-CH3的结构简式分别为:___。
【答案】② ① ③ ⑤⑦ ABDCE nCH2=CH2![]()
![]() 7 CH3CH=CH2+Br2→CH3CHBrCH2Br 加成反应 C7H16 CH3CH2CH(CH3)CH2CH2CH3、CH3CH(CH3)CH2CH2CH2CH3、(CH3CH2)2CHCH2CH3
7 CH3CH=CH2+Br2→CH3CHBrCH2Br 加成反应 C7H16 CH3CH2CH(CH3)CH2CH2CH3、CH3CH(CH3)CH2CH2CH2CH3、(CH3CH2)2CHCH2CH3
【解析】
(1)同种元素的不同核素互为同位素,所以35Cl和37Cl互为同位素,选②;
同种元素的不同单质互为同素异形体,所以O2和O3互为同素异形体,选①;
结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物,CH3CH3和CH3CH2CH3结构相似,分子组成相差一个CH2二者互为同系物,选③;
分子式相同,结构不同的化合物互为同分异构体,CH3(CH2)2CH3和(CH3)2CHCH3分子式均为C4H10,结构不同互为同分异构体;![]() 和CH3(CH2)3CH3分子式均为C5H12,结构不同互为同分异构体,所以选⑤⑦;
和CH3(CH2)3CH3分子式均为C5H12,结构不同互为同分异构体,所以选⑤⑦;
(2)随着相对分子质量的增大,分子间的范德华引力增大,所以烷烃的沸点随着相对分子质量的增加而升高,对于含碳数相同的烷烃而言,支链越多,沸点越低;则五种物质的沸点由高到低的顺序为ABDCE;
(3)乙烯发生加聚反应生成聚乙烯,化学方程式为nCH2=CH2![]()
![]() ;
;
(4)丙烯的结构简式为CH3CH=CH2,乙烯为平面结构,丙烯即乙烯中一个氢原子被甲基代替,则甲基上的碳原子可共面,根据甲烷的空间结构可知甲基上最多还有1个氢原子可共面,所以最多7个原子共面;丙烯含有碳碳双键可以和溴发生加成反应使溴水褪色,化学方程式为CH3CH=CH2+Br2→CH3CHBrCH2Br;
(5)烷烃的通式为CnH2n+2,根据元素守恒可知1mol烷烃燃烧消耗的氧气的物质的量为(n+![]() )=11mol,解得n=7,所以该烷烃的化学式为C7H16;其结构中含有3个-CH3的结构简式分别为CH3CH2CH(CH3)CH2CH2CH3、CH3CH(CH3)CH2CH2CH2CH3、(CH3CH2)2CHCH2CH3。
)=11mol,解得n=7,所以该烷烃的化学式为C7H16;其结构中含有3个-CH3的结构简式分别为CH3CH2CH(CH3)CH2CH2CH3、CH3CH(CH3)CH2CH2CH2CH3、(CH3CH2)2CHCH2CH3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图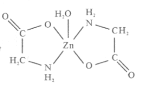 。
。
(1)基态Zn2+的价电子排布式为_______________;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的顺序是___________________。
(2)甘氨酸(H2N-CH2-COOH)中N的杂化轨道类型为______________;甘氨酸易溶于水,试从结构角度解释___________________________________________。
(3)一水合甘氨酸锌中Zn2+的配位数为______________________。
(4) [Zn(IMI)4](ClO4)2是Zn2+的另一种配合物,IMI的结构为![]() ,则1 mol IMI中含有________个σ键。
,则1 mol IMI中含有________个σ键。
(5)常温下IMI的某种衍生物与甘氨酸形成的离子化合物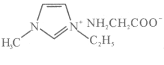 为液态而非固态,原因是________________________________________。
为液态而非固态,原因是________________________________________。
(6)Zn与S形成某种化合物的晶胞如图Ⅰ所示。
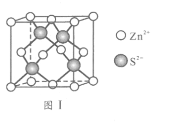
①Zn2+填入S2-组成的________________空隙中;
②由①能否判断出S2- 、Zn2+相切?_________(填“能”或“否”);已知晶体密度为d g/cm3,S2-半径为a pm,若要使S2-、Zn2+相切,则Zn2+半径为____________________pm(写计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,体积均为20mL、浓度均为0.1mol·L-1的两种酸HX、HY分别与0.1mol·L-1的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是( )
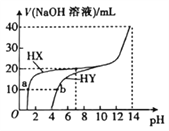
A. Ka(HY)的数量级约为10-3
B. a点c(X-)>b点c(Y-)
C. HX发生反应的离子方程式为HX+OH-=X-+H2O
D. pH=7时,两种反应后的溶液中c(Y-)>c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
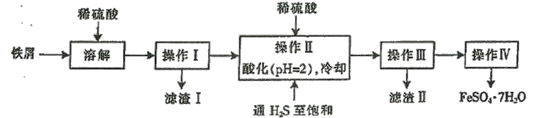
已知:室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6,FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。根据以上流程图,下列说法不正确的是
A.操作I所得滤液中不含有Fe3+
B.操作Ⅱ中用硫酸酸化至pH=2的主要目的是抑制Fe2+的水解
C.操作Ⅱ中,通入H2S至饱和的目的是使Sn2+转化为SnS沉淀并防止Fe2+被氧化。
D.操作Ⅳ中所得的晶体最后用乙醇洗去晶体表面附着的水分。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4·7H2O广泛用于医药和工业领域,实验室制备FeSO4·7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_________。
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;②_____________________。
(3)FeSO4·7H2O是某些补血剂的主要成分,将1.5 g某补血剂预处理,配成100mL溶液。实验室用KMnO4溶液通过氧化还原滴定测定该补血剂(1.5 g)中铁元素的含量,①配制100 mL 1.200 × 10—2 mol·L—1的KMnO4溶液时,将溶解后的溶液转移至容量瓶中的操作方法是__________________________;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是_________________。
a. 稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在__________滴定管中。滴定到终点时的现象为____________。
③滴定完毕,三次实验记录KMnO4标准溶液的读数如下。
滴定次数实验数据 | 1 | 2 | 3 |
V(样品)/mL | 20.00 | 20.00 | 20.00 |
V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
该补血剂中铁元素的质量分数为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体, 一定条件下发生如下反应: 3A(g) ![]() B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )

A. 若 t1=15 s,则用 A 的浓度变化表示 t0~t1阶段的平均反应速率为 0.004 mol·L-1·s-1
B. t1时该反应达到平衡, A 的转化率为 60%
C. 该容器的容积为2 L,B的起始的物质的量为 0.02 mol
D. t0~t1 阶段, 此过程中容器与外界的热交换总量为 a kJ,该反应的热化学方程式为 3A(g)![]() B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)PCl5(g)。5min末达到平衡,有关数据如表。
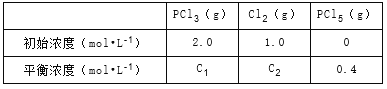
下列判断不正确的是( )
A.若升高温度,反应的平衡常数减小,则正反应为吸热
B.反应5min内,v(PCl3)=0.08molL-1min-1
C.当容器中Cl2为1.2mol时,可逆反应达到平衡状态
D.平衡后移走2.0molPCl3和1.0molCl2,在相同条件下再达平衡时,c(PCl5)<0.2molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,A、B 两种气体反应生成 C 气体。反应过程中 A、B、C 浓度变化如图(I)所示 , 若保持其他条件不变,温度分别为 T1和 T2时,B 的体积分数与时间的关系如图(II)所示 ,则下列结论正确的是 ( )

A.该反应的热化学方程式 A(g)+2B(g)=2C(g)△H= -285.84kJmol-1
B.该反应中 T1<T2
C.其他条件不变,升高温度,正、逆反应速率均增大,且 A 的转化率增大
D.T℃时,在相同容器中,若由 0.3 mol/L A、0.1 mol/L B 和 0.4 mol/L C 反 应,达到平衡后,C 的浓度仍为 0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10﹣4molL﹣1 | K1=4.4×10﹣6molL﹣1 K2=5.6×10﹣11molL﹣1 | 3.0×10﹣8 molL﹣1 |
请回答下列问题:
(1)同浓度的CH3COOH、H2CO3、HClO溶液的pH最大的是_____.
(2)常温下0.1molL﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_____(填字母序号,下同).
A.c(H+)
B.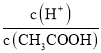
C.c(H+)c(OH﹣)
D.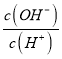
E.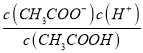
若该溶液升高温度,上述5种表达式的数据增大的是_________.
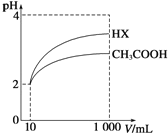
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数_____(填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中有水电离出来的c(H+)_____(填“大于”、“等于”或“小于”)醋酸的溶液中有水电离出来的c(H+),理由是___________.
(4)已知100℃时,水的离子积为1×10﹣12,该温度下测得某溶液PH=7,该溶液显_____(填“酸”、“碱”或“中”)性.将此温度下PH=1的H2SO4溶液aL与PH=11的NaOH溶液bL混合,若所得混合液PH=2,则a:b=_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com