
����Ŀ���������������ʵ���Һ����Na2CO3 ��Al2(SO4)3 ��CH3COOH ��NaHCO3 ��HCl ��Al(OH)3
(1)pHֵ��ͬ�����������ֱ�������ˮϡ����ԭ����![]() ����
����![]() ����ϡ�ͺ�����Һ��
����ϡ�ͺ�����Һ��![]() ֵ��Ȼ��ͬ����
ֵ��Ȼ��ͬ����![]() ______
______![]() (����<������>������=��)
(����<������>������=��)
(2)�����£�![]() ֵΪ11������Һ�У���ˮ���������c(OH��)=______
ֵΪ11������Һ�У���ˮ���������c(OH��)=______
(3)д������Һ�ĵ���غ㣺____________��
(4)д��������ʽ���뷽��ʽ��________________
(5)������������Һ����������ĭ��������ԭ��Ϊ��________________(�����ӷ���ʽ����)
(6)��֪��ӦNH4��+HCO3��+H2ONH3��H2O+H2CO3���÷�Ӧƽ�ⳣ��K=_____��(��֪������NH3��H2O�ĵ���ƽ�ⳣ��Kb=2��10-5��H2CO3�ĵ���ƽ�ⳣ��Ka1=4��10-7��Ka2=4��10-11)
���𰸡�> 0.001 mol/L c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) Al(OH)3AlO2��+ H+ +H2O Al3+ +3HCO3- =Al(OH)3�� +3CO2�� 1.25��10-3
��������
(1)![]() ��ͬ��ǿ�������ϡ�ͺ�
��ͬ��ǿ�������ϡ�ͺ�![]() ֵ��Ȼ��ͬ������ϡ�͵ı�������
ֵ��Ȼ��ͬ������ϡ�͵ı�������
(2) Na2CO3Ϊǿ�������Σ���Һ�е�����������������ˮ��ˮ�������������������������Ũ����ȣ�
(3)������ҺΪ�����ԣ��������������ӵĵ��������ȣ�
(4)��������Ϊ������������ݴ˷�����
(5) Al2(SO4)3 ��NaHCO3��Ϻ���˫ˮ�⣻
(6)���ݷ�ӦNH4��+HCO3��+H2ONH3��H2O+H2CO3��ƽ�ⳣ������ʽ��ʽ���㣻
(1)CH3COOH ΪһԪ���ᣬHCl ΪһԪǿ�ᣬ![]() ��ͬ��һԪǿ���һԪ����ϡ�ͺ�
��ͬ��һԪǿ���һԪ����ϡ�ͺ�![]() ֵ��Ȼ��ͬ����ϡ�ͺ���Һ��������Ũ����ͬ��ǿ��ϡ�ͺ�������Ũ�ȱ������С�ĸ��࣬Ҫʹ������Ũ����ͬ��������ϡ�͵ı���������M��N��
ֵ��Ȼ��ͬ����ϡ�ͺ���Һ��������Ũ����ͬ��ǿ��ϡ�ͺ�������Ũ�ȱ������С�ĸ��࣬Ҫʹ������Ũ����ͬ��������ϡ�͵ı���������M��N��
(2)�����£�![]() =11��Na2CO3��Һ��c(H+)=10-11mol/L��Na2CO3��ˮ�з���ˮ�ⷴӦ������ˮ�е������ӣ���Һ��c(OH-)=
=11��Na2CO3��Һ��c(H+)=10-11mol/L��Na2CO3��ˮ�з���ˮ�ⷴӦ������ˮ�е������ӣ���Һ��c(OH-)=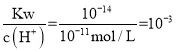 mol/L����Һ�е�����������������ˮ������ˮ���������c(OH-)= 0.001 mol/L��
mol/L����Һ�е�����������������ˮ������ˮ���������c(OH-)= 0.001 mol/L��
(3) Na2CO3��Һ�к��У�Na+��H+��HCO3-��CO32-��OH-����ҺΪ�����ԣ������غ�ʽΪ��c(Na+)+c(H+)==c(HCO3-)+2c(CO32-)+c(OH-)��
(4)��������Ϊ�������������ʽ���뷽��ʽΪ��Al(OH)3AlO2-+H++H2O��
(5) Al2(SO4)3 ��NaHCO3��Ϻ���˫ˮ�ⷴӦ�������������Ͷ�����̼����Ӧԭ��Ϊ��Al3+ +3HCO3- =Al(OH)3�� +3CO2����
(6)��֪��ӦNH4��+HCO3��+H2ONH3��H2O+H2CO3���÷�Ӧƽ�ⳣ��K= 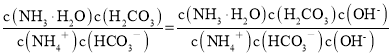 =
=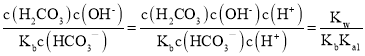 =
=![]() =1.25��10-3��
=1.25��10-3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��������������������˵��������ȷ���ǣ� ����
A.������������������Һ���к��Ȳⶨ��ʵ������У�������Ҫ�ⶨ����¼�¶ȵĴ�����3��
B.������ͭ�����нᾧˮ�����ⶨ��ʵ���У���ʵ����������ٳ���4��
C.��ij�л�������к�n����CH2����m��![]() ��a����CH3������Ϊ�ǻ������ǻ��ĸ������Ϊm - a + 2
��a����CH3������Ϊ�ǻ������ǻ��ĸ������Ϊm - a + 2
D.���л���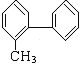 �����д���ͬһƽ���ڵ�̼ԭ���������13��
�����д���ͬһƽ���ڵ�̼ԭ���������13��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������̿�(��Ҫ�ɷ�ΪMnO2������������FeCO3��Al2O3��SiO2)Ϊԭ����ȡ�����̵Ĺ����������£�
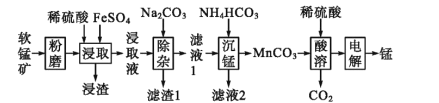
(1)д��������������Ҫ�ɷֵ���; ________(д������)��
(2)����1����Ҫ�ɷ��� ________(�û�ѧʽ��ʾ)
(3)���������ȡҺ������Fe2+������ȡ��ʱMnO 2������Ӧ�����ӷ���ʽΪ ________��
(4)д���������������з�����Ӧ�����ӷ���ʽ��________��
(5)���������������Һ��Ϊ���Һ������ͼ1װ�õ�⣬Ӧ���� ______(����������������)���ӽ���Ĥ�������ĵ缫��ӦʽΪ________��
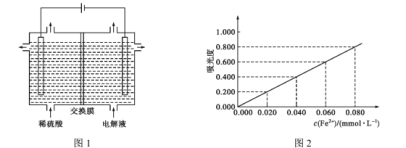
(6)Ϊ�������������1������ⶨ��������Ԫ�صĺ�����������·�����
�ٽ�ag����������xmL��Һ��
��ȡ����������Һ��EDTA�ζ������Һ��Fe3+ ��Al3+ ��Ũ��֮��Ϊymmol��L��1 ��
����ȡ����������Һ��Fe3+ �������ǰ�(����Һ�п���ȫ�����NH3OH+��Cl�� )��ԭΪFe2+�����ӷ���ʽΪ ________��
�ܽ���������Һ��������ȷ�����������Ϊ0.400(�������Fe2+��Ũ�ȹ�ϵ����ͼ2��ʾ)������Ʒ����Ԫ�ص���������Ϊ _________(�ú���ĸ�ı���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ2A(s)��3B(g) ![]() C(g)��2D(g)����H��0����һ�������´ﵽƽ�⣬�����й�������ȷ����
C(g)��2D(g)����H��0����һ�������´ﵽƽ�⣬�����й�������ȷ����
������A������ƽ��������Ӧ�����ƶ�
�������¶ȣ���Ӧ��������ƽ�����淴Ӧ�����ƶ�
��ѹ����������ѹǿ��ƽ�ⲻ�ƶ��������ܶȲ���
�ܺ��º�ѹʱ������������壬ƽ�ⲻ�ƶ�
�ݼ��������B��ƽ��ת�������
A.�٢�B.��C.�٢�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ������ѧ�������ڿ�������ӵ�ط�������Խ������λ��ѧ�ҡ�����ӵ�صĹ㷺Ӧ��Ҫ������ط����Խ�Լ��Դ����������������ʪ��ұ���ջ��շϾ���������﮵������Ƭ(��Al����LiFePO4���Բ��ϡ��������������ĵ�������)�е���Դ������������ͼ��
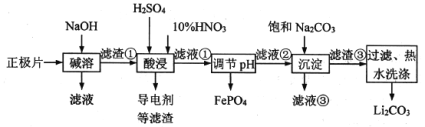
��֪��Ksp(Li2CO3)��1.6��10��3���������ʵ��ܽ��(S)�����ʾ��
T/�� | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g | S(LiH2PO4)/g |
20 | 1.33 | 34.2 | 0.039 | 126 |
80 | 0.85 | 30.5 | ���� | ���� |
(1)�����յķϾ�����ӵ�ؽ���Ԥ�ŵ硢������顢�ȴ�����Ԥ������ɸ�ֺ�������Ƭ�����з�������Ϊ��������__________��
A.�Ͼ�����ӵ���ڴ���֮ǰ��Ҫ���г��ŵ磬�����ں��������У�����������Ἧ���ͷţ����ܻ���ɰ�ȫ������
B.Ԥ�ŵ�ʱ����е�������������������������Ƭ���Ԫ�صĻ����ʡ�
C.�ȴ������̿��Գ�ȥ�Ͼ�����ӵ���е������л��̼�۵ȡ�
(2)д������ʱ��Ҫ������Ӧ�����ӷ���ʽ��________��
(3)Ϊ�������Ľ����ʣ������顢���衢�����⣬���ɲ��õķ�����______��(д��һ�ּ���)
(4)���ʱ���������3.36 L NOʱ���ܽ�LiFePO4________mol(�������ʲ���HNO3��Ӧ)��
(5)����Һ����c(Li��)��4 mol��L��1������������Na2CO3�����е�LiԪ��ռԭLiԪ��������90%��������Һ����c(CO32��)��__________mol/L��
(6)������������ˮϴ������ԭ����________��
(7)��ҵ�Ͻ����յ�Li2CO3��FePO4����������̿�ڻ�ϸ������������Ʊ�LiFePO4��д����Ӧ�Ļ�ѧ����ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����84����Һ����1984�걱��ijҽԺ����ʹ�ö����������ճ�������ʹ�ù㷺������Ч�ɷ���NaClO��ij��ѧ�о���ѧϰС����ʵ�����Ʊ�NaClO��Һ������������̽���ͳɷֲⶨ��
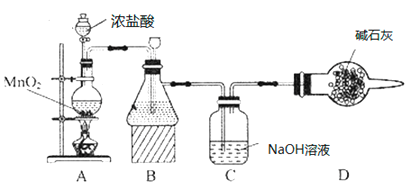
(1)��ѧϰС�鰴��ͼװ�ý���ʵ��(���ּг�װ��ʡȥ)����Ӧһ��ʱ��ֱ�ȡB��Cƿ�е���Һ����ʵ�飬ʵ���������±���
ʵ�鲽�� | ʵ������ | |
Bƿ | Cƿ | |
ʵ��1��ȡ�����μ���ɫʯ����Һ | ��죬����ɫ | ����������ɫ |
ʵ��2���ⶨ��Һ��pH | 3 | 12 |
��֪���ٱ���NaClO��ҺpHΪ11����25��Cʱ��������볣��Ϊ��H2CO3��K1=4.4��10-7��K2=4.7��10-11��HClO��K=3��10-8���ش��������⣺
��װ��Bʢװ���Լ���___________��װ��A�з�����Ӧ�����ӷ���ʽ__________��
��Cƿ��Һ�е�������NaCl��__________(�ѧʽ)��
������Cƿ��Һ����NaHCO3��Һ�������������������ʵ�飬Cƿ����Ϊ��ʵ��1����ɫʯ����Һ������ɫ��ʵ��2��Cƿ��Һ��pH=7�����ƽ���ƶ�ԭ��������ɫʯ����Һ������ɫ��ԭ��______
(2)�ⶨCƿ��Һ��NaClO����(��λ��g/L)��ʵ�鲽�����£�
��.ȡCƿ��Һ20mL����ƿ�У����������ữ���������KI��Һ���ǽ�ƿ�����ڰ�����ַ�Ӧ��
��.��0.1000mol/LNa2S2O3����Һ�ζ���ƿ�е���Һ��������Һ��ʾ�յ���ظ�����2��3�Σ�Na2S2O3��Һ��ƽ������Ϊ24.00mL��(��֪��I2+2S2O32-=2I-+S4O62-)
�ٲ���I����ƿ�з�����Ӧ�����ӷ���ʽΪ_________��
�ڵζ����յ������_____________��
��Cƿ��Һ��NaClO����Ϊ______g/L(����2λС��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɼ״��������ѵ����ȼ�ϡ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
��CH4(g)��H2O(g)![]() CO(g)��3H2(g) ��H1����206.1 kJ/mol
CO(g)��3H2(g) ��H1����206.1 kJ/mol
��CH4(g)��CO2(g)![]() 2CO(g)��2H2(g) ��H2����247.3 kJ/mol
2CO(g)��2H2(g) ��H2����247.3 kJ/mol
��CO(g)��H2O(g)![]() CO2(g)��H2(g) ��H3
CO2(g)��H2(g) ��H3
��ش��������⣺
(1)��һ�ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ��ʾ��

��Ӧǰ5min��ƽ����Ӧ����v(H2)��______��10minʱ���ı���������������_______(�����)��
A.ѹ����� B.������� C.�����¶� D.�������
(2)��ͼ��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䡣
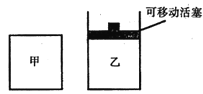
��֪��������CH4��ת������ʱ��仯��ͼ����ͼ��ʾ������ͼ�л�����������CH4��ת������ʱ��仯��ͼ��_______��
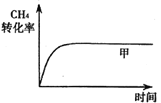
(3)��Ӧ���С�H3��________��800��ʱ����Ӧ�۵Ļ�ѧƽ�ⳣ��K��1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ���������
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
��ʱ��Ӧ���������淴Ӧ���ʵĹ�ϵʽ��________(�����)��
a.v(��)>v(��) b.v(��)<v(��) c.v(��)��v(��) d.���ж�
(4)800Kʱ�����������ܱ������и�����2 mol H2��1 mol CO��������Ӧ��2H2(g)��CO(g)CH3OH(g) ��H<0������������ʼ�����ͬ���������ڷ�Ӧ�����б���ѹǿ���䣬����������������䣬������ά�־��ȣ����������Խ�����ѧƽ�⡣
��. ��.
��. ��.
��.
�ٴﵽƽ��ʱ��ƽ�ⳣ��K(��)________K(��)��K(��)________K(��)(������������������������)��
�ڴﵽƽ��ʱH2��Ũ��c(H2)(��)________c(H2)(��)��c(H2)(��)________c(H2)(��)(������������������������)��
(5)���Լ״�Ϊȼ�ϵĵ���У��������ҺΪ���ԣ������ĵ缫��ӦʽΪ_________���״�Ӧ����ȼ�ϵ�رȼ״�ֱ������ȼ��ȼ�յ��ŵ���_______(�ش�һ������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(�۵�660��)��һ��Ӧ�ù㷺�Ľ�������ҵ����![]() (�۵�2045��)�ͱ���ʯ(
(�۵�2045��)�ͱ���ʯ(![]() )������ں����Ƶá���ش��������⣺
)������ں����Ƶá���ش��������⣺
(1)�����ڻ��ý���ȴ���ڿ������ȶ����ڣ���ԭ����__________��ұ��ҵ�ϳ��ý���������ԭ��ұ�����������̵Ƚ�������д������V2O5�ڸ����·�Ӧ�Ļ�ѧ����ʽ��___________��
(2)��![]() Һ��
Һ��![]() ��Һ�����ȡ
��Һ�����ȡ![]() ����ʵ������ʢװNaF��Һ���Լ�ƿ_________(������������������)�ò���ƿ��ԭ����_______��
����ʵ������ʢװNaF��Һ���Լ�ƿ_________(������������������)�ò���ƿ��ԭ����_______��
(3)���й�����Ԫ�ص���������ȷ����__________(�����)��
A.������������ʹ�õĽ���
B.þ���Ͻ�ȿ���ȫ���ڹ��������ᣬ�ֿ���ȫ���ڹ�����NaOH��Һ
C.����������һ���������������������������������NaOH��Һ
D.��������������Ԫ��֮һ�����������������Ӧ����ʹ�����ƴ��ߺͲ;߸����������彡��
(4)ij�����ŷų��ж�����NOCl������ˮ�ͻ�����![]() ��NOCl�����и�ԭ�Ӿ�����8�����ȶ��ṹ����NOCl�ĵ���ʽΪ_________��ˮԴ�е�
��NOCl�����и�ԭ�Ӿ�����8�����ȶ��ṹ����NOCl�ĵ���ʽΪ_________��ˮԴ�е�![]() �����ཡ�������Σ����Ϊ�˽���ˮԴ��
�����ཡ�������Σ����Ϊ�˽���ˮԴ��![]() ��Ũ�ȣ����о���Ա�����ڼ��������������۽�
��Ũ�ȣ����о���Ա�����ڼ��������������۽�![]() ��ԭΪN2����ʱ����Ҫ��
��ԭΪN2����ʱ����Ҫ��![]() ����ʽ��������Һ�У���д���÷�Ӧ�����ӷ���ʽ��__________�����÷�Ӧת��5mol����ʱ��������
����ʽ��������Һ�У���д���÷�Ӧ�����ӷ���ʽ��__________�����÷�Ӧת��5mol����ʱ��������![]() �ڱ���µ����ԼΪ_______L��
�ڱ���µ����ԼΪ_______L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������0.1000mol��L-1NaOH��Һ�ζ�20.00mL0.1000mol��L-1HCl��ҺΪ��������ǿ��ζ�ǿ��������ͨ����������±�(��֪��lg2��0.3��lg5��0.7����Һ���ʱ������仯���Բ���)��
����NaOH��Һ�����V/mL | 0.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
ʣ��������Һ�����V/mL | 20.00 | 2.00 | 0.20 | 0.02 | 0.00 | / | / | / | / |
����NaOH��Һ�����V/mL | / | / | / | / | / | 0.02 | 0.20 | 2.00 | 20.00 |
pH | 1.00 | 2.28 | 3.30 | __ | 7.00 | 9.70 | __ | 11.70 | 12.50 |
��1�������ñ������ݻ��Ƶζ�����_____��
��2�������������ĩ������ͼ��ʾ���ζ�Һ������Ϊ__mL��

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com