
【题目】由有机物Ⅰ合成Ⅳ(香豆素)的合成路线如下:
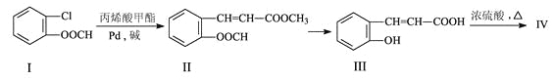
回答下列问题:
(1)写出分子式:丙烯酸甲酯____________________;
(2)写出反应类型:Ⅰ→Ⅱ_____________;若要Ⅱ→Ⅲ的反应完全,则Ⅱ→Ⅲ 反应需要的条件是_____________________________;
(3)已知化合物Ⅳ的相对分子质量为146,写出结构简式:Ⅳ_________________;
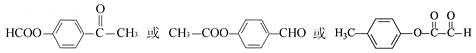
(4)化合物V是Ⅲ的一种同分异构体,V有如下特征:分子中除苯环外,无其它环状结构;在核磁共振氢谱图中,有四个吸收峰;能发生银镜反应;1 mol V最多能与2mol的NaOH反应。V的结构简式为________________;
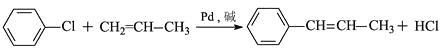
(5)根据已有知识并模仿香豆素合成路线的相关反应,试写出以氯苯和丙烯(CH2=CH-CH3)为原料,合成![]() 的化学方程式__________(无机试剂任选)。
的化学方程式__________(无机试剂任选)。
【答案】C4H6O2 取代反应 NaOH溶液/加热 ![]()
 、
、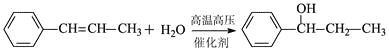
【解析】
(1)从化合物Ⅱ可以知道丙烯酸甲酯的结构简式为:CH2=CHCOOCH3,分子式为C4H6O2。
(2)比较化合物Ⅰ、Ⅱ,可以看出是—CH=CHCOOCH3取代了苯环上的—Cl,所以反应是取代反应;Ⅱ→Ⅲ是酯类水解反应,反应要完全进行要在碱性条件下,故反应条件是:NaOH溶液、加热。
(3)化合物Ⅲ的相对分子质量为164,化合物Ⅳ的相对分子质量为146,可知Ⅲ生成Ⅳ分子内脱去了1个水分子,—OH和—COOH发生酯化反应,则Ⅳ的结构简式为:![]() 。
。
(4)V有如下特征:分子中除苯环外,无其它环状结构;在核磁共振氢谱图中,有四个吸收峰;能发生银镜反应,说明有醛基;1 mol V最多能与2mol的NaOH反应。V的结构简式为: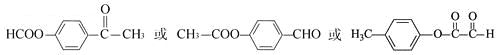 。
。
(5)根据Ⅰ→Ⅱ,可以通过取代反应在苯环上加长碳链,反应的化学方程式为:![]() ,在通过加成反应得到产物,方程式为:
,在通过加成反应得到产物,方程式为: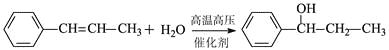 。
。


科目:高中化学 来源: 题型:
【题目】化学在环境保护中起着十分重要的作用,电化学降解NO3-的原理如图所示。下列说法不正确的是( )
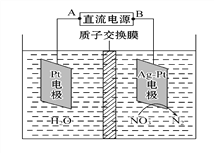
A. A为电源的正极
B. 溶液中H+从阳极向阴极迁移
C. 电解过程中,每转移2 mol电子,则左侧电极就产生32gO2
D. Ag-Pt电极的电极反应式为2NO3-+12H++10e- = N2↑+ 6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有三个不成对的电子;C元素可分别与A、B、D生成RC2型化合物,其中的DC2与C3互为等电子体。下列叙述中不正确的是
A. D原子的简化电子排布式为[Ar]3s23p4
B. B、C两元素的第一电离能大小关系为B>C
C. 用电子式表示AD2的形成过程为![]()
D. 由B60分子形成的晶体与A60相似,分子中总键能:B60>A60
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确的是 ( )

A.电负性:![]()
B.离子半径:![]()
C.![]() 分子中各原子的最外层均满足8电子稳定结构
分子中各原子的最外层均满足8电子稳定结构
D.Z元素基态原子的最外层电子排布图为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,配制一组c(H2A)+c(HA-)+c(A2-)=0.10mol·L-1的H2A和NaOH的混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法中正确的是( )
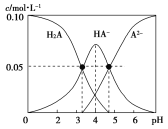
A.在c(Na+)=0.10mol·L-1的溶液中:c(A2-)-c(H+)=c(H2A)-c(OH-)
B.pH=4的溶液中:c(HA-)=c(H2A)+c(A2-)
C.pH=7的溶液中:c(Na+)=c(A2-)+c(HA-)
D.Ka1(H2A)的数量级为10-5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 为五种短周期元素。
为五种短周期元素。![]() 原子的质子数与电子层数相同,
原子的质子数与电子层数相同,![]() 原子核外电子数是
原子核外电子数是![]() 原子最外层电子数的2倍,
原子最外层电子数的2倍,![]() 、
、![]() 、
、![]() 、
、![]() 在周期表中的相对位置如图所示。下列说法不正确的是( )
在周期表中的相对位置如图所示。下列说法不正确的是( )
|
|
| |
|
A.原子半径:![]()
B.热稳定性:![]() ;沸点:
;沸点:![]()
C.仅由![]() 、
、![]() 、
、![]() 三种元素形成的化合物中不可能含离子键
三种元素形成的化合物中不可能含离子键
D.![]() 、
、![]() 分子中每个原子最外层均满足8电子结构
分子中每个原子最外层均满足8电子结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种物质有如下相互转化关系(其中X、W为单质,Y、Z为化合物,未列出反应条件)
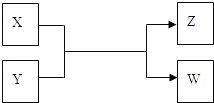
Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
(1)常温下,X的颜色是____________。
(2)工业上Z有多种用途,用化学方程式表示Z的一种用途_________________________。
(3)生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到这种碘酸盐,此反应的离子方程式是______________________________________。
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是__________________________________。
(2)将3.48g Z加入50mL 4mol/L的稀HNO3中充分反应,产生112mL的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀.当沉淀量最多,至少需要加入2mol/L的NaOH溶液_____mL (精确到0.1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选做(10分)
(1)写出有机物的系统命名: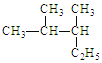 。
。
(2)键线式![]() 表示的分子式为 ;名称是 。
表示的分子式为 ;名称是 。
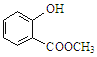 中含有的官能团的名称为 。
中含有的官能团的名称为 。
(3)丁基的4个结构简式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.已知KCl与MgO的晶体结构跟NaCl的晶体结构相似,则晶体的熔点:MgO>KCl>NaCl
B.向滴有酚酞的碳酸钠溶液中加入BaCl2溶液,溶液褪色
C.分散系中分散质粒子的直径:Fe(OH)3胶体>Fe(OH)3悬浊液>FeCl3溶液
D.Na2O、MgO、Al2O3均属于碱性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com