
【题目】铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:

已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有______________________(任写一种)。
(2)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为_____________,若加 A 后溶液的 pH调为5,则溶液中 Fe3+的浓度为_____________mol/L。
(3)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:____________________。
(4)“赶氨”时,最适宜的操作方法是______________________。
【答案】升高温度或搅拌 3.7≤pH<5.6 4×10-11 Mn2+ + HCO3-+ NH3 = MnCO3↓+NH4+ 加热
【解析】
⑴加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有升高温度或搅拌。
⑵常温下“除铁”时加入的试剂A可用CuO等,主要是除掉铁离子不能沉淀铜离子,因此调节pH调的范围为3.7≤pH<5.6,若加 A 后溶液的 pH调为5,c(OH-) = 1×10-9mol/L,则溶液中 Fe3+的浓度为![]() 。
。
⑶“沉锰”(除 Mn2+)过程中反应的离子方程式:Mn2+ + HCO3-+ NH3 = MnCO3↓+NH4+。
⑷升高温度,氨气在水中的溶解度减小,所以“赶氨”时,最适宜的操作方法是加热。
⑴加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有升高温度或搅拌,故答案为:升高温度或搅拌。
⑵常温下“除铁”时加入的试剂A可用CuO等,主要是除掉铁离子不能沉淀铜离子,因此调节pH调的范围为3.7≤pH<5.6,若加 A 后溶液的 pH调为5,c(OH-) = 1×10-9mol/L,则溶液中 Fe3+的浓度为![]() ,故答案为:3.7≤pH<5.6,4×10-11。
,故答案为:3.7≤pH<5.6,4×10-11。
⑶“沉锰”(除 Mn2+)过程中反应的离子方程式:Mn2+ + HCO3-+ NH3 = MnCO3↓+NH4+,故答案为:Mn2+ + HCO3-+ NH3 = MnCO3↓+NH4+。
⑷升高温度,氨气在水中的溶解度减小,所以“赶氨”时,最适宜的操作方法是加热,故答案为:加热。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.实验室用锌与稀硫酸反应时,滴加少量硫酸铜溶液能加快反应速率,因为硫酸铜是催化剂
B.某温度下,一定体积的密闭容器中进行可逆反应:![]() ,平衡后加入一定量X,则
,平衡后加入一定量X,则![]() 增大
增大
C.温度和压强一定时,对于可逆反应:![]() ,混合气体的密度不再改变,则反应达到平衡状态
,混合气体的密度不再改变,则反应达到平衡状态
D.将![]() 溶液与
溶液与![]() 溶液混合后生成白色沉淀,是两种溶液水解相互促进的结果
溶液混合后生成白色沉淀,是两种溶液水解相互促进的结果
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及解释或结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 解释或结论 |
A | 向足量的浓硝酸中加入铁片,一段时间后加入铜粉 | 有气体生成,溶液呈蓝绿色 | 浓硝酸将Fe氧化为 |
B | 分别向 | 均有白色沉淀产生 | 金属性: |
C | 表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触 | 银器变得光亮如新 | 构成原电池,铝做负极,硫化银得电子被还原成单质银 |
D | 向 | 白色沉淀逐渐变为浅蓝色 |
|
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)Al(OH)3酸式电离方程式:___________________________________
(2)用离子方程式分析Na2CO3溶液显碱性的主要原因:___________________________________
(3)CaCO3沉淀溶解平衡方程式:_____________________________________
(4)25℃时,四种溶液 ① pH=2的H2SO4溶液、②pH=12的Ba(OH)2溶液,③pH=4的NH4Cl溶液,④pH=12的CH3COONa溶液,水电离的c(H+)之比是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吗啡是严格查禁的毒品.吗啡分子含C71.58%,H6.67%,N4.91%,其余为O.已知其相对分子质量不超过300,则吗啡的分子式是
A.C17H19NO3B.C17H20N2OC.C18H19NO3D.C18H20N2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:Ksp(BaCO3)=5.1×10-9 mol2·L-2;Ksp(BaSO4)=1.1×10-10 mol2·L-2。下列推断正确的是( )
A. 不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4)
B. 抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替
C. 若误饮[Ba2+]=1.0×10-5 mol·L-1的溶液时,会引起钡离子中毒
D. 可以用0.36 mol·L-1的Na2SO4溶液给钡离子中毒患者洗胃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现拟在实验室里利用空气和镁粉为原料,制取少量氮化镁(Mg3N2)。已知这一过程中可能发生下列反应:
①2Mg+O2![]() 2MgO ②3Mg+N2
2MgO ②3Mg+N2![]() Mg3N2
Mg3N2
③2Mg+CO2![]() 2MgO+C④Mg+H2O(蒸气)=MgO+H2
2MgO+C④Mg+H2O(蒸气)=MgO+H2
⑤Mg3N2+6H2O=3Mg(OH)2+2NH3可供选择的仪器和药品如下图所示。且假设正确操作时,装置内所发生的反应是完全的。
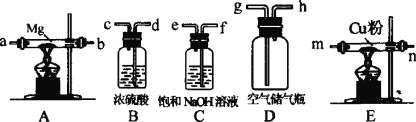
试回答下列问题:
(1)实验开始时,先点燃________装置中的酒精灯,原因是________;再将与g连接的自来水龙头打开,形成自h导管流出的气流,则气流依次流经的导管为(填字母代号):h→________;
(2)你是否选择了B装置,理由是什么________________________ ;
(3)你是否选择了C装置,理由是什么________________________;
(4)如果同时点燃A、E装置的酒精灯,对实验结果产生的影响________ 为什么___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.Ksp(AB2)小于Ksp(CD),说明AB2的溶解度一定小于CD的溶解度
B.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
C.2C+SiO2![]() Si+2CO↑,此反应能够进行是因为碳的还原性比硅强
Si+2CO↑,此反应能够进行是因为碳的还原性比硅强
D.弱酸也可以通过复分解反应制强酸,如:H2S+CuSO4=H2SO4+CuS↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素硼对植物的生长和人体骨骼的健康有着十分重要的作用。请回答下列问題:
(1)区分晶体硼和无定硼形科学的方法为_________________________________。
(2)下列B原子基态的价层电子排布图中正确的是___________
A. B.
B.
C. D.
D.
(3)NaBH4是重要的储氢载体,阴离子的立体构型为___________。
(4)三硫化四磷分子(结构如下图1所示)是___________分子(填极性”或非极性)。
(5)图2表示多硼酸根离子的一种无限长的链式结构,其化学式可表示为___________。

(6)硼酸晶体是片层结构,其中一层的结构如图3所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是_________________________________。
(7)立方氮化硼(BN)是新型高强度耐磨材料,可作为金属表面的保护层,其晶胞结构(如右图)与金刚石类似。已知该晶体密度为ag/cm3,则晶体中两个N原子间的最小距离为___________pm。(用含a的代数式表示,NA表示阿伏加德罗常数)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com