
【题目】常温下,下列溶液中的微粒浓度关系正确的是( )
A. 新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B. pH=8.3的NaHS溶液:c(Na+)>c(HS-)>c(S2-)>c(H2S)
C. pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+)
D. 0.2 mol·L-1 CH3COOH溶液与0.1 mol·L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH)
【答案】D
【解析】A.方程式左侧缺c(H+),不满足电荷守恒规律,A错误;B. NaHS溶液存在平衡:HS-![]() H++S2-电离显酸性,HS-+H2O
H++S2-电离显酸性,HS-+H2O![]() H2S+OH-水解显碱性,pH=8.3,水解过程大于电离过程,c(HS-)>c(H2S) >c(S2-),B错误;C. 氨水为弱碱,pH=11的氨水,c(OH-)=10-3 mol·L-1 c(NH3H2O)10-3 mol·L-1,反应后氨水过量,溶液显碱性,C错误;D.醋酸和强碱反应,溶液中存在的微粒:Na+、H+、CH3COO-、OH-、CH3COOH、H2O;电荷守恒:c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-),物料守恒:c(CH3COO-)+c(CH3COOH)=2c(Na+),消去c(Na+),得到:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH),D正确;答案选D。
H2S+OH-水解显碱性,pH=8.3,水解过程大于电离过程,c(HS-)>c(H2S) >c(S2-),B错误;C. 氨水为弱碱,pH=11的氨水,c(OH-)=10-3 mol·L-1 c(NH3H2O)10-3 mol·L-1,反应后氨水过量,溶液显碱性,C错误;D.醋酸和强碱反应,溶液中存在的微粒:Na+、H+、CH3COO-、OH-、CH3COOH、H2O;电荷守恒:c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-),物料守恒:c(CH3COO-)+c(CH3COOH)=2c(Na+),消去c(Na+),得到:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH),D正确;答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】用Na2CO3·10H2O晶体配制0.20 mol/L Na2CO3溶液480 mL。
(1)实验时要用到的玻璃仪器有:除托盘天平、量筒、烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是___________________,在使用该仪器前必须进行的操作是_______________________。
(2)应用托盘天平称取Na2CO3·10H2O晶体的质量为___________g。
(3)配制溶液时有以下几个操作:

简述定容的过程:_______________________________。
(4)配制过程中,下列操作对所配溶液的浓度有什么影响,完成填空。
a.Na2CO3·10H2O晶体不纯,混有NaCl
b.用“左码右物”的称量方法称量晶体
c.容量瓶中洗净后未干燥,残留少量水
d.未冷却至室温就转移定容
e.加蒸馏水时不慎超过了刻度线,立即用胶头滴管将多余的水吸出
f.定容时,俯视刻度线
会引起所配溶液的浓度偏大的有________,无影响的有________。(填序号)
(5)如果直接使用浓度为2.00mol/L的Na2CO3溶液来配制100mL 1.00mol/L的Na2CO3溶液,需要量取2.00mol/L的Na2CO3溶液的体积为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种理想的绿色能源。利用生物质发酵得到的乙醇制取氢气,具有良好的应用前景。
乙醇水蒸气重整制氢的部分反应过程如下左图所示:
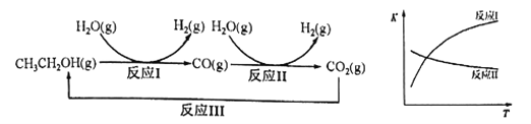
已知:反应Ⅰ和反应Ⅱ的平衡常数随温度变化曲线如上右图所示。
(1)反应Ⅰ中,1molCH3CH2OH(g)参与反应后的热量变化是256kJ。反应1的热化学方程式是_____________________。
(2)反应Ⅱ,在进气比[n(CO):n(H2O)]不同时,测得相应的CO的平衡转化率见下图(各点对应的反应温度可能相同,也可能不同)。
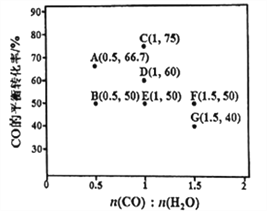
①图中D、E两点对应的反应温度分别为TD和TE判断:TD_______TE (填“<”“=”或“>”)。
②经分析,A、E 和G 三点对应的反应温度相同,其原因是A、E和G三点对应的________相同。
③当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系
是_________________。
(3)反应Ⅲ,在经CO2饱和处理的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。
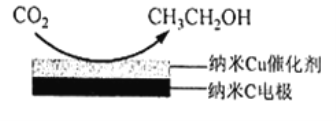
①阴极的电极反应式是____________________。
②从电解后溶液中分离出乙醇的操作方法是_________________。
③直接向KOH溶液中通入CO2,可以获得“经CO2饱和处理的KHCO3电解液”,该过程中浓度先增大后减小的离子是__________________ (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质检验的实验结论正确的是
选项 | 实 验 操 作 及 现 象 | 实 验 结 论 |
A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
B | 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有 Fe2+ |
C | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
D | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该钾盐是K2CO3 |
A. A B. B C. C D. D
【答案】B
【解析】
白色沉淀可能为AgCl;产生的气体能使澄清石灰水变浑浊,气体为二氧化碳或二氧化硫;先加入硫氰化钾溶液,溶液不显示红色,说明溶液中不存在铁离子,再加入具有氧化性的氯水,溶液变成红色,说明原溶液中一定存在亚铁离子;能使品红褪色的气体不一定为SO2;产生的气体能使澄清石灰水变浑浊,气体为二氧化碳或二氧化硫。
白色沉淀也可能为AgCl,若先加盐酸排除干扰,不生成沉淀,再加氯化钡生成沉淀,则溶液中一定含有SO42-,A错误;向某溶液中加入2滴KSCN溶液,溶液不显红色,说明溶液中不存在铁离子;再向溶液中加入几滴新制的氯水,溶液变为红色,说明加入氯水后溶液中出现了铁离子,证明原溶液中一定含有Fe2+,B正确;能使品红褪色的气体不一定为SO2,也可能为其它强氧化性气体,如氯气、臭氧等,C错误;产生的气体能使澄清石灰水变浑浊,气体可能为二氧化碳或二氧化硫,则溶液中可能含有CO32-、HCO3-,或SO32-、HSO3-,D错误。
【点睛】
本题考查化学实验方案的评价,侧重分析与实验能力的考查,注意实验的评价性分析,把握常见离子的检验、物质的性质、气体的检验等为解答的关键。
【题型】单选题
【结束】
17
【题目】在铜与浓硫酸的反应中,如果转移0.4mol电子,则被还原的硫酸物质的量
A. 0.4mol B. 0.2mol
C. 小于0.4mol D. 小于0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马日夫盐(Mn(H2PO4)2)是一种白色晶体,易溶于水,常用于机械设备的磷化处理。以软锰矿(主要成分为MnO2,还含有少量的Fe2O3、FeO和Al2O3)为原料制备马日夫盐的流程如下:
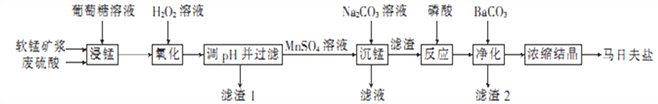
(1)粉碎软锰矿制成矿浆的目的是_________________________________________,葡萄糖(C6H12O6)与MnO2反应时,产物为MnSO4、CO2和H2O,该反应中氧化剂与还原剂的物质的量之比为__________。
(2)用H2O2溶液“氧化”时发生反应的离子方程式为_______________________________。
(3)已知几种金属离子的氢氧化物开始沉淀和完全沉淀的pH如下表所示、“调pH并过滤”时,应调整的pH范围为____________,滤渣1的主要成分为_________(填化学式)。
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.8 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
Mn2+ | 7.8 | 9.8 |
(4)加入磷酸后发生反应的化学方程式为_____________________________________。
(5)某工厂用上述流程制备马日夫盐,已知软锰矿中MnO2的含量为87%,整个流程中锰元素的损耗率为9%,则1t该软锰矿可制得马日夫盐__________t。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、R为原子序数依次增大的六种元素,位于元素周期表的前四周期。B元素原子含有3个能级,且毎个能级所含的电子数相同;D的原子核外有8种运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子3d轨道上有4个未成对电子。请回答下列问题:
(1)写出C基态原子的价层电子排布____________,F基态原子的外围电子排布式_____________。
(2)下列说法不正确的是____________ (填序号)。
A.二氧化硅的相对分子质量比二氧化碳大,所以沸点:SiO2 > CO2
B.笫一电离能由小到大的顺序:B <C < D
C.N2与CO为等电子体,结构相似
D.稳定性:H2O> H2S,水分子更稳定的原因是水分子间存在氢键
(3)F元素位于周期表中_________区,其离子是人体内多种酶的辅因子,人工模拟酶是当前研究的热点。向F的硫酸盐溶液中通人过量的C与A形成的气体X可生成[F(X)4]2+,该离子的结构式为__________(用元素符号表示)。
(4)某化合物与F(I)(I表示化合价为+ 1)结合形成下图1所示的离子,该离子中碳原子的杂化方式为________________________________。
(5)B单质的一种同素异形体的晶胞如下图2所示,则一个晶胞中所含B原子的个数为____________。
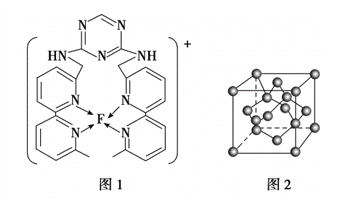
(6)D与F形成离子个数比为1:1的化合物,晶胞与NaCl类似,设D离子的半径为apm, F离子的半径bpm,则该晶胞的空间利用率为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵NH4ClO4是复合火箭推进剂的重要成分,实验室可通过下列反应制取
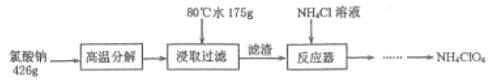
(1)氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为___________________________。
(2)反应得到的混合溶液中 NH4ClO4 和 NaCl 的质量分数分别为 0.30 和 0.15, 从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)_______、______、 _______、冰水洗涤、干燥。用冰水洗涤的目的是___________________________________________________。若氯化铵溶液用氨气和浓盐酸代替,则该反应不需要加热就能进行,其原因是_____________。
(3) 样品中NH4ClO4的含量可用蒸馏法进行则定,蒸馏装置如图所示(加热和仪器固定装置已略去),实验步骤如下:
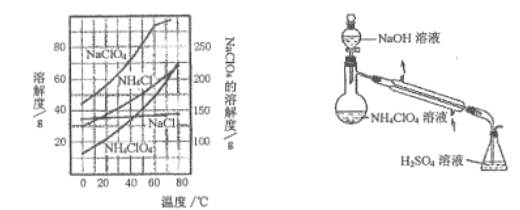
步骤1: 按上图所示组装仪器,检查装置气密性。
步骤2: 准确称取样品a g 于蒸馏烧瓶中,加入150mL 水溶解。
步骤3: 准确量取40.00mL、0.1000mol/L H2SO4溶解于锥形瓶中。
步骤4: 经分液漏斗向蒸馏瓶中加入20.00mL、3mol /LNaOH 溶液。
步骤5: 加热蒸馏至蒸馏烧瓶中剩余约100mL溶液。
步骤6: 用新煮沸过的水冲洗冷凝装置2--3 次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用c mol/L NaOH 标准溶液滴定剩余H2SO4至终点时消耗NaOH 标准溶液VmL。
①步骤3 中,准确量取40.00mL.H2SO4溶液的玻璃仪器是___________。
②样品中NH4ClO4的质量分数为_______。若取消步骤6,则对定结果的影响是______(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)![]() pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是
pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是

A.T1<T2 p1>p2 m+n>p 放热反应
B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应
D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com