
【题目】Ⅰ(1)用CCl4萃取碘水中的碘,下图的分液漏斗中,下层液体呈______色;打开分液漏斗活塞,却未见液体流下,原因可能是_____。

Ⅱ 某同学用某种粗盐进行提纯实验,步骤见下图。

请回答下列问题:
(1)步骤①和②的操作名称是________。
(2)步骤③判断加入盐酸“适量”的方法是______________;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了____________,当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干。
(3)猜想和验证:
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | _______ | 猜想Ⅰ成立 |
猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入________,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | _____ |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,________ | _______ | 猜想Ⅲ成立 |
【答案】紫红 分液漏斗上口活塞小孔未与空气相通或者分液漏斗上口活塞未打开 过滤 滴加盐酸至无气泡产生为止 防止溶液飞溅 有气泡放出,澄清石灰水变浑浊 稀盐酸(或稀硝酸) 猜想Ⅱ不成立 滴入BaCl2溶液和稀盐酸溶液 有白色沉淀且不溶于稀盐酸
【解析】
Ⅰ(1)四氯化碳的密度大于水且和水不互溶,四氯化碳能萃取碘,所以有机层在下方,水在上方;如果分液漏斗上口活塞小孔未与空气相通或者分液漏斗上口活塞未打开,则液体不会流出;
Ⅱ 粗盐溶于水,先采用过滤方法除去难溶性泥沙,得到滤液1,向滤液中加入过量碳酸钠溶液,搅拌,然后过滤除去难溶性固体A,得到滤液2,向滤液中加入适量稀盐酸,过量的碳酸钠溶于稀盐酸得到氯化钠,将氯化钠溶液蒸发得到氯化钠晶体;
(1)分离难溶性固体和溶液采用过滤方法;
(2)碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水;步骤④加热蒸发时要用玻璃棒不断搅拌,目的是防止溅出液体;
(3)猜想I:碳酸盐能和稀盐酸反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊;
猜想II:碳酸根离子可以用稀盐酸或稀硝酸检验,钡离子可以用可溶性的硫酸盐检验;
猜想III:要鉴定该混合物中的硫酸根离子,可以用盐酸酸化的氯化钡溶液检验。
Ⅰ(1)四氯化碳的密度大于水且和水不互溶,四氯化碳能萃取碘,所以有机层在下方,水在上方,碘的四氯化碳溶液呈紫红色;如果分液漏斗上口活塞小孔未与空气相通或者分液漏斗上口活塞未打开,则液体不会流出;
故答案为:紫红;分液漏斗上口活塞小孔未与空气相通或者分液漏斗上口活塞未打开;
Ⅱ 粗盐溶于水,然后采用过滤方法除去难溶性泥沙,得到滤液1,向滤液中加入过量碳酸钠溶液,搅拌,然后过滤除去难溶性固体A,得到滤液2,向滤液中加入适量稀盐酸,过量碳酸钠溶于稀盐酸得到氯化钠,将氯化钠溶液蒸发得到氯化钠晶体,
(1)步骤①和②都是将不溶于液体的固体和液体分离,操作方法都是过滤;
故答案为:过滤;
(2)盐酸与过量的碳酸钠反应生成氯化钠、水和二氧化碳,滴加盐酸至无气泡产生为止,说明刚好与碳酸钠反应完;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止局部过热,造成液滴飞溅;当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干;
故答案为:滴加盐酸至无气泡产生为止;防止溶液飞溅;
(3)猜想I:碳酸盐能和稀盐酸反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊,所以可以用澄清石灰水检验二氧化碳,如果有气泡放出且澄清石灰水变浑浊,则说明猜想I成立;
猜想II:碳酸根离子可以用稀盐酸或稀硝酸检验,所以滴加的试剂是稀盐酸或稀硝酸,钡离子可以用可溶性的硫酸盐检验,如果有气泡冒出说明含有碳酸根离子,如果不产生白色沉淀说明不含钡离子,则猜想II不成立;
猜想Ⅲ中要检验硫酸根离子,固体溶于水滴入BaCl2溶液和稀盐酸溶液,观察到有白色沉淀且不溶于稀盐酸,则猜想Ⅲ成立;
故答案为:有气泡放出,澄清石灰水变浑浊;稀盐酸(或稀硝酸);猜想Ⅱ不成立;滴入BaCl2溶液和稀盐酸溶液;有白色沉淀且不溶于稀盐酸。


 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】苯是实验室常用的萃取剂,下列关于苯的说法错误的是( )
A. 常温下是液体,密度比水小B. 不能使高锰酸钾溶液褪色
C. 能和液溴发生加成反应D. 能和硝酸发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体含氧65%、碳18%、氢10%、氮3%、钙1.5%、磷1%、钾0.35%、硫0.25%、钠0.15%、氯0.15%、镁0.05%,它们被称为人体常量元素。
(1)人体的构成元素,从周期表来看,元素数目最多族为___________ 族。属于第三周期的非金属元素的原子半径由大到小的顺序______________。人体还有许多微量元素,请列举其中的一种____________。
(2)含量最高的元素原子核外运动状态有___________种,最外层电子轨道表示式_____________;与它同族的另一种元素的活动性相比_______>_______。(用元素符号表示),请用一个事实说明该结论______。
(3)含量前3位的元素按原子个数比1:1:2形成的物质的名称是_____________(写出一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用铁的氧化物在高温条件下循环裂解水制氢气的流程如下图所示。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g)![]() 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________。
(2)反应III为:CO2(g)+C(s)![]() 2CO(g)
2CO(g) ![]() H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________(任写一条措施)。
(3)上述流程中铁的氧化物可用来制备含有Fe3+的刻蚀液,用刻蚀液刻蚀铜板时,可观察到溶液颜色逐渐变蓝,该反应的离子方程式为_________。刻蚀液使用一段时间后会失效,先加酸,再加入过氧化氢溶液,可实现刻蚀液中Fe3+的再生,该反应的离子方程式为_________。
(4)上述流程中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用粗锌与稀硫酸反应制取氢气,利用氢气还原氧化铜来测定铜的相对原子质量。实验装置如下:

(1)在启普发生器中纯锌与稀硫酸反应过于缓慢,可采取的加快速率的措施是①______,②______。
(2)用纯度不高的锌(粗锌)制取氢气,反应速率快,但制得的氢气因含H2S等还原性杂质而有难闻的气味,CuSO4洗气瓶中观察到的现象是有黑色沉淀生成,请写出该洗气瓶中发生复分解反应的化学方程式_______,是否可以将CuSO4溶液换成浓硫酸_________(答“是”或“否”);理由是_____________。请简述用CuSO4溶液配制检验醛基的新制氢氧化铜的方法________________________。
(3)装置中氯化钙的作用是__________________________。有同学发现粗锌与稀硫酸反应一段时间后,锌粒表面变黑,于是收集了少量该黑色固体,验证黑色固体含铁元素的化学方法___________。
(4)实验中得到的数据有:小瓷皿的质量mg,小瓷皿加样品的质量n g,反应后小瓷皿加固体的质量w g,已知氧的相对原子质量为16,则铜的相对原子质量是________________ (用含m、n、w的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一固定体积的密闭容器中,对于可逆反应A(s)+3B(g)![]() 2C(g),下列说法不能说明达到化学平衡状态的是
2C(g),下列说法不能说明达到化学平衡状态的是
A. 气体密度不再变化 B. 混合气体的总压强不再变化;
C. A、B、C的物质的量之比为1∶3∶2 D. 混合气体的平均相对分子质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)0.25 mol CH4在标准状况下的体积为_______L,0.25 mol CH4中含有______个氢原子。
(2)相同质量的CO和CO2,它们所含的原子数之比为_______,标准状况下,含有相同氧原子数的CO和CO2的体积之比为________。
(3)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为________,该金属元素的相对原子质量为__________。
(4)若ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是___________(设NA为阿伏加德罗常数的值)。
(5)标准状况下有①0.112 L水 ②0.5NA个HCl分子③25.6 g SO2气体 ④0.2 mol氨气(NH3) ⑤2 mol Ne所含原子个数从大到小的顺序为_____。
(6)6.72 L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为__________g。
(7)某温度时,一定量的元素A的气态氢化物AH3,在恒温密闭容器中分解为两种气体单质,此时压强增加了75%,则AH3分解反应的化学方程式________________________。
(8)V mL Fe2(SO4)3溶液中,含有Fe 3+ m g,取出V/2mL该溶液稀释至4V mL,则溶液中SO42-的物质的量浓度为___________。(用含有m、V的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.将少量饱和氯化铁溶液滴入沸水中,继续煮沸,可制得Fe(OH)3胶体,反应的方程式为:FeCl3 + 3H2O![]() Fe(OH)3(胶体) + 3HCl。
Fe(OH)3(胶体) + 3HCl。
①当溶液呈__时,停止加热,即制得Fe(OH)3胶体。
②氢氧化铁胶体粒子直径大小的范围是________。
③下列叙述错误的是_____。
A.雾属于胶体,能产生丁达尔效应
B.“PM2.5”悬浮在空气中形成胶体,危害人体健康 (“PM2.5”指大气中直径小于或等于2.5微米的细小颗粒物,也可称为可吸入肺颗粒物)
C.明矾、硫酸铁可以净水,净水原理和胶体有关
D.胶体在一定条件下能稳定存在,属于介稳体系
Ⅱ.(1)下列4组物质均有一种物质的类别与其它3种不同
A.CaO、Na2O、CO2、CuO B. H2、C、P、Cu
C.O2、Fe、Cu、Zn D. HCl、H2O、H2SO4、HNO3
以上四组物质中与其他不同的物质依次是(填化学式):A__;B__;C___;D___。
(2)下列物质:①HCl②蔗糖③NaOH④KCl⑤SO2⑥Fe⑦碳酸钠溶液,属于电解质的是:__(填序号)能导电的是:____(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:H2(g)+1/2O2(g)H2O(g),反应过程中能量变化如图所示,则:
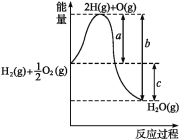
①a、b、c分别代表什么意义?
a______________________________;
b_______________________________;
c_______________________________。
②该反应是ΔH____________0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,已知:H2(g)+![]() O2(g)H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)H2(l) ΔH=-0.92 kJ·mol-1
O2(g)O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧生成气态水的热化学方程式____________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com