
【题目】在容积为1L的恒容密闭容器中,用三种纳米级Cu2O分别进行催化分解水的实验:2H2O(g)![]() 2H2(g)+O2(g) ΔH>0。水蒸气的浓度c随时间t的变化如下表所示:
2H2(g)+O2(g) ΔH>0。水蒸气的浓度c随时间t的变化如下表所示:
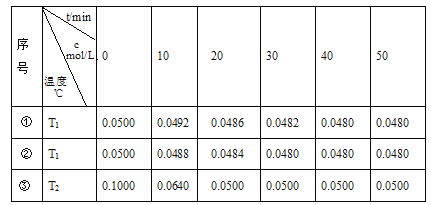
(1)对比实验的温度:T2_________T1(填“>”、“<”或“=”)
(2)催化剂催化效率:实验①________实验②(填“>”或“<”)
(3)在实验③达到平衡状态后,向该容器中通入水蒸气与氢气各0.1mol,则反应再次达到平衡时,请确定化学反应进行的方向_________________(填“向正反应反应进行”或“向逆反应方向进行”或“平衡不移动”)。
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列加点的物质在化学反应中能完全消耗的是( )
A.向150mL3mol·L-1的稀硝酸中加入6.4g铜
B.标准状况下,将1g铁片投入15mL18.4mol·L-1的硫酸中
C.用50mL8mol·L-1浓盐酸与10g二氧化锰共热制取氯气
D.5×107Pa、500℃和铁触媒条件下,用1mol氮气和4mol氢气合成氨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1mol C与1mol水蒸气反应生成1mol CO和1mol H2,吸热131.5kJ:______________________。此反应的反应类型_________。
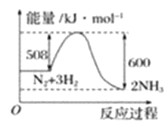
(2)根据如图写出热化学方程式____;此反应为____反应(放热或吸热);此反应的活化能____千焦。
(3)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式________________________。
(4)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6kJ·mol–1
2SO3(g) ΔH=-196.6kJ·mol–1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0kJ·mol–1
2NO2(g) ΔH=-113.0kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g)在温度为T1、T2(T2>T1)时,平衡体系中NO2的体积分数随压强变化如图所示。下列说法正确的是
2NO2(g)在温度为T1、T2(T2>T1)时,平衡体系中NO2的体积分数随压强变化如图所示。下列说法正确的是

A. 由图可知B点的平衡常数大于C点的平衡常数
B. A、C两点气体的颜色:A深,C浅
C. A、C两点气体的平均相对分子质量:A<C
D. 保持容器体积不变,再充入N2O2气体,平衡逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭体系中,可逆反应:A(s)+2B(g)![]() 2C(g) ΔH<0,不能作为该反应达到化学平衡的标志的是
2C(g) ΔH<0,不能作为该反应达到化学平衡的标志的是
①v正(B)=v逆(C) ②n(B)∶n(C)=1∶1 ③容器内压强不再改变
④容器内气体的密度不再改变 ⑤容器内混合气体的平均相对分子质量不再改变
A. ②③④⑤ B. ①③④ C. ②③ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂二次电池新正极材料的探索和研究对锂电池的发展非常关键。
(1) 锂硒电池具有优异的循环稳定性。
①正极材料Se可由SO2通入亚硒酸(H2SeO3)溶液反应制得,则该反应的化学方程式为__。
②一种锂硒电池放电时的工作原理如图1所示,写出正极的电极反应式:________________。充电时Li+向________(填“Se”或“Li”)极迁移。
③ Li2Sex与正极碳基体结合时的能量变化如图2所示,图中3种Li2Sex与碳基体的结合能力由大到小的顺序是________。
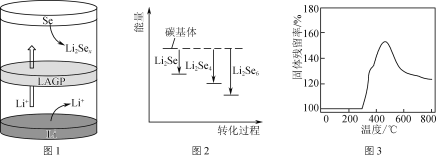
(2) Li2S电池的理论能量密度高,其正极材料为碳包裹的硫化锂(Li2S)。
① Li2S可由硫酸锂与壳聚糖高温下制得,其中壳聚糖的作用是________。
②取一定量Li2S样品在空气中加热,测得样品固体残留率随温度的变化如图3所示。(固体残留率=![]() ×100%)分析300 ℃后,固体残留率变化的原因是________。
×100%)分析300 ℃后,固体残留率变化的原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
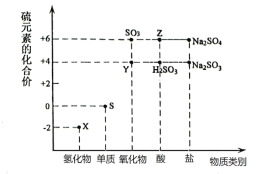
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___(填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中还原剂与氧化剂的物质的量之比为___。
(3)检验物质Y的方法是___。
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为___。
(5)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___(填代号)。
a.Na2S+S b.SO2+Na2SO4 c.Na2SO3+S d.Na2SO3+Na2SO4 e.SO2+ Na2S2+Na2CO3
(6)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL0.05 mol·L-1的Na2SO3溶液与20mL0.02mol·L-1的K2Cr2O7溶液恰好完全反应时,Cr元素在还原产物中的化合价为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O (方程式中H为+1价,O为-2价)下列说法正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O (方程式中H为+1价,O为-2价)下列说法正确的是( )
A.KClO3在反应中失电子B.ClO2是氧化产物
C.H2C2O4在反应中被氧化D.1 molKClO3参加反应有2mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值。下列叙述正确的是( )
为阿伏加德罗常数的值。下列叙述正确的是( )
A.![]() 乙烷分子中含有的共价键数目为
乙烷分子中含有的共价键数目为![]()
B.![]() 完全溶于水转移的电子数为
完全溶于水转移的电子数为![]()
C.标准状况下,![]() 含有的原子数为
含有的原子数为![]()
D.![]() 乙烯和丙烯的混合物中含有的质子数为
乙烯和丙烯的混合物中含有的质子数为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com