
【题目】利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理。
某工厂对制革工业污泥中Cr元素的回收与再利用工艺如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
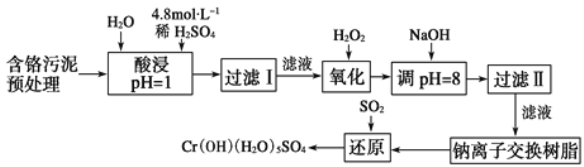
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | - | - | - |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9(>9溶解) |
(1) 酸浸时,为了提高浸取率可采取的措施是____(至少写两条)。
(2)H2O2的作用是_____。
(3)调pH=8是为了除去___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(4)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(5)已知以下氧化还原反应方程式(未配平):Na2Cr2O7+SO2+H2O=Cr(OH)(H2O)5SO4+Na2SO4;以上反应各物质的配平系数依次为___。每生成1 mol Cr(OH)(H2O)5SO4转移电子的数目为___。
【答案】升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)、适当延长浸取时间 将Fe2+和Cr3+氧化 Fe3+、Al3+ Mg2+、Ca2+ 1、3、11、2、1 3NA
【解析】
硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+,过滤后向滤液中加入双氧水,双氧水有强氧化性,能氧化还原性的Fe2+生成Fe3+;加入氢氧化钠溶液后,调节溶液的pH至8,根据表中数据知,Fe3+、Al3+转化为沉淀除去;然后过滤,向滤液中加入钠离子交换树脂,然后加入二氧化硫,发生氧化还原反应得到Cr(OH)(H2O)5SO4。
(1)升高温度、搅拌、增大反应物浓度都可以提高浸取率,其采用措施为升高温度、搅拌、过滤后再向滤渣中加入硫酸(多次浸取)、适当延长浸取时间(只要答出任意一点即可,其他合理答案也可);
(2)过氧化氢具有氧化性,可将Fe2+和Cr3+氧化;
(3)pH=8时,Fe3+、Al3+完全生成沉淀,所以pH=8时除去阳离子为Fe3+、Al3+;
(4)钠离子交换树脂交换的离子是钙离子和镁离子,即:Mg2+、Ca2+;
(5)二氧化硫具有还原性,被滤液Ⅱ中通过离子交换后的溶液中Na2CrO4氧化为硫酸,Na2CrO4氧被还原为CrOH(H2O)5SO4,水溶液中生成硫酸反应生成硫酸钠,依据原子守恒分析书写配平;Na2CrO4+3SO2+11H2O=2CrOH(H2O)5SO4↓+Na2SO4,
根据方程式:3SO2~2CrOH(H2O)5SO4,可知每生成1mol Cr(OH)(H2O)5SO4转移电子的数目为3NA。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如下图所示操作能实现实验目的的是( )
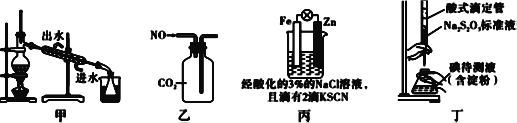
A. 用图甲装置分离碘和四氯化碳,在锥形瓶中收集到碘单质
B. 用图乙装置收集NO气体
C. 用图丙装置验证牺牲阳极的阴极保护法
D. 用图丁装置测定待测液中I2的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.3molNH3分子中所含氢原子数与___个H2O分子中所含氢原子数相等。
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的物质的量是___。
(3)2.3gNa中含___mole-,在跟足量水反应中失去___mole-。
(4)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加德罗常数)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,装置在常温下工作(溶液体积变化忽略不计).闭合K,灯泡发光.下列叙述中不正确的是( )
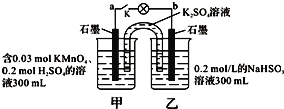
A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的H+浓度约为0.1mol/L
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.电池工作时,甲烧杯发生的反应为MnO4- + 3e- + 4H+ = MnO2 + 2H2O
D.乙池中的氧化产物为SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验和现象,所得实验结论正确的是( )
选项 | 实验 | 现象 | 实验结论 |
A | 向某溶液中先滴加适量稀硝酸,再滴加少量BaCl2溶液 | 出现白色沉淀 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
B | 向装有Fe(NO3)2溶液的试管中加入稀硫酸 | 在管口观察到红棕色气体 | HNO3分解成了NO2 |
C |
| 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性:Cl2>Br2>I2 |
D | SO2和SO3混合气体通入Ba(NO3)2溶液 | 出现白色沉淀 | 得到的沉淀只有BaSO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列有机分子的模型回答问题
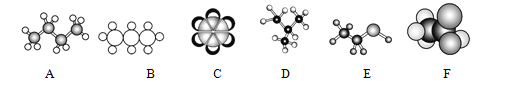
(1)写出A、B、C、D的结构简式:
A:_____ B、_____ C、__________ D、________
(2)E、F中官能团的名称分别是:_________ _________
(3)用“同分异构体”“同系物”填空:
A与B的关系是互为:__________ A与D的关系是互为:_________
(4)A的一氯代物有_____种,B的二氯代物有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1, Q在元素周期表的各元素中电负性最大。P元素的第三电子层处于全充满状态,第四电子层只有一个电子。请回答下列问题:
(1)基态X的外围电子电子排布图为_________ 。P元素属于__________ 区元素,
(2)XZ2分子的空间构型是______,YZ2分子中Y的杂化轨道类型为_____,相同条件下两者在水中的溶解度较大的是_____(写分子式),理由是_____。
(3)元素M与元素Q形成晶体中,M离子与Q离子的配位数之比为__________
(4)P单质形成的晶体中,P原子采取的堆积方式为_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)![]()
![]() 2Z(g)此反应达到平衡的标志是( )
2Z(g)此反应达到平衡的标志是( )
A. 容器内压强不随时间变化
B. 容器内气体的密度不随时间变化
C. 容器内X、Y、Z的浓度之比为1︰2︰2
D. 单位时间消耗0.1mol X同时生成0.2mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸锌作为补锌药,具有见效快、吸收率高、副作用小、使用方便等优点。某学习小组在实验室以葡萄糖和氧化锌为主要原料合成该物质。
反应原理:CH2OH(CHOH)4CHO + H2O2 ![]() CH2OH(CHOH)4COOH + H2O
CH2OH(CHOH)4COOH + H2O
2CH2OH(CHOH)4COOH + ZnO ![]() Zn[CH2OH(CHOH)4COO] 2 + H2O
Zn[CH2OH(CHOH)4COO] 2 + H2O
设计的合成路线为:
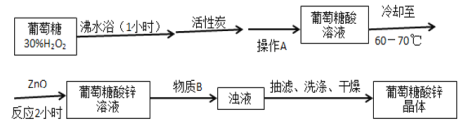
相关信息如下:
葡萄糖酸锌易溶于水,在乙醇与水的混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如图1
实验中所涉及的部分装置如图所示(图2装置先制备葡萄糖酸,再与ZnO反应制备
葡萄糖酸锌),图3为抽滤装置
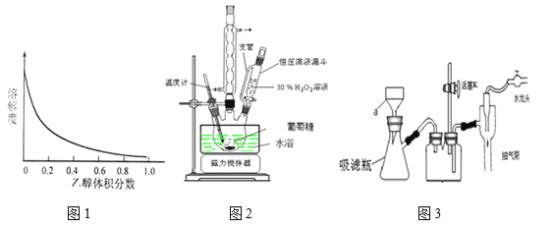
请根据以上信息,回答下列问题:
(1)图2中恒压滴液漏斗的支管的作用是___________,图3中a装置的名称____________。
(2)30%H2O2所用的物质的量大概是葡萄糖的3倍,而且并未一次性与葡萄糖混合,而是利用恒压滴液漏斗缓慢滴加的理由_________________________________。
(3)操作A是______________,物质B是________________。
(4)抽滤完毕或中途停止抽滤时,应先___________________,然后____________________。
(5)三颈烧瓶中的葡萄糖酸锌晶体转入到抽滤装置中时,瓶壁上往往还粘有少量晶体,需选用液体将瓶壁上的晶体冲洗下来后转入到抽滤装置中,下列液体最合适的是_______。
A 无水乙醇 B 饱和NaCl溶液 C 70%乙醇水溶液 D 滤液
(6)下列说法正确的是________。
A 用银氨溶液来替代30%H2O2将葡萄糖转变成葡萄糖酸,既经济又方便
B ZnO粉末与葡萄糖酸反应时,利用磁力搅拌可以增大ZnO粉末与葡萄糖酸的接触面积,加快反应速率
C 在抽滤过程中,如果吸滤瓶中的液体快接近支管口时,则拔掉吸滤瓶上的橡皮管,并从吸滤瓶的支管口倒出溶液
D 将葡萄糖酸锌晶体放在干燥器中可以防潮,在干燥器中放有干燥剂,并添加了无水CoCl2来指示是否得更换干燥剂,如果CoCl2为蓝色,说明干燥剂已经失效
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com