
【题目】能正确表示下列反应的离子方程式是( )
A.硫酸铝溶液中加入过量氨水Al3++3OH- =Al(OH)3 ↓
B.碳酸钠溶液中加入澄清石灰水 Ca(OH)2+![]() = CaCO3 ↓+2OH-
= CaCO3 ↓+2OH-
C.冷的氢氧化钠溶液中通入氯气Cl2 +2OH-=ClO-+H2O +Cl-
D.稀硫酸中加入铁粉2Fe + 6H+= 2Fe3++ 3H2↑
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 向酸性高锰酸钾溶液中通入SO2 | 溶液颜色褪去 | SO2具有漂白性 |
B | 将少量铜粉加入FeCl3溶液中 | 铜粉消失 | 还原性:Cu>Fe2+ |
C | 向溶液X中先滴加稀硝酸,再滴加氯化钡溶液 | 有白色沉淀生成 | 溶液X中含有SO |
D | 锌与稀硫酸反应制取氢气时,加入少量硫酸铜溶液 | 反应速率加快 | Cu2+起催化作用 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】有机玻璃是一种高分子化合物,在工业上和生活中有着广泛用途,工业上合成有机玻璃流程为:

下列说法不正确的是
A. 反应①的原子利用率达100%
B. 反应②是加聚反应
C. 相对分子质量为86,且与甲基丙烯酸甲酯具有相同官能团的有机物有5种
D. 甲基丙烯酸甲酯能使酸性高锰酸钾褪色,也能使Br2/CCl4褪色,二者原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:

(1)A是一种遇到碘单质能变蓝的多糖,A的分子式是_______________。
(2)物质B、C都能在加热条件下与新制的氢氧化铜反应产生砖红色沉淀,但不能发生水解反应,B中官能团的名称为____________,写出反应②的化学方程式___________________。
(3)下图是实验室通过反应①制取少量E的装置图。

实验时,加热前试管a中三种化学试剂的加入顺序依次为__________________(填名称),其中浓硫酸的作用是____________,写出试管a中生成E的化学反应方程式___________________。
(4)上述流程中C2H3Cl的结构简式____________。
(5)上述流程中标号①至④的反应中,与下列反应属同一反应类型的有______________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。回答下列问题:
(1)CH3OH的摩尔质量是__gmol-1。
(2)2molH2O中所含原子的物质的量为__mol。
(3)__g的氢气中所含H原子的数目与1molCH3OH相同。
(4)含0.1NA个O的CO2中有__个电子,标况下该CO2的体积为__L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于取代反应的是
①CH3CH=CH2+Br2![]() CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3![]() C6H5NO2+H2O
C6H5NO2+H2O
A. ①②B. ③④C. ①③D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种有机物,请回答下列问题:
A. | B. | C. |
D.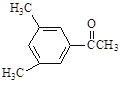 E.
E.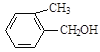 F.
F.![]()
(1)A物质中含有的官能团名称为_____________、______________。
(2)B的分子式为_________________。
(3)D的一氯代物最多有________________种。
(4)上述化合物中互为同分异构体的是_____;互为同系物的是____。(填字母)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇酸树脂固化成膜后具有良好的耐磨性和绝缘性,下面是一种成膜性良好的醇酸树脂的合成路线,如下图所示:
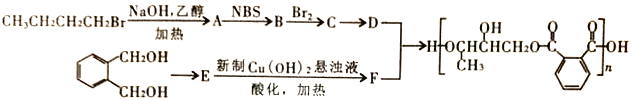
已知:①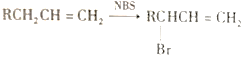 ②RCH=CH2
②RCH=CH2![]() RCH2CH2Br
RCH2CH2Br
(1)A的化学名称为________________,E中官能团的名称是__________________。
(2)B的结构简式为_______________,C制备D的反应条件是_____________,制备E的反应类型是_______________________。
(3)下列说法正确的是_________。
A.D是甘油的同系物
B.C是不溶于水的油状液体
C.F不能与新制氢氧化铜悬浊液反应
D.只用硝酸银溶液,就可以检出CH3CH2CH2CH2Br中是否含有溴原子
(4)写出D、F在一定条件下反应生成醇酸树脂的化学方程式________________________。
(5)芳香族化合物X是![]() 的同分异构体,X遇FeCl3溶液显紫色,可发生消去反应,其核磁共振氢谱显示有6 种不同化学环境的氢,峰面积比为1∶1∶1∶2∶2∶3。写出符合要求的X的结构简式________________。
的同分异构体,X遇FeCl3溶液显紫色,可发生消去反应,其核磁共振氢谱显示有6 种不同化学环境的氢,峰面积比为1∶1∶1∶2∶2∶3。写出符合要求的X的结构简式________________。
(6)请参考本题信息写出以CH3CH=CH2为原料制备化合物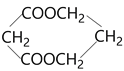 的合成线路流程图(无机试剂任选)。_______________
的合成线路流程图(无机试剂任选)。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g) ΔH1,平衡常数为K1;反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2;在不同温度K1、K2值如下表:
700 ℃ | 900 ℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
①反应CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=________(用ΔH1和ΔH2表示),K=________(用K1和K2表示)。
CO(g)+H2O(g) ΔH平衡常数为K,则ΔH=________(用ΔH1和ΔH2表示),K=________(用K1和K2表示)。
②能判断CO2(g)+H2(g)![]() CO(g)+H2O(g)达到化学平衡状态的依据是____(填字母)。
CO(g)+H2O(g)达到化学平衡状态的依据是____(填字母)。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO)=c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示。
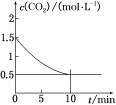
①该条件下反应的平衡常数为________;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为________ mol·L-1。
②下列措施中能使平衡时![]() 增大的是________(填字母)。
增大的是________(填字母)。
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com