
| A、2Na+2H2O=2NaOH+H2↑ |
| B、2Na2O2+2H2O=4NaOH+O2↑ |
| C、3NO2+H2O=2HNO3+NO |
| D、2Cl2+2H2O=4HCl+O2 |


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
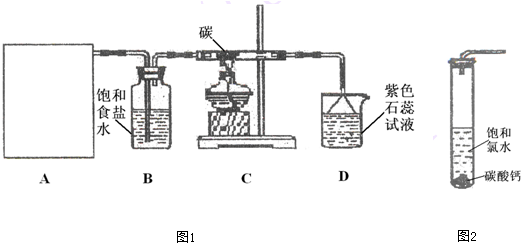
| 实验序号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KCl晶体、BaC03 |
| B、铁、二氧化硫 |
| C、液态的醋酸、乙醇 |
| D、熔融的K2SO4、盐酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、71 g氯相当于2 mol氯 |
| B、每摩尔物质中含有6.02×1023个原子 |
| C、阿伏加德罗常数为12 g 12C所含的碳原子数 |
| D、1 mol KClO3中含有3 mol氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极,被还原 |
| B、正极,被氧化 |
| C、负极,被还原 |
| D、负极,被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是① |
| B、具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,第一电离能最大的是③ |
| C、①Na、K、Rb ②O、S、Se ③Na、P、Cl,元素的电负性随原子序数增大而递增的是③ |
| D、某元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,18gH2O所含原子数为NA |
| B、常温常压下,11.2L氧气含原子数为NA |
| C、2.3g金属钠变为钠离子失去0.1NA电子 |
| D、在同温同压时,相同体积的任何气体单质都含有相同数目的原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com