
【题目】下列说法不正确的是( )
A.35Cl2与37Cl2互称同位素
B.白磷和红磷互为同素异形体
C.戊烷共有三种同分异构体,其沸点各不相同
D.(CH3)3CCH=CHCH3与H2加成反应后的产物名称是2,2-二甲基戊烷
科目:高中化学 来源: 题型:
【题目】草酸即乙二酸,是一种有机二元酸,在工业上有重要的作用。已知![]() 的电离常数:
的电离常数:![]() ,
,![]() ;
;![]() 电离常数:
电离常数:![]()
⑴![]() 溶液的pH______
溶液的pH______![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 。
。
⑵用惰性电极电解饱和草酸溶液可制得乙醛酸![]() 。阴极的电极反应式为_____。
。阴极的电极反应式为_____。
⑶草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸![]()
![]()
![]() 草酸钠晶体
草酸钠晶体
![]() 酒精的作用是________________。
酒精的作用是________________。
![]() 当草酸与碳酸钠的物质的量按2:1充分混合后,溶液中
当草酸与碳酸钠的物质的量按2:1充分混合后,溶液中![]() 。请将该溶液中离子浓度按由大到小的顺序排列______。
。请将该溶液中离子浓度按由大到小的顺序排列______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃A的相对分子质量为84。回答下列问题:
(1)烃A的分子式为_________。
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为__________。若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为__________。若烃B的相对分子质量比烃A小6,且B为最简单芳香族化合物,写出B与浓硝酸,浓硫酸混合共热的化学方程式__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O
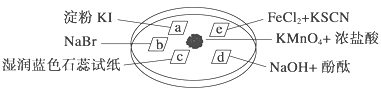
对实验现象的“解释或结论”正确的是 ( )
选项 | 实验现象 | 解释或结论 |
A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
C | d处立即褪色 | 氯气与水生成了漂白性物质 |
D | e处变红色 | 还原性:Fe2+>Cl- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用滴有酚酞和氯化钠溶液湿润的滤纸分别做甲、乙两个实验,下列判断错误的是( )

A.b极附近有气泡冒出B.d极附近出现红色
C.a、c极上都发生氧化反应D.甲中铁棒比乙中铁棒更易腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁带能在CO2中燃烧,生成氧化镁和单质碳。请完成下列填空:
(1)碳元素形成的单质有金刚石、石墨、足球烯等。金刚石的熔点远高于足球烯的原因是_______。
(2)氧化镁的电子式为_______,CO2的结构式为______。与镁同周期、离子半径最小的元素,其原子最外层的电子排布式为______,其1个原子中能量最高的电子有______个。
(3)一定条件下,在容积恒为2.0L的容器中,Fe和CO2发生如下反应:CO2(g)+Fe(s)![]() FeO(s)+CO(g),若起始时向容器中加入1molCO2,5.0min后,容器内气体的相对平均分子量为32,则n(CO2):n(CO)之比为_______,这段时间内用CO2表示的速率v(CO2)=_______。
FeO(s)+CO(g),若起始时向容器中加入1molCO2,5.0min后,容器内气体的相对平均分子量为32,则n(CO2):n(CO)之比为_______,这段时间内用CO2表示的速率v(CO2)=_______。
(4)下列说法错误的是_______。
a.当混合气体的密度不变时说明反应达到了平衡
b.混合气体的平均相对分子质量不变时说明反应达到了平衡
c.平衡后移除二氧化碳时,正反应速率一直减小直至建立新的平衡
d.平衡后缩小容器的体积,正逆反应速率不变,平衡不移动
(5)保持温度不变的情况下,待反应达到平衡后再充入一定量的二氧化碳,平衡向______移动(选填“正向”、“逆向”、或“不”),二氧化碳的转化率_____(填“增大”,“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组对一氧化碳还原氧化铁的实验中最后的产物产生浓厚兴趣,试通过实验来探究其成分。
Ⅰ、实验装置:

该装置B中发生的离子方程式是 ______,装置B的作用是 ______。
Ⅱ、实验现象:玻璃管A中的粉末由红色逐渐变为黑色时,停止加热,继续通一氧化碳,冷却到室温,停止通气,同时观察到澄清的石灰水变浑浊。
Ⅲ、实验结论:
甲认为:依据上述实验现象可以判断出生成的黑色固体为金属铁。
乙认为:仅从上述实验现象,不足以证明生成的黑色固体为金属铁,他增加一个实验:用磁铁靠近黑色固体,看到有黑色固体被磁铁吸引,于是得出生成的黑色固体为金属铁的结论。
请你通过该反应的相关资料对他们的结论作出判断,并通过实验检验其合理性:
⑴在一定条件下,一氧化碳与氧化铁在加热条件下,可发生如下反应:
CO +3Fe2O3 = 2Fe3O4+ CO2↑ 4CO + Fe3O4 = Fe+ 4CO2↑
⑵四氧化三铁(Fe3O4)为黑色固体,有强磁性,能够被磁铁吸引。
甲、乙同学的结论 ______。你对此评价的理由是 ______。
Ⅳ、实验探究
对反应后固体成分提出假设:
假设1:反应后固体中只有Fe;
假设2:反应后固体中只有Fe3O4;
假设3:反应后固体中 ______ 。
为确定实验中最后产物中的成分,丙同学设计如下实验,请你利用限选试剂和仪器帮助他完成该探究过程,并将答案写在答题卡相应位置。
限选试剂和仪器:1mol/L CuSO4、0.01mol/L KSCN溶液、1mol/L 盐酸、0.01mol/L 氨水、试管、玻璃棒、胶头滴管。
实验操作 | 预期现象和结论 |
步骤一;取硬质玻璃管中固体产物少量分别于A、B试管中,加入足量1mol/L CuSO4溶液,搅拌溶解。 | ⑴若A试管中黑色固体不溶解,并且没有观察到其它现象,则黑色固体为 ______。 ⑵若B试管中有红色固体析出,则说明黑色固体中含有 ______。 |
步骤二:对试管B中溶液过滤,将所得固体洗涤干净后加足量1mol/L盐酸后再依次分别加入适量0.01mol/L氨水、少量0.01mol/L KSCN溶液。 | ①若溶液不变红色,则______。 ②若溶液变红色,则______。 |
Ⅴ、延伸探究:丁同学试图通过反应前后固体质量的变化来确定黑色固体的成分,你认为可行吗?(假设氧化铁在反应中完全反应)______(填“行”或“不行”),理由是:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室处理含FeBr3废催化剂的溶液,可得到溴的苯溶液和无水FeCl3。下列做法能达到相应实验目的的是( )
A. 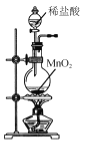 制取Cl2
制取Cl2
B. 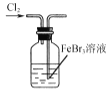 使Br-转化为Br2
使Br-转化为Br2
C.  分液,先放出水层,再倒出溴的苯溶液
分液,先放出水层,再倒出溴的苯溶液
D.  将分液后的水层蒸干获得无水FeCl3
将分液后的水层蒸干获得无水FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一支硬质大试管,通过排饱和![]() 溶液的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是( )。
溶液的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是( )。
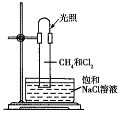
A.反应过程中试管内黄绿色逐渐消失,试管壁上有油珠产生
B.甲烷和![]() 反应后的产物有4种
反应后的产物有4种
C.盛放饱和![]() 溶液的水槽底部不会有晶体析出
溶液的水槽底部不会有晶体析出
D.![]() 和
和![]() 完全反应后液面上升,液体充满试管
完全反应后液面上升,液体充满试管
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com