
【题目】如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色。下列说法正确的是
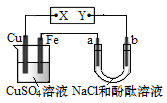
A.X是负极,Y是正极
B.CuSO4溶液的pH减小
C.a极产生的气体能使湿润的红色石蕊试纸先变红后褪色
D.若电路中转移了0.02 mol e-,Fe电极增重0.64g
【答案】CD
【解析】
a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则b电极上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,则b是阴极、a是阳极,所以Y是负极、X是正极,Cu是阳极,Fe是阴极,电解时,阳极上Cu失电子变成Cu2+、阴极上铜离子得电子,据此分析解答。
a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则b电极上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,则b是阴极、a是阳极,所以Y是负极、X是正极,Cu是阳极,Fe是阴极,电解时,阳极上Cu失电子变成Cu2+、阴极上铜离子得电子。
A. 通过以上分析知,Y是负极、X是正极,故A错误;
B. 电解时,左边装置阳极上为Cu失电子变成Cu2+,阴极Fe上为Cu2+得到电子被还原成Cu,所以CuSO4溶液的pH不变,故B错误;
C. a是阳极,电解质溶液中的氯离子失电子,a极产生氯气,氯气与水反应生成盐酸和次氯酸,湿润的红色石蕊试纸先变红后褪色,故C正确;
D. Fe是阴极,阴极上铜离子得电子生成铜单质,电极反应为Cu2++2e-=Cu,若电路中转移了0.02 mol e-时,Fe电极上生成0.01mol的铜单质,质量为0.64g, Fe电极增重0.64g,故D正确;
答案选CD。


科目:高中化学 来源: 题型:
【题目】[化学—选修3:物质结构与性质] 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为YBaCu3O7,其中1/3的Cu以罕见的Cu3+形式存在。Cu在元素周期表中的位置为_______,基态Cu3+的核外电子排布式为____________。
(2)磁性材料在生活和科学技术中应用广泛。研究表明,若构成化合物的阳离子有未成对电子时,则该化合物具有磁性。下列物质适合作录音磁带磁粉原料的为____(填选项字母)。
A.V2O5 B.CrO2 C.PbO D.ZnO
(3)屠呦呦因在抗疟药——青蒿素研究中的杰出贡献,成为首获科学类诺贝尔奖的中国人。青蒿素的结构简式如图l所示,其组成元素的电负性由大到小的顺序为___________;碳原子的杂化方式有_______。
(4)“可燃冰”因储量大、污染小被视为未来石油的替代能源,由甲烷和水形成的“可燃冰”结构如图2所示。
①“可燃冰”中分子间存在的2种作用力为________________。
②H2O的VSEPR模型为___________,比较键角的大小:H2O_______CH4(填“>”“<”或“=”),原因为___________________________________。
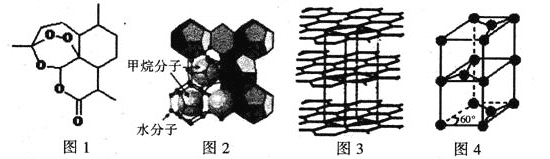
(5)锂离子电池在便携式电子设备以及电动汽车、卫星等领域显示出广阔的应用前景,该电池负极材料为石墨,石墨为层状结构(如图3),其晶胞结构如图4所示,该晶胞中有__________个碳原子。已知石墨的层间距为apm,C-C键长为b pm,阿伏伽德罗常数的值为NA,则石墨晶体的密度为_________________g·cm-3(列出计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.水是弱电解质,电离方程式为H2O+H2O![]() H3O++OH-
H3O++OH-
B.常温下,向水中加入H2SO4溶液,H+ 浓度增大,Kw增大
C.将纯水加热到100℃,pH≈6,显酸性
D.常温下,将0.1mol·L-1的 NaOH溶液体积稀释到原来的10倍,则pH=12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氮的变化关系图如下,则下列说法不正确的是
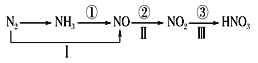
A.路线①②③是工业生产硝酸的主要途径
B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C.上述所有反应都是氧化还原反应
D.氮气在足量的氧气中通过一步反应可生成NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某锂离子电池充电时的工作原理如图所示,LiCoO2中的Li+穿过聚内烯微孔薄膜向左迁移并嵌入石墨(C6表示)中。下列说法错误的是( )
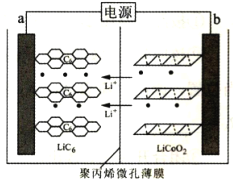
A.充电时,阳极电极反应式为LiCoO2-xe-=xLi++Lil-xCoO2
B.放电时,该电池将化学能转化为电能
C.放电时,b端为负极,发生氧化反应
D.电池总反应为LixC6+Lil-xCoO2![]() C6+LiCoO2
C6+LiCoO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】遵义市某些地区出现了不同程度的雾霾天气,我校课题小组的同学对其进行了调查研究,
Ⅰ.课题小组研究发现,其中首要污染物为可吸入颗粒物PM2.5,其主要来源为燃煤、机动车尾气等。
(1)25℃时将PM2.5样本用蒸馏水处理制成待测溶液。测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
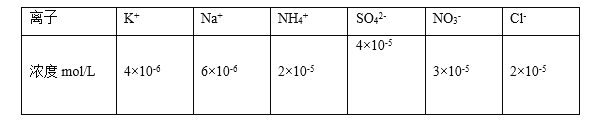
根据表中数据判断试样的pH=________。
Ⅱ.课题组就其酸性物质做进一步研究
一氧化氮、二氧化氮的研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应:
2NO(g)+O2(g) ![]() 2NO2(g),下列状态能说明该反应达到化学平衡的是_______(填字母编号)。
2NO2(g),下列状态能说明该反应达到化学平衡的是_______(填字母编号)。
A.混合气体的密度保持不变 B.NO的转化率保持不变
C.NO和O2的物质的量之比保持不变 D.O2的消耗速率和NO2的消耗速率相等
(2)活性炭可处理大气污染物NO,反应原理为:C(s)+2NO(g)![]() N2(g)+CO2(g),T℃时,在2L密闭容器中加入0.100mol NO和2.030mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol,则该温度下的平衡常数为_________;达平衡时,若再向容器中充入0.04molNO,0.03molN2和0.03molCO2,则平衡________移动。(填“向左”“向右”或“不”)
N2(g)+CO2(g),T℃时,在2L密闭容器中加入0.100mol NO和2.030mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol,则该温度下的平衡常数为_________;达平衡时,若再向容器中充入0.04molNO,0.03molN2和0.03molCO2,则平衡________移动。(填“向左”“向右”或“不”)
III.一氧化碳、二氧化碳的研究
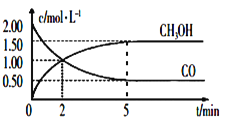
(1)CO或CO2在一定条件下可以用来合成甲醇。工业上常用CO和H2制备CH3OH的反应为:CO(g)+2H2(g)![]() CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到5min,用H2表示的平均反应速率v(H2)=_____。
CH3OH(g),在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。从反应开始到5min,用H2表示的平均反应速率v(H2)=_____。
(2)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △ H=+131.0kJ/mol
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △ H= - 43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(S) △ H= - 178.3kJ/mol
①计算反应Ⅳ:C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)的△H=______kJ/mol;
CaCO3(s)+2H2(g)的△H=______kJ/mol;
对硫的氧化物的研究
②SO2可被Na2FeO4氧化而去除污染,工业上用Fe和石墨作电极电解浓NaOH溶液制备Na2FeO4。写出电解过程中阳极发生的电极反应________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 A、B、C、D、E 五种主族元素分属三个短周期,且原子序数依次增大。A、C 同主族,可形成离子化合物 CA;B、D 同主族,可形成 DB2、DB3 两种分子。请回答下列问题:
(1)五种元素原子半径由小到大的顺序为_______________(用元素符号回答)。
(2)A、B 两种元素能形成既含极性键又含非极性键的化合物 M,M 的电子式为_______________。
(3)非金属性强弱:D_______________E(填“>”“<”),用离子方程式表示__________________________。
(4)写出均由 A、B、C、D 四种元素组成的两物质的浓溶液发生反应的离子方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a曲线表示一定条件下X(g)+Y(g)![]() 2Z(g)+W(s) △H<0的反应过程。若使a曲线变为b曲线,可采用的措施是 ( )
2Z(g)+W(s) △H<0的反应过程。若使a曲线变为b曲线,可采用的措施是 ( )
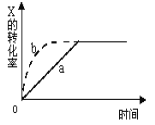
A.加入催化剂B.增大Y的浓度C.降低温度D.增大体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯碱工业是基本无机化工之一。完成下列填空:
(1)常温下向纯碱溶液中滴加酚酞试液,溶液变红,原因是___(用离子方程式表示);继续滴加足量氯化钡溶液,可以看到__。
(2)最早的勒布朗法制碱涉及如下反应:Na2SO4+2C+CaCO3![]() Na2CO3+CaS+2CO2↑。该反应中被还原的元素是___。若转移6.02×1024个电子,生成CO2在标准状况下的体积为__L。
Na2CO3+CaS+2CO2↑。该反应中被还原的元素是___。若转移6.02×1024个电子,生成CO2在标准状况下的体积为__L。
(3)索尔维法(氨碱法)是工业生产纯碱的主要方法,其主要原理可以表示为:NaCl(饱和)+H2O+CO2+NH3=NaHCO3↓+NH4Cl。该反应涉及的各物质中,属于弱电解质的是___。综合平衡理论解释通入CO2和NH3后为何会有NaHCO3析出___。
(4)侯德榜对索尔维法进行了改进,利用平衡移动原理从析出NaHCO3后的母液中提取NH4Cl产品,所需的物质有___(填化学式)。
(5)纯碱厂在生产过程中要时刻关注设备的腐蚀情况。输送饱和食盐水的铸铁管道受到腐蚀时,正极的电极反应方程式为:___。为缓解腐蚀,可在铸铁管道上固定铝-锌-镉三元合金,该方法称为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com