
����Ŀ��I ����HCl����״��������ƿ������Ȫʵ���õ���ϡ������Һ���ñ�����������Һ�ζ�����ȷ����ϡ�����ȷ���ʵ���Ũ�ȡ��ش��������⣺
��1���õζ�ʵ��ʢװ��Һ��������__________�� ��������������Ϊ50mL����Һ��Ϊ0����������������Һ��ų�����ų�����Һ���_______50mL���������������������������
��2�����õζ�ʵ���÷�̪��ָʾ�����ﵽ�ζ��յ�ʱ����Һ��ɫ��____ɫ��Ϊ____ɫ�ұ���30s�ڲ���ɫ��
��3���������ֲ�ͬŨ�ȵı�����������Һ������Ϊ����ʵ��ǵ�______�֡�
��5.000 mol/L ��0. 5000 mol/L ��0.0500 mol/L
��4���������������ʵı�����������Һ�ζ�ϡ���ᣬ��������������ζ����ʵ���������£�
ʵ���� | ��������������mL�� | ��������������Һ�������mL�� |
1 | 20.00 | 17.30 |
2 | 20.00 | 17.02 |
3 | 20.00 | 16.98 |
���õ�ϡ��������ʵ���Ũ��Ϊ_________________________��
II ��Ѫ�Ƶĺ���ʱ���ɽ�2��0 mLѪҺ������ˮϡ�ͺ������м������������(NH4)2C2O4���壬��Ӧ����CaC2O4��������������ϡ���ᴦ����H2C2O4����������KMnO4��Һ�ζ�����������ΪCO2����ԭ����ΪMn2+�����յ�ʱ��ȥ20��0 mL 1��0��10-4 mol��L-1��KMnO4��Һ��
��1��д����KMnO4�ζ�H2C2O4�����ӷ���ʽ______________��
��2���жϵζ��յ�ķ�����______��
��3�����㣺ѪҺ�к������ӵ�Ũ��Ϊ____g��mL-1��
���𰸡���ʽ�ζ��� > ��ɫ ��ɫ �� 0.04250 mol/L 2MnO4-+5H2C2O4+6H+2Mn2++10CO2��+8H2O ������һ������KMnO4��Һ����Һ����ɫ��Ϊdz��ɫ���Ұ�����ڲ���ɫ 1��0��10-4
��������
I��1���õζ�ʵ��ʢװ������������Һ�������Ǽ�ʽ�ζ��ܣ� ��������������Ϊ50mL����Һ��Ϊ0����������������Һ��ų������ڵζ���50�̶����µ�Һ��Ҳ�ų�����ų�����Һ�������50mL��
��2�����õζ�ʵ���÷�̪��ָʾ�����ﵽ�ζ��յ�ʱ����Һ��ɫ����ɫ��Ϊ��ɫ�ұ���30s�ڲ���ɫ��
��3������HCl����״��������ƿ������Ȫʵ���õ���ϡ������Һ��������������ʵ���Ũ��Ϊc(HCl)=![]() ��Ϊ�������Ӧ��Ũ����֮�ӽ�������������Һ���еζ����ʴ�ѡ����
��Ϊ�������Ӧ��Ũ����֮�ӽ�������������Һ���еζ����ʴ�ѡ����
��4�����ݱ������ݿ�֪����1���������ƫ��Ӧ��ȥ����������������Ƶ�ƽ�����Ϊ![]() �����c(HCl)=
�����c(HCl)=![]() ��
��
II��1���������⣬������غͲ��ᷴӦ���ɶ�����̼�������ӣ������е�̼Ԫ�ش�+3�����ߵ�+4�ۣ���Ԫ�ش�+7�۽��͵�+2�ۣ����������ӺͲ���ļ�����Ϊ2��5���ٸ���ԭ���غ��������ƽ�������ӷ���ʽΪ2MnO4-+5H2C2O4+6H+2Mn2++10CO2��+8H2O��
��2�����������ҺΪ��ɫ���ζ��յ�Ϊ������һ������KMnO4��Һ����Һ����ɫ��Ϊdz��ɫ���Ұ�����ڲ���ɫ��
��3�����ݷ���ʽ����
2MnO4----5H2C2O4 ----5Ca2+
2 5
20��1.0��10-4 c��2
��c=2.5��10-3mol/L����ѪҺ�к������ӵ�Ũ��Ϊ2.5��10-3mol/L ��40g/mol��10-3L/mL=1.0��10-4g��mL-1��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaH2PO2(��������)������ˮ��ˮ��Һ�����ԣ�����ǿ��ԭ�ԣ������ڻ�ѧ�������������ȡ�һ����������(��P4������CaO��Fe2O3��Al2O3��CaCl2��)Ϊԭ���Ʊ�NaH2PO2��H2O�Ĺ����������£�
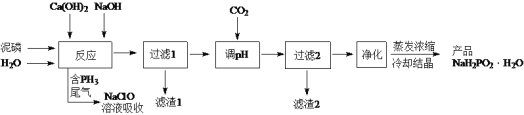
��֪P4�����ּ�ķ�Ӧ��Ҫ�У�
��. 2Ca(OH)2+P4+4H2O=2Ca(H2PO2)2+2H2��
��. 4NaOH + P4+8H2O = 4NaH2PO2��H2O+2H2��
��. 4NaOH + P4+2H2O = 2Na2HPO3 +2PH3��
��. NaH2PO2+NaOH = Na2HPO3+H2��
(1)β���е�PH3��NaClO��Һ��������NaH2PO2��NaCl�����ӷ���ʽΪ_____��
(2)����Ӧ�����¶Ⱥ�ˮ��һ��ʱ����ϼ������ʵ�����P4�����ʵ���֮��[n(��)/ n(��)]��NaH2PO2���ʵĹ�ϵ��ͼ��ʾ����n(��)/ n(��)��2.6ʱ��NaH2PO2�IJ�����n(��)/ n(��)����������͵Ŀ���ԭ����_____��

(3)ͨCO2����pH������Һ��pHԼΪ_____������2��Ҫ�ɷ�Ϊ_____(�ѧʽ)��
(4)������2������Һ����Ag2SO4��Ba(OH) 2��Na2S��Һ��ȥ����Cl����Fe2+�ȣ����м����Ag2SO4��Һ���˹���̫�࣬����Ҫԭ����_____��
(5)��NiCl2��NaH2PO2��Һ��ѧ��Ni��ͬʱ����H3PO4���Ȼ���Ļ�ѧ����ʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�Ksp(CaSO4)=9��10-6�������£�CaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ�������жϴ������

A. a��c��������Ա�ʾ������CaSO4����ˮ���γɵı�����Һ
B. a���Ӧ��Ksp����c���Ӧ��Ksp
C. b�㽫�г������ɣ�ƽ�����Һ��c(SO42-)һ��������3��10-3molL-1
D. ��d����Һ�м�������CaCl2������Ա䵽c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʹ�ý�������ʷ�����絽����˳����
A.����ͭ����B.ͭ��������C.ͭ��������D.��������ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У��������(����)
A. Ԫ�����ڱ�����7�����塢7������B. ϡ������Ԫ��ԭ�ӵ�������������Ϊ8��
C. ̼Ԫ��λ�ڵ�2����IVA��D. ������еĻ�ѧ���ǹ��ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��ԭ��������������������Ԫ�طֱ�λ�ڲ�ͬ�����壬���ǵĵ��ʳ����¾�����̬��X��Y��W���ڲ�ͬ���ڣ�����һ���������䵥���ܷ�����Ӧ��X2+Y2���ף�X2+W2���ң���֪���ס��ҳ����¾�Ϊ��̬���������ڿ���������ʱ�ɻ��ϳɱ����Իش��������⣺
(1)Y��Z��Ӧ���⻯��Ƚ��ȶ����ǣ�_____________��(�ѧʽ)
(2)�����������_____����(�������)����ˮ��Һ�����ԣ������ӷ���ʽ��ʾ��ԭ��___��
(3)X��Z�������ԭ�ӻ����ﶡ�����������Ļ�ѧ������Ϊ��____________������˵�������ﶡ��һ�ֳ�����;��__________________________��
(4)X��Y��ɵĻ�����Y2X4������Z2��������Ч��ȼ�ϵ�أ����������ҺΪNaOH��Һ���������ĵ缫��ӦʽΪ��__________________________��
(5)һ�������£�ȡ 3.4 g����������1 L���ݵ������У�4���Ӻ������ڵ�ѹǿ��Ϊԭ����1.2�����Ҳ��ٱ仯���÷�Ӧ�м������ת����Ϊ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ����������������ԭ�����͵���
A. ��ˮ����ƽ�⣺Br2+ H2O ![]() HBr+ HBrO�������� AgNO3��Һ����Һ��ɫ��dz
HBr+ HBrO�������� AgNO3��Һ����Һ��ɫ��dz
B. ��CO + NO2 ![]() CO2+ NO��ƽ����ϵ����ѹǿ��ʹ��ɫ����
CO2+ NO��ƽ����ϵ����ѹǿ��ʹ��ɫ����
C. �ڵ�⺬�з�̪����������Һʱ������������Һ����ɫ���
D. �ϳ� NH3��Ӧ��Ϊ��� NH3�IJ��ʣ�������Ӧ��ȡ��Խϵ��¶ȵĴ�ʩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У���Ӧ���������С�������������������
A. ����ȼ��B. ���ȷ�ӦC. ̼��Ʒֽ�D. ����к�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ�����1996��8�£��ҹ���ѧ���״��Ƴ�һ���º����ѡ�235����֪�ѣ�Am����ԭ������Ϊ95�����й���![]() ��������ȷ����
��������ȷ����
A. �ѡ�235���ˡ�235������ͬ��������
B. �ѡ�235��ԭ��������12Cԭ��������235��
C. �ѡ�235ԭ�Ӻ���������Ϊ140�����������Ϊ95
D. �ѡ�235ԭ��һ�������з�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com