
【题目】下列变化是氧化还原反应的是
A.CaO+CO2=CaCO3B.SiO2+2NaOH=Na2SiO3+H2O
C.NH4HCO3![]() NH3↑+H2O+CO2↑D.2FeSO4
NH3↑+H2O+CO2↑D.2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
科目:高中化学 来源: 题型:
【题目】假设烷烃的通式为![]() ,以下物理量随n的增加而减小的是 ( )
,以下物理量随n的增加而减小的是 ( )
A. 1mol烷烃中共价键的数目B. 1mol烷烃完全燃烧时的耗氧量
C. 一氯代物的种类D. 氢元素的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)绿色植物是空气天然的“净化器”,在家里科学选种一些绿色植物,可以达到净化空气、吸收有害物质的作用。科学研究发现,1公顷柳杉每月可以吸收160 kg SO2,则1公顷柳杉每月吸收的SO2的物质的量为________。
(2)铅笔芯的主要成分是石墨和黏土,这些物质按照不同的比例加以混合、压制,就可以制成不同型号的铅笔芯。如果某铅笔芯质量的一半成分是石墨,且用铅笔写一个字消耗的质量约为1 mg。那么一个铅笔字含有的碳原子数约为________。
(3)吸食“摇头丸”会严重破坏人体的中枢神经,“摇头丸”的化学式为C9H13N,请计算:
①“摇头丸”的摩尔质量为________;
②某毒枭被查获带有270 g“摇头丸”,该毒枭所带的“摇头丸”的物质的量为________。
(4)将14.3 g Na2CO3·10H2O固体溶于水配成250 mL溶液,则所得溶液物质的量浓度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
①水的摩尔质量是18g
②0.5molH2的体积为11.2L
③1 mol 水中含有 2 mol 氢和 1mol 氧
④1mol 任何物质都约含有6.02×1023个分子
⑤0.5mol H2SO4含有的原子数目为3.5NA
⑥只有在标准状况下,体积相同的任何气体所含的分子数相同
⑦质量分数为40%的硫酸溶液与等体积的水混合,所得溶液浓度大于20%
⑧物质的量浓度为4mol/L 的硫酸溶液与等质量的水混合,所得溶液浓度小于2mol/L
A. ①③④⑤⑦⑧ B. ②⑤⑦⑧ C. ⑤⑦⑧ D. ⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知十种物质:①H2O ②空气 ③ Mg ④ CaO ⑤H2SO4 ⑥氢氧化钡⑦饱和FeCl3溶液 ⑧氨水 ⑨HNO3 ⑩胆矾,根据上述提供的物质,回答下列问题:
(1)属于混合物的是__________ (填序号,下同),属于电解质的是__________ 。
(2)上述物质中__________与__________在水溶液中可发生反应,且离子方程式为H++OH-=H2O。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________,反应的离子方程式为__________;证明有Fe(OH)3胶体生成的实验操作及现象是__________
(4)实验室配制900mL 0.1mol/L硫酸铜溶液,需要称取的溶质(从上述物质中选取)的质量为__________g,从配制好的溶液中取出300mL,其中含有SO42-的数目为__________(设
NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是
A.5.6g铁在足量氯气中燃烧,铁失去电子数为0.2NA
B.常温常压下,32gO2和O3的混合气体所含原子数为2NA
C.9g重水(2H216O)中含有的电子数为5NA
D.0.5 mol/L MgCl2溶液中,含有的Cl-个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,一定体积的容器中发生反应:A(s)+3B(g)![]() 2C(g)+2D(g),下列描述中能说明该反应达到平衡的是( )
2C(g)+2D(g),下列描述中能说明该反应达到平衡的是( )
①A的质量不发生变化 ②单位时间内生成a mol A,同时消耗2a mol C
③容器中的压强不再变化 ④混合气体的密度不再变化
⑤n(A):n(B):n(C):n(D)=1:3:2:2 ⑥B的浓度不变
A. ①③⑤⑥B. ①③④⑥C. ②④⑤D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化钠可用作碘的助溶剂,是制备碘化物的原料。化学实验小组用NaOH、单质碘和水合肼(N2H4·H2O)为原料制备碘化钠。
已知:①水合肼(N2H4·H2O)的沸点118℃,100℃开始分解;具有强还原性。②I-、IO3-在碱性条件下共存,酸性条件下反应生成I2。化学实验小组用下图所示装置制备碘化钠,实验步骤如下:
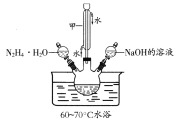
Ⅰ.制备水合肼:用:NaC1O氧化NH3制得水合肼,并将所得溶液装入上述装置左侧分液漏斗。
Ⅱ.向三颈烧瓶中加入一定量单质碘,打开右侧分液漏斗活塞,加入足量NaOH溶液,保持60~70℃水浴,充分反应得到NaI和NaIO3的混合溶液。
Ⅲ.打开左侧分液漏斗活塞,将水合肼溶液加入三颈瓶,并保持60~70℃水浴至反应充分。
Ⅳ.向Ⅲ所得溶液中加入适量活性炭,煮沸半小时,过滤,从滤液中分离出产品。
回答下列问题:
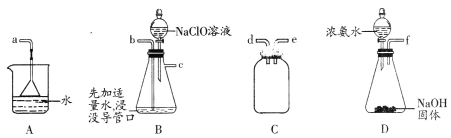
(1)仪器甲的名称是________________。
(2)用下图所示装置制备水合肼:
①仪器的接口依次连接的合理顺序是________________________(用字母表示)。
②实验过程中,需要缓慢滴加NaC1O溶液的主要原因是____________________________。
(3)步骤Ⅲ中温度保持在70℃以下的原因是_______________________________________。
(4)步骤Ⅳ中分离出产品的操作是_____________________、洗涤、干燥。
(5)设计方案检验步骤Ⅲ所得溶液中含有NaIO3:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,下列各组离子一定能大量共存的是( )
A.滴入石蕊试液显红色的溶液:K+、Mg2+、AlO2、SO32
B.1.0mol·L1的KNO3溶液:H+、Fe2+、Cl、SO42
C.在![]() =1×1012的溶液中:NH4+、Fe2+、Cl-、NO3
=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3
D.通入足量CO2的溶液:Ca2+、Cl、K+、Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com