
【题目】实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是
A. 950mL 111.2 g B. 500mL 117.0 g
C. l000mL 117.0 g D. 任意规格 111.2 g
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W和N均是由短周期元素组成的五种化合物.已知五种化合物水溶液的焰色反应均呈黄色,Y、Z和N均由三种元素组成.请根据题目要求回答下列问题.
(1)固体化合物X为浅黄色粉末,该化合物中含有的化学键有(填序号).
A.离子键
B.极性共价键
C.非极性共价键
D.氢键
(2)写出X与二氧化碳反应的化学方程式 .
(3)下表为Y与Z实验的部分内容:
序号 | 主要实验步骤及实验现象 |
① | 在含Y的溶液中,加入稀硫酸放置,产生浅黄色沉淀和无色有刺激性气味的气体,该气体可使品红溶液褪色 |
② | 在含Z的溶液中,滴加盐酸,开始有白色沉淀,继续滴加盐酸,白色沉淀先增加后消失,然后加入过量的氨水又出现白色沉淀 |
③ | 将实验②最终得到的混合物加热蒸发、灼烧,最终得到白色固体 |
写出Y与稀硫酸反应的离子方程式 .
(4)写出含0.1mol Z的溶液与20mL 5molL﹣1的盐酸反应的离子反应式 . 实验③加热蒸发、灼烧得到的最终产物主要是 .
(5)化合物W和N可以相互转化:W ![]() N.若有W和NxH2O的混合物6.52g,加热到完全反应后,气体产物通过浓硫酸增重1.71g,剩余气体通过碱石灰增重1.10g,则混合物中W的质量为 , NxH2O的化学式为 .
N.若有W和NxH2O的混合物6.52g,加热到完全反应后,气体产物通过浓硫酸增重1.71g,剩余气体通过碱石灰增重1.10g,则混合物中W的质量为 , NxH2O的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列仪器和药品制取干燥纯净的氯气.
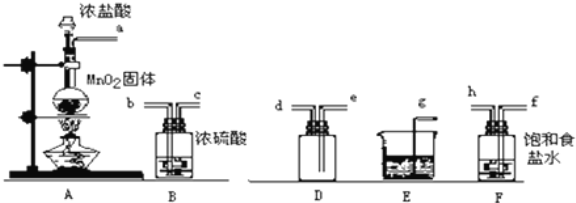
(1)按气流从左到右,装置正确的连接顺序:a接 接 接 接 接 接 接(填各接口字母)____________
(2)装置F的作用是____,装置E的作用是____.
(3)装置A和E中的反应化学方程式为(每空2分):A___.E____.
(4)若有8.7gMnO2参加了反应,将产生的氯气通入足量的KI溶液中能产生单质碘的质量____g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应MnO2+4HCl(浓)==MnCl2+Cl2↑+2H2O,_____元素化合价降低,_______电子,发生_______反应,被_________;氧化剂是_____________,氧化产物是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时Agl饱和溶液中c(Ag+)为1.22×10﹣6mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10﹣6mol/L.若在5mL含有KCl和KI各为0.01mol/L的溶液中,加入8mL0.01mol/LAgNO3溶液,这时溶液中所含溶质的离子浓度大小关系正确的是( )
A.c(K+)>c(NO![]() )>c(Cl﹣)>c(Ag+)>c(I﹣)
)>c(Cl﹣)>c(Ag+)>c(I﹣)
B.c(K+)>c(NO![]() )>c(Ag+)>c(Cl﹣)>c(I﹣)
)>c(Ag+)>c(Cl﹣)>c(I﹣)
C.c(NO3﹣)>c(K+)>c(Ag+)>c(Cl﹣)>c(I﹣)
D.c(K+)>c(NO ![]() )>c(Ag+)=(Cl﹣)+c(I﹣)
)>c(Ag+)=(Cl﹣)+c(I﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25℃时0.1mol/L的氨水.请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 ![]() (填“增大”、“减小”或“不变”);
(填“增大”、“减小”或“不变”);
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式;所得溶液的pH7(填“>”、“<”或“=”),用离子方程式表示其原因;
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol/l,则c(SO ![]() )=;
)=;
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子物质的量浓度由大到小的关系是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在5NH4NO3═ 2HNO3+4N2↑+9H2O中,发生氧化反应的氮原子和发生还原反应的氮原子的质量比是
A. 1:1 B. 3:5 C. 5:3 D. 2:8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学设计了如下实验装置并开展研究(部分夹持装置已略去)。
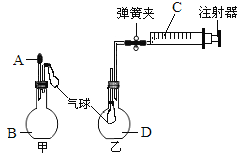
(1)当将A慢慢滴入甲瓶后,观察到甲瓶上的气球慢慢鼓起,则A和B分别可能是下列组合中的______(填选项序号)。
①稀硫酸和NaHCO3溶液 ②浓硫酸和NaOH溶液
③NaCl溶液和KNO3溶液 ④蒸馏水和NH4NO3固体
(2)将少量C慢慢推入乙瓶。
①若观察到乙瓶内的气球慢慢鼓起,且C为蒸馏水,则气体D可能为________(任填一种物质的化学式)。
②若C为O2,气体D为NO,则能观察到乙瓶中的现象是____________________。
(3)若他们利用下图所示装置进行实验。
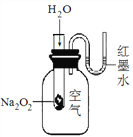
①将水滴入试管后能观察到的现象为________________,这是因为该反应为____________反应(填“放热”或“吸热”),反应物的总能量比生成物的总能量____________(填“高”或“低”,下同),反应物化学键断裂时吸收的总能量________于生成物化学键形成时放出的总能量。
②该反应的化学方程式为_______________________________,反应中能量的主要转化形式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做如下实验,以检验反应中的能量变化.
实验中发现反应后(a)中温度升高,由此可以判断(a)中反应是________热反应;(b)中温度降低,根据能量守恒定律,(b)中反应物的总能量应该________其生成物的总能量.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com