
【题目】(1)根据有机化合物分子中所含官能团,可对其进行分类和性质预测。
①下列有机化合物属于醇类物质的是____(填字母)。
a.CH3CH2OH b.CH3CHO c.![]()
②下列有机化合物中加入浓溴水能生成白色沉淀的是____(填字母)。
a.CH2=CH2 b.苯 c.![]()
③下列有机化合物能发生水解反应的是____(填字母)。
a.乙酸 b.油脂 c.葡萄糖
(2)有机物W(![]() )广泛存在于肉桂类植物的果肉中。
)广泛存在于肉桂类植物的果肉中。
①W分子中所含官能团的名称为____和____。
②W分子中处于同一平面的碳原子最多有____个。
③1mol W分子最多能与____mol H2发生加成反应。
(3)对羟基苯甲酸乙酯( )是常用的食品防腐剂,可通过以下方法合成:
)是常用的食品防腐剂,可通过以下方法合成:
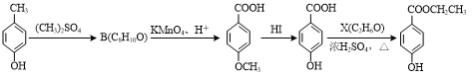
A C D E
①C→D的反应类型为____。
②B的结构简式为____。
③D与碳酸氢钠反应后所得有机物的结构简式为____。
④D→E反应的化学方程式为____。
⑤写出同时满足下列条件的C的一种同分异构体的结构简式:____。
Ⅰ.能和FeCl3溶液发生显色反应;
Ⅱ.能发生银镜反应,不能发生水解反应;
Ⅲ.分子中含有4种不同化学环境的氢原子。
【答案】a c b 碳碳双键 醛基 9 5 取代反应 ![]()
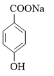

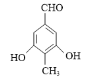 或
或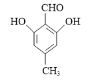
【解析】
(1)①含-CHO的有机物为醛;
②苯酚与溴水反应生成白色沉淀;
③油脂可发生水解反应;
(2)①根据结构简式进行判断;
②根据甲醛分子中四个原子共平面、乙烯六个原子共平面、苯分子中十二个原子共平面判断;
③W分子中含有一个苯环、一个碳碳双键和一个醛基;
(3)①C发生取代反应生成D;
②根据对甲基苯酚与(CH3)2SO4发生发生取代反应生成B,结合B的分子式、C的结构简式推出B的结构简式;
③D中只有羧基能与碳酸氢钠反应;
④D和乙醇在浓硫酸作催化剂、加热条件下发生酯化反应生成酯;
⑤C的同分异构体符合:
Ⅰ.能和FeCl3溶液发生显色反应;
Ⅱ.能发生银镜反应,不能发生水解反应;
Ⅲ.分子中含有4种不同化学环境的氢原子。
(1)①含-CHO的有机物为醛,a、b、c分别为醛、醇、羧酸,故答案为:a;
②苯酚与溴水反应生成白色沉淀,而乙烯与溴水发生加成反应,苯与溴水不反应,故答案为:c;
③油脂可发生水解反应,葡萄糖为单糖不能水解,乙酸不能发生水解反应;故答案为:b;
(2)①W(![]() )分子中所含官能团的名称为碳碳双键和醛基;
)分子中所含官能团的名称为碳碳双键和醛基;
②根据甲醛分子中四个原子共平面、乙烯六个原子共平面、苯分子中十二个原子共平面可知,W分子中处于同一平面的碳原子最多有9个;
③W分子中含有一个苯环、一个碳碳双键和一个醛基,故1mol W分子最多能与5mol H2发生加成反应;
(3)①C发生取代反应生成D,反应类型是取代反应;
②根据对甲基苯酚与(CH3)2SO4发生发生取代反应生成B,结合B的分子式C8H10O、C的结构简式推出B的结构简式为![]() ;
;
③D中只有羧基能与碳酸氢钠反应生成羧酸钠,生成的物质的结构简式为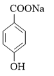 ;
;
④D和乙醇在浓硫酸作催化剂、加热条件下发生酯化反应生成酯,反应的化学方程式为 ;
;
⑤C的同分异构体符合:Ⅰ.能和FeCl3溶液发生显色反应,说明含有酚羟基;Ⅱ.能发生银镜反应,不能发生水解反应,说明含有醛基不含酯基;Ⅲ.分子中含有4种不同化学环境的氢原子,说明结构高度对称,符合条件的有机物有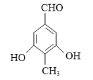 或
或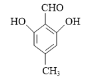 。
。


 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列有关叙述正确的是
A.16g由O2和O3组成的混合气体中的氧原子数为2NA
B.1molN2与足量H2充分反应生成NH3的分子数为2NA
C.1mol Fe溶于过量稀硝酸,转移的电子数为3NA
D.标准状况下,2.24L苯中含有的原子数为1.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)标准状况下,32gCH4和22.4LCO2的密度之比为_______;物质的量之比为______。
(2)将20gNaOH溶于水得2L溶液,则该NaOH溶液的物质的量浓度为_________;若从中取出100mLNaOH溶液,其中含有的Na+与____molNa2CO3含有的Na+数目相同。
(3)已知标准状况下,现有四种物质:
A.49g H2SO4 B.6.02×1023个H2O C.44.8L CO和CO2混合气体 D.6g H2
其中所含分子物质的量最小的是____________(填字母);所占体积最大的是________(填字母);若C中气体重量为64g,则该混合气体中CO和CO2的体积比为__________________。
(4)标准状况下,将aLHCl完全溶于100mL水,假设该溶液的密度为ρ g·mL-1,则所得盐酸溶液中溶质的物质的量为________________,溶液的物质的量浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制500mL 0.2mol/L的NaOH溶液。
(1)在下图所示仪器中,配制上述溶液肯定不需要的是_____________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是__________、____________。
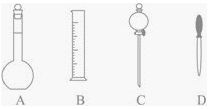
(2)填写下述过程中的空白;
具体步骤如下:
①计算需要称量NaOH固体的质量___________g;
②用托盘天平称量NaOH固体;
③将称好的NaOH固体放入烧杯中,加适量蒸馏水溶解、搅拌,并_________至室温;
④将NaOH溶液沿玻璃棒注入____________中;
⑤用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;
⑥将蒸馏水注入容量瓶,液面离刻度线下_______cm时,改用____________滴加蒸馏水至液面于刻度线相切;
⑦盖好瓶塞,反复上下颠倒,摇匀;
(3)经精确测量,最后所得溶液物质的量浓度为0.192mol/L,原因可能是_____________
A.使用滤纸称量NaOH固体;
B.溶解NaOH后的烧杯未经多次洗涤;
C.容量瓶中原来有少量蒸馏水;
D.称量时所用的砝码生锈;
E.未冷却直接转移至容量瓶,立即配好。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~H为中学化学中常见的物质,其转化关系如图所示,其中“〇”代表化合物,“□”代表单质,A为医学上治疗胃酸过多的一种药剂,G为淡黄色固体,C在通常状况下为无色液体,F为金属单质。请回答下列问题:
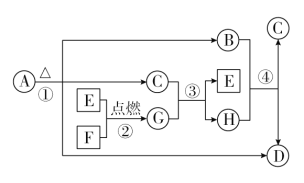
(1)G的化学式为________,G中阴阳离子个数比为______,每生成1mol G转移电子物质的量为________ 。
(2)A、D的水溶液均呈_______(填酸性、碱性或中性),反应①②③④中属于氧化还原反应的有_______个。
(3)写出下列反应的化学方程式。
A→B+C+D:__________________,
F+C:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,1.7g氨气所占的体积为__L,它与标准状况下__L硫化氢含有相同数目的氢原子。
(2)同温同压下,SO2与氦气的密度之比为___;若质量相同,则两种气体的体积之比为___;若体积相同,两种气体的质量之比为___。
(3)在标准状况下,①4gH2;②11.2LO2;③1molH2O中,所含分子数最多的是(填序号,下同)___,含原子数最多的是___,质量最大的是___,体积最小的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示渗透作用装置图,其中半透膜为膀胱膜,甲、丙装置中A、B、a、b溶液浓度分别用MA、MB、Ma、Mb表示,乙、丁装置分别表示一段时间后甲、丙装置的状态,液面上升的高度分别为h1、h2。如果A、B、a、b均为蔗糖溶液,且MA>MB,Ma=Mb>MA,则达到平衡后( )
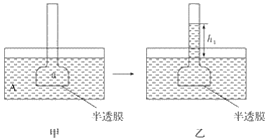
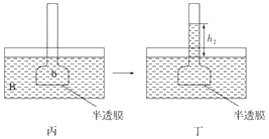
A. h1>h2、Ma>MbB. h1>h2、Ma<Mb
C. h1<h2、Ma<MbD. h1<h2、Ma>Mb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2+ +2OH- ![]() CH3COONH4 +3NH3+2Ag↓+H2O
CH3COONH4 +3NH3+2Ag↓+H2O
B. 苯酚钠溶液中通入少量CO2:CO2 +H2O+2C6H5O-→2C6H5OH+CO32-
C. 氯乙烷中滴入AgNO3溶液检验其中氯元素:Cl-+Ag+=AgCl↓
D. 乙酸滴入氢氧化铜悬浊液中:2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②KMnO4+ HCl(浓)= KCl+ MnCl2+ Cl2↑+ H2O(未配平)
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目(写在答题卡上)_________________________
(2)配平②___KMnO4+___HCl(浓)=___KCl+___MnCl2+___Cl2↑+___H2O 写出②的离子方程式________________________________;(友情提示:MnCl2易溶于水)②中氧化剂与还原剂分子数之比为_____________。
(3)反应②中氯化氢表现出的性质是________________________。
(4)Cl2、SO2和KMnO4的氧化性由强到弱的顺序为__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com