
【题目】A、B、X、Y、Z、W六种短周期主族元素,A是地壳中含量最多的金属元素,短周期主族元素中B的原子半径最大,X、Y、Z、W元素在周期表中的相对位置如图所示,其中Z元素原子最外层电子数是电子层数的2倍。请回答下列问题:
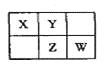
(1)W的最高价氧化物化学式是________________;Z的原子结构示意图为______。
(2)A、B各自最高价氧化物对应的水化物反应的化学方程式为_____________。
(3) AW3可用于净水,其原理是_____________。(请用离子方程式表示)
(4)工业合成X的简单气态氢化物是放热反应。下列措施中既能提高反应速率,又能提高原料转化率的是__________________。
a.升高温度
b.加入催化剂
c.将X的简单气态氢化物及时移离
d.增大反应体系的压强
(5)标准状况下,2.24L X的简单气态氢化物被100 mL l mol L-1X的最高价氧化物对应的水化物溶液吸收后,所得溶液中离子浓度从大到小的顺序是(用离子符号表示)_______________________________。
(6)WY2在杀菌消毒的同时,可将剧毒氰化物氧化成两种无毒气体而除去,写出用WY2(沸点9.9℃)氧化除去CN-的离子方程式____________________。
【答案】Cl2O7  Al(OH)3+NaOH=NaAl(OH)4 Al3++3 H2O
Al(OH)3+NaOH=NaAl(OH)4 Al3++3 H2O![]() Al(OH)3(胶体)+3H+ d c(NO3-)>c(H+)>c(NH4+)>c(OH-) 2ClO2+2CN-=N2+2Cl-+2CO2
Al(OH)3(胶体)+3H+ d c(NO3-)>c(H+)>c(NH4+)>c(OH-) 2ClO2+2CN-=N2+2Cl-+2CO2
【解析】
A是地壳中含量最多的金属元素,所以A为Al,短周期主族元素中B的原子半径最大,所以B为Na,根据图中位置,可知Z元素为三个电子层,最外层电子数是电子层数的2倍,可以推出Z原子核外排布是2,8,6,所以Z元素是S,以此为突破口,可以推出X为N,Y为O,W为Cl。
(1)W(Cl)的最高价氧化物化学式是Cl2O7;Z(S)的原子结构示意图为 。
。
(2)A、B各自最高价氧化物对应的水化物分别为Al(OH)3和NaOH,反应的化学方程式为Al(OH)3+NaOH=NaAl(OH)4。
(3)AW3(AlCl3)可用于净水,其原理是Al3+水解生成的Al(OH)3胶体能吸附水中的杂质,方程式为Al3++3 H2O![]() Al(OH)3(胶体)+3H+。
Al(OH)3(胶体)+3H+。
(4)合成氨气是放热反应,升高温度所以逆向移动,转化率变小;加入催化剂,只是加快化学反应速率,转化率不变;将氨气移走,虽然提高了转化率,但是化学反应速率降低;加大压强,加快了化学反应速率,正向移动,提高了原料的转化率,所以选d。
(5)标准状况下,2.24L(0.1mol)NH3与100 mL l mol L-1(0.1mol)HNO3反应恰好生成0.1molNH4NO3,因为NH4+会发生水解,所以c(NO3-)>c(NH4+)>c(H+)>c(OH-)。
(6)根据题意,反应物是ClO2和CN-,CN-中的N化合价是-3,C化合价是+2,再根据氧化成两种无毒气体,判断出无毒气体是N2和CO2,CN-中N和C化合价均升高,所以ClO2中Cl的化合价只有降低,判断出应该生成Cl-,然后用化合价升降法和电荷守恒配平:2ClO2+2CN-=N2+2Cl-+2CO2。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,向0.1mol·L1二元弱酸H2A的溶液中逐滴加入NaOH溶液,H2A、HA-、A2的物质的量分数随pH的变化如图所示。下列叙述正确的是( )
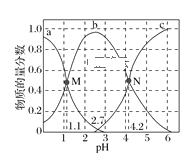
A.a曲线代表HA的物质的量分数随pH的变化
B.M点pH=1.1时,溶液中微粒浓度关系为c(H+)>c(HA)=c(H2A)
C.pH=2.7时,c(A2)+c(HA)+c(H2A)=0.1mol·L1
D.N点pH=4.2时,c(A2)=c(HA),溶液中不存在H2A分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型高效净水剂PAFC--聚合氯化铁铝![]()
![]() ,
,![]() ,
,![]() 广泛用于生活用水的净化和废水的净化
广泛用于生活用水的净化和废水的净化
![]() 为测定PAFC中Al的含量,采用如图所示流程进行.
为测定PAFC中Al的含量,采用如图所示流程进行.
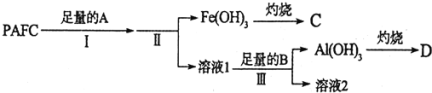
回答下列问题:
![]() 有关PAFC的说法正确的是 ______
有关PAFC的说法正确的是 ______
A PAFC中铁显![]() 价
价
B PAFC用于净化饮用水时,可以除去水中所有的有害物质
C PAFC用于净水时,比用相同量的氯化铝和氯化铁对水的pH改变小
D PAFC在强酸性或强碱性溶液中都能稳定存在
![]() 步骤I中的试剂A是 ______
步骤I中的试剂A是 ______ ![]() 填“氨水”或“氢氧化钠溶液”
填“氨水”或“氢氧化钠溶液”![]()
![]() 步骤III的离子方程式为 ______ .
步骤III的离子方程式为 ______ .
![]() 实验室进行“灼烧”时所需的陶瓷仪器有 ______ .
实验室进行“灼烧”时所需的陶瓷仪器有 ______ .
![]() 溶液2中存在的电荷守恒式为 ______ ;向溶液2中滴加少量NaOH镕液,则
溶液2中存在的电荷守恒式为 ______ ;向溶液2中滴加少量NaOH镕液,则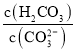 ______填“变大”、“变小”或“不变”
______填“变大”、“变小”或“不变”![]() .
.
![]() 已知C和某一金属在高温下发生反应可用于焊接钢轨,某同学在实验室中进行此反应,反应结束后将所得固体溶于足量的稀硫酸,滴加KSCN溶液无明显现象,由此该同学确定该固体混合物中无
已知C和某一金属在高温下发生反应可用于焊接钢轨,某同学在实验室中进行此反应,反应结束后将所得固体溶于足量的稀硫酸,滴加KSCN溶液无明显现象,由此该同学确定该固体混合物中无![]() ,他的判断是否正确?说明理由.
,他的判断是否正确?说明理由.![]() 可用文字或离子方程式解释理由
可用文字或离子方程式解释理由![]() .______ .
.______ .
![]() 有资料介绍:溶液中铝元素以氢氧化物
有资料介绍:溶液中铝元素以氢氧化物![]() 用
用![]() 表示
表示![]() 形式存在的pH范围是
形式存在的pH范围是![]() 现有A、B两种均含铝元素形成的某种离子溶液,其pH分别为1、13,两溶液等体积混合时反应的离子方程式为 ______ .
现有A、B两种均含铝元素形成的某种离子溶液,其pH分别为1、13,两溶液等体积混合时反应的离子方程式为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是学习化学的重要的思维方法,下列陈述Ⅰ及类比推理陈述Ⅱ均正确的是( )
陈述Ⅰ | 类比推理陈述Ⅱ | |
A | 单质的熔点Br2 < I2 | 单质的熔点Li < Na |
B | 工业上电解熔融的Al2O3得到铝单质 | 工业上电解熔融的MgO得到镁单质 |
C | 还原性:I- > Br- | 还原性:P3- > N3- |
D | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型锂-空气电池具有能量密度高的优点,可以用作新能源汽车的电源,其结构如图所示,其中固体电解质只允许Li+通过。下列说法正确的是
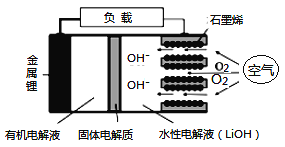
A. Li+穿过固体电解质向正极移动而得到LiOH溶液
B. 放电时,当外电路中有1 mol e-转移时,水性电解液离子总数增加NA
C. 应用该电池电镀铜,阴极质量增加64 g,理论上将消耗11.2 L O2
D. 放电时,负极反应式:Li-e-+OH-=LiOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在两份相同的 Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、 NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析不正确的是( )
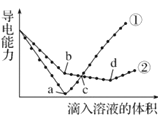
A.b点,水电离产生的c(H+)< 10-7 mol/LB.①代表滴加H2SO4溶液的变化曲线
C.a、d两点对应的溶液均显中性D.c点,两溶液中含有相同量的 OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物分子的结构简式如图所示,下列相关叙述正确的是( )

A.该有机化合物含有3种官能团
B.该有机物分子中最多有12个碳原子在同一平面内
C.该有机物分子中最多有6个碳原子共线
D.该有机物分子中最多有14个碳原子在同一平面内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL0.10mol·L-1HClO溶液中逐滴加入0.10mol·L-1NaOH溶液,滴定过程中溶液中水电离出的c(H+)变化曲线如图所示。下列说法正确的是
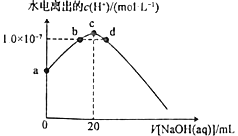
A.可用pH试纸测定a点溶液的pH
B.b、c、d三点溶液中离子、分子种类不同
C.a、b、c、d四点溶液中水的电离程度:c>b=d>a
D.d点溶液中c(Na+)=c(ClO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com