
【题目】一种制备高效漂白剂NaClO2的实验流程如图所示,反应I中发生的反应为3NaClO3+4SO2+3H2O====2ClO2+Na2SO4+3H2SO4+NaCl,下列说法中正确的是
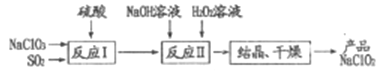
A. 反应Ⅱ中H2O2做还原剂
B. 产品中含有SO42-、Cl-
C. NaClO2的漂白原理与SO2相同
D. 实验室进行结晶操作通常在坩埚中进行
【答案】A
【解析】
A. 反应I中发生的反应为3NaClO3+4SO2+3H2O=2ClO2+Na2SO4+3H2SO4+NaCl,反应产生的ClO2气体进入反应II装置,发生反应:2ClO2+2H2O2+2NaOH=2NaClO2+O2+2H2O,H2O2中氧元素的化合价由反应前的-1变为反应后中O2中的0价,化合价升高,失去电子,H2O2作还原剂,A正确;
B.反应II是在NaOH溶液中进行,操作过程没有经过洗涤步骤,因此得到的NaClO2中可能混有NaOH引入杂质离子OH-,不可能含SO42-、Cl-,B错误;
C. NaClO2中Cl元素化合价为+3价,该物质具有强的氧化性,因而具有漂白性,NaClO2的漂白是氧化漂白;而SO2能与某些有色物质结合,产生不稳定的无色物质,因此二者的漂白原理不相同,C错误;
D. 实验室进行结晶操作通常在蒸发皿中进行,坩埚是灼烧使用的仪器,D错误;
故本题合理选项是A。


科目:高中化学 来源: 题型:
【题目】常温下pH为2的盐酸,下列叙述正确的是( )
A.将10mL该溶液稀释至100mL后,pH=4
B.向该溶液中加入等体积pH为12的氨水恰好完全中和
C.该溶液中盐酸电离出的c(H+)与水电离出的c(H+)之比为1010:1
D.该溶液中由水电离出的c(H+)水×c(OH-)水=1×10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列叙述中正确的是
A.1mol 葡萄糖分子含有的羟基数目为6NA
B.标准状况下,2.24 L Cl2溶于足量的水中充分反应后,溶液中Cl-数为0.1NA
C.100g 46%的乙醇溶液中,含H-O键的数目为NA
D.7 g CO(NH2)2与23 g乙酸组成的混合物中含氢原子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学上常用AG表示溶液中的lg![]() 。25℃时,用0.100molL-1的NaOH溶液滴定20.00mL 0.100molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
。25℃时,用0.100molL-1的NaOH溶液滴定20.00mL 0.100molL-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
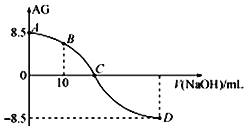
A. D点溶液的pH=11.25
B. C点之前溶液显碱性,C点之后溶液显酸性
C. C点时,加入NaOH溶液的体积为20mL
D. 25℃时,HNO2的电离常数Ka=1.0×10-5.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
![]() 浓硫酸与木炭在加热条件下反应的化学方程式是 ______ 。
浓硫酸与木炭在加热条件下反应的化学方程式是 ______ 。
![]() 试用图所列各种装置设计一个实验来验证上述反应所产生的各种产物。
试用图所列各种装置设计一个实验来验证上述反应所产生的各种产物。
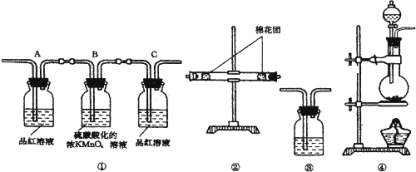
这些装置的连接顺序,按产物气流从左到右的方向是![]() 填装置的编号
填装置的编号![]() : ______
: ______ ![]() ______
______ ![]() ______
______ ![]() ______ 。
______ 。
![]() 装置
装置![]() 中所装的固体药品是 ______ ,可验证的产物是 ______ 。
中所装的固体药品是 ______ ,可验证的产物是 ______ 。
![]() 装置
装置![]() 中所盛溶液是 ______ ,可以验证的产物是 ______ 。
中所盛溶液是 ______ ,可以验证的产物是 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu的单质和合金在生活、生产中有着广泛的应用。回答下列问题:
(1)Cu的基态原子价电子排布式为___。
(2)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是___,反应的化学方程式为___。
(3)配离子Cu(CN)32-中,中心离子的杂化类型是___,该配离子的空间构型为___;CN-中配位原子是___(填名称)。
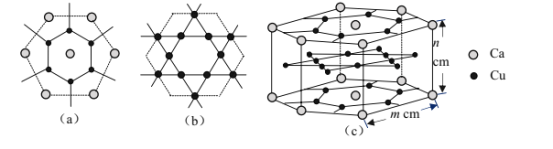
(4)CaCux合金可看作由如图所示的(a)、(b)两种原子层交替堆积排列而成。(a)是由Cu和Ca共同组成的层,层中Cu—Cu之间由实线相连;(b)是完全由Cu原子组成的层,Cu—Cu之间也由实线相连。图中虚线构建的六边形,表示由这两种层平行堆积时垂直于层的相对位置;(c)是由(a)和(b)两种原子层交替堆积成CaCux合金的晶体结构图。在这种结构中,同一层的Ca—Cu距离为294pm,相邻两层的Ca—Cu距离为327pm。
①该晶胞中Ca有___个Cu原子配位(不一定要等距最近)。
②同一层中,Ca原子之间的最短距离是___pm,设NA为阿伏加德罗常数的值,CaCu晶体的密度是___g/cm3(用含m、n的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸钠是一种常见的食品防腐剂.实验室制备苯甲酸的反应装置图和有关数据如下:
相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
甲苯 | 92 | -94.9 | 110.6 | 难溶于水 |
苯甲酸 | 122 | 122.13 | 249 | 微溶于水 |
苯甲酸钠 | 144 | — | 249.3 | 易溶于水 |

按下列合成步骤回答问题:
(1)制备苯甲酸
在三颈瓶中加入4mL甲苯和20mL蒸馏水,再加入5mL浓硫酸,放入碎瓷片后,加热至沸腾,加入![]() 高锰酸钾,加热到甲苯层消失。将三颈瓶在冰水浴中冷却,分离出苯甲酸.
高锰酸钾,加热到甲苯层消失。将三颈瓶在冰水浴中冷却,分离出苯甲酸.
(2)制备苯甲酸钠
控制温度为70℃,向三颈瓶中加入![]() 苯甲酸和适量的
苯甲酸和适量的![]() 的碳酸钠溶液,充分反应后停止加热.在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体.
的碳酸钠溶液,充分反应后停止加热.在深色的溶液中加入活性炭,并将反应混合物过滤,得到无色透明的苯甲酸钠溶液,将滤液转入蒸发皿中,加热蒸发、冷却结晶,过滤、洗涤、干燥制得苯甲酸钠晶体.
①球形冷凝管的作用是 ______ ,其进水口是 ______ ![]() 填“a”或“b”
填“a”或“b”![]() .
.
②三颈瓶中反应的离子方程式 ______ .
③分离苯甲酸选用的玻璃仪器是 ______ ![]() 填标号
填标号![]()
A分液漏斗B玻璃棒C烧杯D漏斗E蒸馏烧瓶F直形冷凝管
④分离出的苯甲酸晶体中可能含有的杂质是 ______ ,为进一步提纯,应采用的方法是 ______ .
⑤控制温度为70℃的方法是 ______ .
⑥加入活性炭的作用是 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列叙述正确的是
A.5. 6 L由CO2和O2组成的混合气体中的分子数为0. 25NA
B.5. 6 g铁与足量的稀硫酸完全反应转移的电子数为0. 2NA
C.0. 5 mol L-1的BaCl2溶液中含有Cl-的数目为NA
D.10 g质量分数为17%的H2O2溶液中含氧原子的数目为0. 1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是
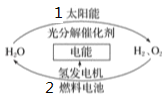
A. 过程1是放热反应
B. 过程2可将化学能转化为电能
C. 氢能源可从自然界直接获取,是一次能源
D. 氢气不易贮存和运输,无开发利用价值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com